名校
解题方法
1 . 下列热化学方程式及有关应用的叙述中,正确的是
A.甲烷的燃烧热的 为 为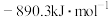 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: 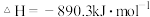 |
B.已知强酸与强碱在稀溶液里反应的中和热的 为 为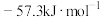 ,则 ,则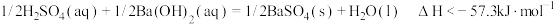 |
C. 、 、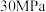 下,将 下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热 ,放热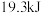 ,其热化学方程式为:N2(g)+3H2(g) ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) 2NH3(g) 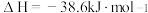 |
D.已知 、 、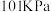 条件下: 条件下: 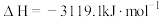 ,则 ,则 比 比 稳定 稳定 |
您最近一年使用:0次
2022-08-25更新
|
468次组卷
|
11卷引用:湖南省衡阳市常宁五中2020届高三11月月考化学试题
湖南省衡阳市常宁五中2020届高三11月月考化学试题江西省宜春市奉新县第一中学2020届高三上学期第四次月考化学试题河北省衡水市第十四中学2019-2020学年高二上学期第三次调研考试化学试题(已下线)1.1.2 热化学方程式(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)辽宁省沈阳市法库县高级中学2020-2021学年高二9月月考化学试题(已下线)第9单元 化学反应中的能量变化(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷江西省宜春市万载中学2021-2022学年高一上学期第二次月考化学试题上海市进才中学2022-2023学年高二上学期10月阶段测试化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高二10月月考化学试题广东省惠州市第一中学2022-2023学年高二上学期第一次月考化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高二上学期期中考试化学试题
名校
2 . 以NA代表阿伏加德罗常数,则关于热化学方程式:C2H2(g)+5/2O2(g)→2CO2(g)+H2O(l)△H=-1300kJ/mol的说法中,正确的是
| A.当10NA个电子转移时,该反应放出1300kJ的能量 |
| B.当1NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.当2NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.当10NA个碳氧共用电子对生成时,放出1300kJ的能量 |
您最近一年使用:0次
2022-08-20更新
|
385次组卷
|
10卷引用:【全国百强校】黑龙江省大庆实验中学2018-2019学年高二上学期10月月考化学试题
【全国百强校】黑龙江省大庆实验中学2018-2019学年高二上学期10月月考化学试题江西省赣县第三中学2018-2019学年高二上学期10月月考化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高一下学期期中考试化学试题广东省蕉岭县蕉岭中学2019-2020学年高二上学期第一次段考化学试题山东省烟台市栖霞市2019-2020学年高二下学期3月网上统一月考化学试题人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热2河北省张家口宣化一中2020-2021学年高二下学期3月月考化学试题(已下线)第一章 化学反应与能量 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)章末检测卷(一)化学反应与能量转化
名校
解题方法
3 . 回答下列问题:
(1)在25℃、101kPa,2gC2H2完全燃烧生成液态水放出99.6kJ热量,写出表示乙炔燃烧热的热化学方程式_______ 。
(2)在两容器A和B,A为恒温恒容容器,B为恒温恒压容器,初始体积均为2L,起始时都充入1molN2和3molH2,发生反应:N2(g)+3H2(g=2NH3(g) △H=-akJ·mol-1,A容器2min时达平衡,放出bkJ热量,B容器达平衡放出ckJ热量。

①a_______ b,b_______ c(填“<”、“=”或“>”)
②B容器达平衡的时间_______ 2min(填“<”、“=”或“>”)
(3)已知①C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ·mol-1
③4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7kJ·mol-1
则Fe3O4(s)=3Fe(s)+2O2(g) △H=_______ 。
(1)在25℃、101kPa,2gC2H2完全燃烧生成液态水放出99.6kJ热量,写出表示乙炔燃烧热的热化学方程式
(2)在两容器A和B,A为恒温恒容容器,B为恒温恒压容器,初始体积均为2L,起始时都充入1molN2和3molH2,发生反应:N2(g)+3H2(g=2NH3(g) △H=-akJ·mol-1,A容器2min时达平衡,放出bkJ热量,B容器达平衡放出ckJ热量。

①a
②B容器达平衡的时间
(3)已知①C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ·mol-1
③4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7kJ·mol-1
则Fe3O4(s)=3Fe(s)+2O2(g) △H=
您最近一年使用:0次
解题方法
4 . 乙烷燃烧热为Q kJ·mol-1,则下列热化学方程式中正确的是
| A.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) △H=-2Q kJ·mol-1 |
| B.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H=+2Q kJ·mol-1 |
C.C2H6(g)+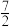 O2(g)=2CO2(g)+3H2O(g) △H=-Q kJ·mol-1 O2(g)=2CO2(g)+3H2O(g) △H=-Q kJ·mol-1 |
| D.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H=-2Q kJ·mol-1 |
您最近一年使用:0次
2022-07-26更新
|
1032次组卷
|
5卷引用:江西宜春市第九中学2020-2021学年高二上学期第一次月考化学试题
江西宜春市第九中学2020-2021学年高二上学期第一次月考化学试题(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)山西省晋中市平遥县第二中学校2022-2023学年高二上学期8月质检化学试题贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题(已下线)【知识图鉴】单元讲练测选择性必修1第1单元02基础练
名校
解题方法
5 . 肼(N2H4)是一种高效清洁的火箭燃料。25℃、101kPa时,0.25molN2H4(g)完全燃烧生成氮气和气态水,放出133.5kJ热量。下列说法正确的是
| A.该反应的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534kJ·mol-1 |
| B.N2H4的燃烧热534kJ·mol-1 |
| C.相同条件下,1molN2H4(g)所含能量高于1molN2(g)和2molH2O(g)所含能量之和 |
| D.该反应是放热反应,反应的发生不需要克服化学键 |
您最近一年使用:0次
2022-07-26更新
|
544次组卷
|
5卷引用:甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题
甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)山西省晋中市平遥县第二中学校2022-2023学年高二上学期8月质检化学试题黑龙江省鸡西市第四中学2022-2023学年高二上学期第一次月考化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高二上学期期中考试化学试题
6 . 请回答以下有关能源的问题:
(1)未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是___________
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
(2)打火机使用的燃料一般是丙烷(C3H8)。
①已知11g丙烷(C3H8)在298K和101Kpa条件下完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式___________ ;
②丙烷在一定条件下发生脱氢反应可以得到丙烯。
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) ΔH1=+156.6kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) ΔH2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的ΔH=___________
(3)已知:H—H键的键能为436kJ·mol-1,H—N键的键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1
①请计算出N≡N键的键能为___________ 。
②若向处于上述热化学方程式相同温度和体积一定的容器中,通入1molN2和3molH2,充分反应后,恢复原温度时放出的热量___________ 92.4kJ(填大于或小于或等于)。
(1)未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是___________
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ | C.③⑤⑥⑦⑧ | D.③④⑤⑥⑦⑧ |
①已知11g丙烷(C3H8)在298K和101Kpa条件下完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式
②丙烷在一定条件下发生脱氢反应可以得到丙烯。
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) ΔH1=+156.6kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) ΔH2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的ΔH=
(3)已知:H—H键的键能为436kJ·mol-1,H—N键的键能为391kJ·mol-1,根据化学方程式:N2+3H2⇌2NH3 ΔH=-92.4kJ·mol-1
①请计算出N≡N键的键能为
②若向处于上述热化学方程式相同温度和体积一定的容器中,通入1molN2和3molH2,充分反应后,恢复原温度时放出的热量
您最近一年使用:0次
2022-07-22更新
|
1501次组卷
|
9卷引用:山东省济宁市泗水县2019-2020学年高二上学期期中考试化学试题
山东省济宁市泗水县2019-2020学年高二上学期期中考试化学试题辽宁省辽阳市辽阳县集美中学2020-2021学年高二上学期第一次月考化学试题山东省邹城市第一中学2020-2021学年高二上学期期中质量检测化学试题河北省唐山市遵化市2020-2021学年高二上学期期中考试化学试题福建省宁德第一中学2020-2021学年高二上学期第一次月考化学试题(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)福建省福安市第一中学2022-2023学年高二上学期第一次月考化学试题山西省大同市第一中学校2023-2024学年高二上学期10月月考化学试题上海市东华大学附属奉贤致远中学2023-2024学年高二上学期期中考试化学(等级)试题
解题方法
7 . 完成下列问题
(1)已知碳的燃烧热为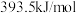 。写出碳燃烧的热化学方程式:
。写出碳燃烧的热化学方程式:_______ 。
(2)试回答:常温下 的盐酸溶液
的盐酸溶液
_______ 。稀释100倍后所得溶液
_______ 4(填“>”“=”或“<”)。
(3)将铜片、锌片和稀硫酸溶液用导线连接成闭合回路可以形成原电池。负极发生_______ (填“氧化”或“还原”)反应,电极反应方程式为:_______ 。
(1)已知碳的燃烧热为
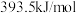 。写出碳燃烧的热化学方程式:
。写出碳燃烧的热化学方程式:(2)试回答:常温下
 的盐酸溶液
的盐酸溶液

(3)将铜片、锌片和稀硫酸溶液用导线连接成闭合回路可以形成原电池。负极发生
您最近一年使用:0次
名校
8 . 下列热化学方程正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A.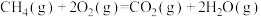 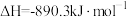 (燃烧热) (燃烧热) |
B. 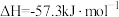 (中和热) (中和热) |
C. 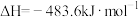 (反应热) (反应热) |
D.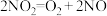 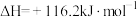 (反应热) (反应热) |
您最近一年使用:0次
2022-07-01更新
|
327次组卷
|
6卷引用:2016-2017学年四川省资阳市高二上学期期末化学试卷
名校
解题方法
9 . 下列热化学方程式中,正确的是
| A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| C.HCl和NaOH反应的中和热△H=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol-1 |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 |
您最近一年使用:0次
2022-05-14更新
|
371次组卷
|
17卷引用:辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题
辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题安徽省安庆市怀宁县第二中学2019-2020学年高二下学期期中线上检测化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)1.1.2 反应热的测量和计算(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题西藏自治区拉萨市拉萨中学2020-2021学年高二第一次月考理综化学试题甘肃省武威第八中学2020-2021学年高二上学期月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期开学考试化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期10月月考化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记福建省南安市柳城中学2020-2021学年高一下学期期中考试化学试题江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷B卷化学试题湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题(已下线)第04讲 燃料燃烧释放的能量与氢燃料的发展前景-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)辽宁省沈阳市第一二〇中学2020-2021学年高一下学期期中化学试题新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二上学期期末考试化学试题
名校
10 . 下列有关说法正确的是
| A.已知:①C(s石墨)+O2(g)=CO2(g)△H1=-393.5mol/L;②C(s金刚石)+O2(g)=CO2(g)△H2=-395.0mol/L,则石墨比金刚石稳定 |
| B.在101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ热量,H2燃烧热为-285.8kJ·mol-1 |
| C.中和热实验测定时,可以用铜棒代替易碎的环形玻璃搅拌棒 |
| D.在一定温度和压强下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)⇌2NH3(g)△H=﹣38.6kJ/mol |
您最近一年使用:0次
2022-04-20更新
|
224次组卷
|
2卷引用:辽宁省沈阳市第二十中学2019-2020学年高一下学期第一次月考化学试题



