1 . 烟气脱硝技术是环境科学研究的热点。实验室模拟 将烟气中的
将烟气中的 深度氧化为
深度氧化为 ,并进一步将
,并进一步将 转化获得含氮产品,流程示意图如下。
转化获得含氮产品,流程示意图如下。
i.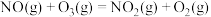
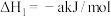
ii.

iii.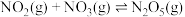

(1) 被
被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:


___________ 
(2)一定条件下,不同温度时, 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。
___________  (填“>”或“<”)。
(填“>”或“<”)。
②8s时, 的浓度不同的原因是
的浓度不同的原因是___________ 。
(3)一定条件下,NO的初始浓度为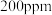 时,不同反应时间,深度氧化器中
时,不同反应时间,深度氧化器中 的浓度随
的浓度随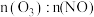 的变化如图所示。反应过程中
的变化如图所示。反应过程中 的浓度极低。
的浓度极低。 时,深度氧化器中发生的反应主要是
时,深度氧化器中发生的反应主要是___________ (填“i”“ii”或“iii”)。
② 时,
时, 的浓度随
的浓度随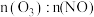 变化的原因是
变化的原因是___________ 。
(4) 且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是
且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是___________ 。
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。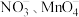 的还原产物分别是
的还原产物分别是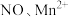 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为___________  。
。
 将烟气中的
将烟气中的 深度氧化为
深度氧化为 ,并进一步将
,并进一步将 转化获得含氮产品,流程示意图如下。
转化获得含氮产品,流程示意图如下。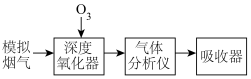
i.
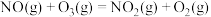
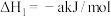
ii.


iii.
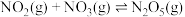

(1)
 被
被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:


(2)一定条件下,不同温度时,
 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。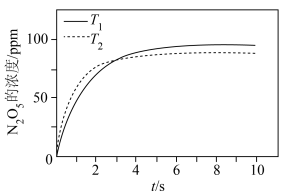

 (填“>”或“<”)。
(填“>”或“<”)。②8s时,
 的浓度不同的原因是
的浓度不同的原因是(3)一定条件下,NO的初始浓度为
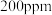 时,不同反应时间,深度氧化器中
时,不同反应时间,深度氧化器中 的浓度随
的浓度随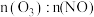 的变化如图所示。反应过程中
的变化如图所示。反应过程中 的浓度极低。
的浓度极低。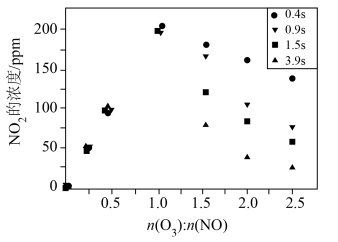
 时,深度氧化器中发生的反应主要是
时,深度氧化器中发生的反应主要是②
 时,
时, 的浓度随
的浓度随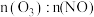 变化的原因是
变化的原因是(4)
 且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是
且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。
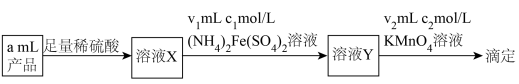
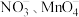 的还原产物分别是
的还原产物分别是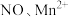 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
解题方法
2 . 我国科学家研发的“液态阳光”计划通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
已知: 产率
产率
(1)制备甲醇的主反应:
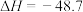 kJ·mol
kJ·mol 。该过程中还存在一个生成CO的副反应,结合反应:
。该过程中还存在一个生成CO的副反应,结合反应:
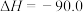 kJ·mol
kJ·mol ,写出该副反应的热化学方程式:
,写出该副反应的热化学方程式:____ 。
(2)为同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,反应条件应选择
的平衡产率,反应条件应选择____ 。
将 和
和 按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
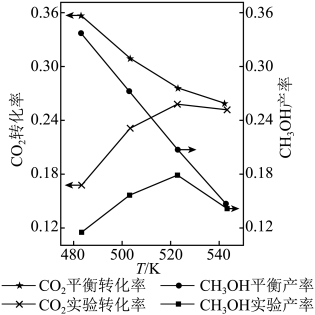
(3)①催化剂活性最好的温度为_____ (填字母序号)。
a.483K b.503K c.523K d.543K
②温度由483K升到523K,_____ (填“主反应”或“副反应”)的反应速率受温度影响更大。
③温度由523K升到543K, 的平衡转化率和
的平衡转化率和 的实验产率均降低,解释原因:
的实验产率均降低,解释原因:_____ 。
④如图,a点对应的坐标为(523K,0.26),b点对应的坐标为(523K,0.18),在523K温度下,b点对应的 的百分含量为
的百分含量为_____ 。
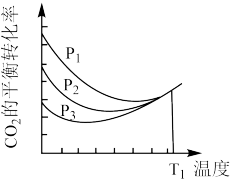
(4)不同压强下,按照 投料,
投料, 平衡转化率随温度变化关系如图所示。
平衡转化率随温度变化关系如图所示。 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的原因是
时的原因是_____ 。
已知:
 产率
产率
(1)制备甲醇的主反应:

 kJ·mol
kJ·mol 。该过程中还存在一个生成CO的副反应,结合反应:
。该过程中还存在一个生成CO的副反应,结合反应:
 kJ·mol
kJ·mol ,写出该副反应的热化学方程式:
,写出该副反应的热化学方程式:(2)为同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,反应条件应选择
的平衡产率,反应条件应选择将
 和
和 按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
(3)①催化剂活性最好的温度为
a.483K b.503K c.523K d.543K
②温度由483K升到523K,
③温度由523K升到543K,
 的平衡转化率和
的平衡转化率和 的实验产率均降低,解释原因:
的实验产率均降低,解释原因:④如图,a点对应的坐标为(523K,0.26),b点对应的坐标为(523K,0.18),在523K温度下,b点对应的
 的百分含量为
的百分含量为(4)不同压强下,按照
 投料,
投料, 平衡转化率随温度变化关系如图所示。
平衡转化率随温度变化关系如图所示。 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的原因是
时的原因是
您最近一年使用:0次
3 . 化学链燃烧( )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
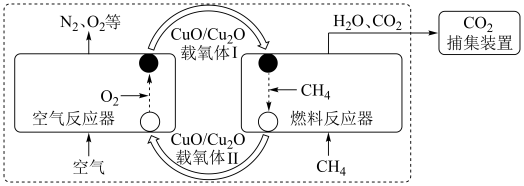
空气反应器与燃料反应器中发生的反应分别为:
①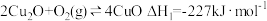
②
(1)反应

_______  。
。
(2)反应②的平衡常数表达式
_______ 。
(3)氧的质量分数:载氧体Ⅰ_______ (填“>”“=”或“<”)载氧体Ⅱ。
(4)往盛有 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。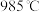 时
时 的平衡转化率
的平衡转化率
_______ (保留2位有效数字)。
(5)根据下图, 随温度升高而增大的原因是
随温度升高而增大的原因是_______ 。反应温度必须控制在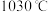 以下,原因是
以下,原因是_______ 。

(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。
由表中数据判断:使用_______ (填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为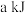 、
、 ,则a
,则a_______ b(填“>”“=”或“<”)。
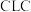 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
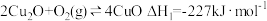
②

(1)反应


 。
。(2)反应②的平衡常数表达式

(3)氧的质量分数:载氧体Ⅰ
(4)往盛有
 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。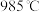 时
时 的平衡转化率
的平衡转化率
(5)根据下图,
 随温度升高而增大的原因是
随温度升高而增大的原因是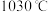 以下,原因是
以下,原因是
(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的
 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。| 载氧体掺杂物质 | 氧化铝 | 膨润土 |
活化能/ |  | 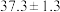 |
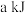 、
、 ,则a
,则a
您最近一年使用:0次
2021-11-09更新
|
5532次组卷
|
7卷引用:北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题
北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题2021年新高考福建化学高考真题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题(已下线)专题17 原理综合题(已下线)专题17 原理综合题福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题
4 . 页岩气中含有较多的乙烷,可将其转化为更有工业价值的乙烯。
(1) 二氧化碳氧化乙烷制乙烯。
将C2H6和CO2按物质的量之比为1∶1通入反应器中,发生如下反应:
ⅰ.C2H6(g) C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol− 1
C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol− 1
ⅱ.CO2(g) + H2(g) CO(g) + H2O(g) ΔH2=+41.2 kJ·mol− 1
CO(g) + H2O(g) ΔH2=+41.2 kJ·mol− 1
ⅲ.C2H6(g) +CO2(g) C2H4(g) +CO(g) +H2O(g) ΔH3
C2H4(g) +CO(g) +H2O(g) ΔH3
①用ΔH1、ΔH2计算ΔH3=______ kJ·mol−1。
②反应ⅳ:C2H6(g) 2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:
2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:__ 。
③二氧化碳氧化乙烷制乙烯的研究热点之一是选择催化剂,相同反应时间,不同温度、不同催化剂的数据如下表(均未达到平衡状态):
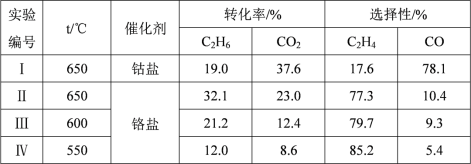
【注】C2H4 选择性:转化的乙烷中生成乙烯的百分比。
CO 选择性:转化的 CO2 中生成 CO 的百分比。
对比Ⅰ和Ⅱ,该反应应该选择的催化剂为__ ,理由是__ 。实验条件下,铬盐作催化剂时,随温度升高,C2H6 的转化率升高,但 C2H4 的选择性降低,原因是__ 。
(2) 利用质子传导型固体氧化物电解池将乙烷转化为乙烯,示意图如图:
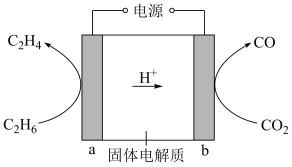
①电极 a 与电源的______ 极相连。
②电极 b 的电极反应式是______ 。
(1) 二氧化碳氧化乙烷制乙烯。
将C2H6和CO2按物质的量之比为1∶1通入反应器中,发生如下反应:
ⅰ.C2H6(g)
 C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol− 1
C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol− 1 ⅱ.CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH2=+41.2 kJ·mol− 1
CO(g) + H2O(g) ΔH2=+41.2 kJ·mol− 1 ⅲ.C2H6(g) +CO2(g)
 C2H4(g) +CO(g) +H2O(g) ΔH3
C2H4(g) +CO(g) +H2O(g) ΔH3①用ΔH1、ΔH2计算ΔH3=
②反应ⅳ:C2H6(g)
 2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:
2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:③二氧化碳氧化乙烷制乙烯的研究热点之一是选择催化剂,相同反应时间,不同温度、不同催化剂的数据如下表(均未达到平衡状态):
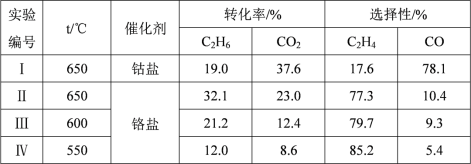
【注】C2H4 选择性:转化的乙烷中生成乙烯的百分比。
CO 选择性:转化的 CO2 中生成 CO 的百分比。
对比Ⅰ和Ⅱ,该反应应该选择的催化剂为
(2) 利用质子传导型固体氧化物电解池将乙烷转化为乙烯,示意图如图:

①电极 a 与电源的
②电极 b 的电极反应式是
您最近一年使用:0次
2020-04-08更新
|
554次组卷
|
5卷引用:北京市西城区2020届高三一模化学试题
北京市西城区2020届高三一模化学试题北京市第十五中学2023-2024学年高三上学期期中考试化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:化学反应原理北京市顺义牛栏山第一中学2022届高三下学期保温练习化学试题北京市第一0一中学2022-2023学年高二下学期3月统练化学试题
5 . 直接排放含SO2的烟气会危害环境。利用工业废碱渣(主要成分Na2CO3)可吸收烟气中的SO2并制备无水Na2SO3,其流程如图1。

已知:H2SO3、HSO3-、SO32-在水溶液中的物质的量分数随pH的分布如图2, Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。


(1)Na2CO3溶液显碱性,用离子方程式解释其原因:______________ 。
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为______________ 。
②NaHSO3溶液中c(SO32-)>c(H2SO3),结合方程式解释其原因:____________ 。
③已知下列反应:
SO2(g)+2OH-(aq)=SO32-(aq)+H2O(l)
CO2(g)+2OH-(aq)=CO32-(aq)+H2O(l)
2HSO3-(aq)=SO32-(aq)+SO2(g)+H2O(l)
吸收塔中Na2CO3溶液吸收SO2生成HSO3-的热化学方程式是______________ 。
④吸收塔中的温度不宣过高,可能的原因是______________ (写出1种即可)。
(3)制备无水Na2SO3:将中和塔中得到的Na2SO3溶液______________ (填操作),过滤出的固体用无水乙醇洗涤、干燥,得无水Na2SO3固体。

已知:H2SO3、HSO3-、SO32-在水溶液中的物质的量分数随pH的分布如图2, Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。


(1)Na2CO3溶液显碱性,用离子方程式解释其原因:
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为
②NaHSO3溶液中c(SO32-)>c(H2SO3),结合方程式解释其原因:
③已知下列反应:
SO2(g)+2OH-(aq)=SO32-(aq)+H2O(l)

CO2(g)+2OH-(aq)=CO32-(aq)+H2O(l)

2HSO3-(aq)=SO32-(aq)+SO2(g)+H2O(l)

吸收塔中Na2CO3溶液吸收SO2生成HSO3-的热化学方程式是
④吸收塔中的温度不宣过高,可能的原因是
(3)制备无水Na2SO3:将中和塔中得到的Na2SO3溶液
您最近一年使用:0次
2019-12-21更新
|
323次组卷
|
3卷引用:【区级联考】北京市西城区2019届高三上学期期末考试化学试题
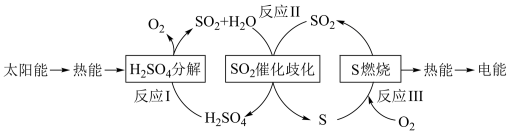
6 . 近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:_________________________________________ 。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。
p2_______ p 1(填“>”或“<”),得出该结论的理由是________________ 。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+===S↓+2I2+2H2O
ii.I2+2H2O+_________ ===_________ +_______ +2I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=__________ 。
②比较A、B、C,可得出的结论是______________________ 。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________ 。
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。
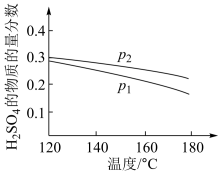
p2
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+===S↓+2I2+2H2O
ii.I2+2H2O+
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
A | B | C | D | |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
您最近一年使用:0次
2018-06-09更新
|
6530次组卷
|
28卷引用:北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题
北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题北京市第八中学2022-2023学年高二上学期期末考试化学试题北京市铁路第二中学2023-2024学年高二上学期期中考试化学试题2018年全国普通高等学校招生统一考试化学(北京卷)(已下线)2018年高考题及模拟题汇编 专题14 化学反应原理综合【校级联考】安徽省江南片2019届高三上学期入学摸底考试化学试题陕西安康市紫阳县紫阳中学2019届高三上学期入学调研考试化学试题福建省泉州第五中学2019届高三入学调研考试化学试题【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期10月月考化学试题江西省丰城中学2018-2019学年高一上学期课改期末考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题福建省福州市第三中学2019-2020学年高三10月月考化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》(已下线)考点12 化学反应速率化学平衡——《备战2020年高考精选考点专项突破题集》2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷四川省成都市实验中学2019-2020学年高三下学期第三次周测化学试题(已下线)专题6.3 化学原理题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率北京东城区2019-2020学年高二下学期期中考试化学试题(已下线)北京市第四中学2021-2022学年高三上学期期中考试化学试题安徽省黄山市屯溪第一中学2021-2022学年高二上学期期中考试化学试题北京市陈经纶中学2022-2023学年高二10月月考化学试题(已下线)化学(上海C卷)-学易金卷:2023年高考第一次模拟考试卷广西壮族自治区钦州市第四中学2022-2023学年高一下学期3月月考化学试卷北京市第一○一中学2023-2024学年高二上学期统练一化学试题浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷北京市广渠门中学2023-2024学年高二上学期期中考试化学试题 10-2023新东方高二上期中考化学



