解题方法
1 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
(1)已知: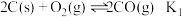

 (其中
(其中 、
、 、
、 为对应化学反应的平衡常数)
为对应化学反应的平衡常数)
①则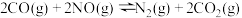 的平衡常数为K,则
的平衡常数为K,则
_______ (用 、
、 、
、 表示)。
表示)。
②在一个恒温恒容的密闭容器中发生反应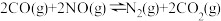 。能表明反应已达到平衡状态的标志有
。能表明反应已达到平衡状态的标志有_______ (填字母)。
A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量保持不变
E.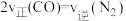 F.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应 ,
, 和
和 的物质的量变化如表所示。
的物质的量变化如表所示。
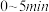 内,以
内,以 表示的平均反应速率
表示的平均反应速率
_______ ,最终达平衡时 的浓度
的浓度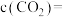
_______ ,平衡时 的转化率
的转化率
_______ ,写出该反应平衡常数的表达式
_______ ,并求该温度 下的平衡常数
下的平衡常数
_______ 。
(1)已知:
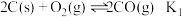

 (其中
(其中 、
、 、
、 为对应化学反应的平衡常数)
为对应化学反应的平衡常数)①则
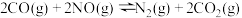 的平衡常数为K,则
的平衡常数为K,则
 、
、 、
、 表示)。
表示)。②在一个恒温恒容的密闭容器中发生反应
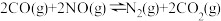 。能表明反应已达到平衡状态的标志有
。能表明反应已达到平衡状态的标志有A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量保持不变
E.
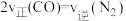 F.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应 ,
, 和
和 的物质的量变化如表所示。
的物质的量变化如表所示。| 条件 | 保持温度为 | ||||||
时间/ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
物质的量/ | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
物质的量/ | 0 | 0.30 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
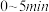 内,以
内,以 表示的平均反应速率
表示的平均反应速率
 的浓度
的浓度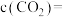
 的转化率
的转化率

 下的平衡常数
下的平衡常数
您最近一年使用:0次
2023-02-18更新
|
135次组卷
|
3卷引用:广西北海市2022-2023学年高二上学期期末考试化学试题
广西北海市2022-2023学年高二上学期期末考试化学试题福建省福州市三校2022-2023学年高二上学期期中联考化学试题(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
2 . 根据要求,回答下列问题:
(1)已知甲烷的燃烧热为 ,
,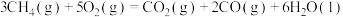
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式:_______ ,若 、
、 键的键能分别为
键的键能分别为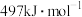 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是_______ ;1mol 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是_______ (保留1位小数)。
(2)煤的气化反应之一为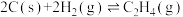

已知:①

②
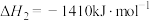
③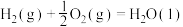

则上述煤的生成 的气化反应的
的气化反应的
_______ 。实际生产中该气化反应需要加入催化剂,其主要原因是_______ (填“速率问题”或“平衡问题”)。
(1)已知甲烷的燃烧热为
 ,
,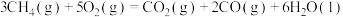
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式: 、
、 键的键能分别为
键的键能分别为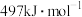 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是(2)煤的气化反应之一为
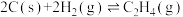

已知:①


②

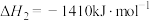
③
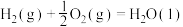

则上述煤的生成
 的气化反应的
的气化反应的
您最近一年使用:0次
2022-12-13更新
|
209次组卷
|
2卷引用:广西北海市2022-2023学年高二上学期期末考试化学试题
3 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为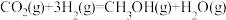 。该反应一般认为通过如下步骤来实现:
。该反应一般认为通过如下步骤来实现:
①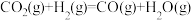
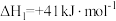
②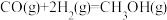
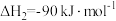
总反应的
___________  ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填字母),判断的理由是___________ 。
A.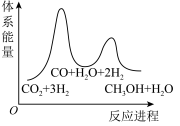 B.
B.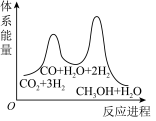 C.
C.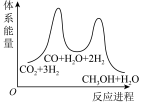 D.
D.
(2) 与
与 反应得到合成气的原理为
反应得到合成气的原理为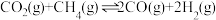 。某小组向体积是
。某小组向体积是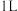 的恒容密闭容器中充入物质的量均为
的恒容密闭容器中充入物质的量均为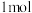 的
的 与
与 ,反应过程中
,反应过程中 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。

①压强:
___________  (填“>”或“<”)。
(填“>”或“<”)。
②1100℃、 条件下,
条件下,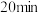 时反应达到平衡状态,则
时反应达到平衡状态,则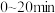 内
内 的反应速率
的反应速率
___________  ,反应的平衡常数
,反应的平衡常数
___________ (用含 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)二氧化碳加氢制甲醇的总反应可表示为
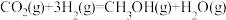 。该反应一般认为通过如下步骤来实现:
。该反应一般认为通过如下步骤来实现:①
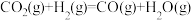
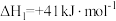
②
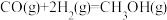
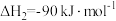
总反应的

 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是A.
 B.
B. C.
C. D.
D.
(2)
 与
与 反应得到合成气的原理为
反应得到合成气的原理为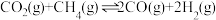 。某小组向体积是
。某小组向体积是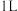 的恒容密闭容器中充入物质的量均为
的恒容密闭容器中充入物质的量均为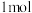 的
的 与
与 ,反应过程中
,反应过程中 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。
①压强:

 (填“>”或“<”)。
(填“>”或“<”)。②1100℃、
 条件下,
条件下,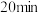 时反应达到平衡状态,则
时反应达到平衡状态,则 内
内 的反应速率
的反应速率
 ,反应的平衡常数
,反应的平衡常数
 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
解题方法
4 . H2S广泛存在于许多燃气和工业废气中,脱除其中的H2S既可回收硫又可防止产生污染。回答下列问题:
(1)Tretford氧化法脱H2S,包括H2S的吸收、氧化析硫、焦钒酸钠的氧化等。
①焦钒酸钠的化学式为Na2V4O9,其中钒元素的化合价为_______ ;
②已知H2S、H2CO3的电离常数如下表所示:
纯碱溶液吸收H2S的离子方程式为______________ 。
(2)Claus氧化回收硫的反应原理为:2H2S(g)+O2(g)=2S(g)+2H2O(g) △H1
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H2=-1124 kJ/mol
2H2S(g) +SO2(g)=S(g) +2H2O(g) △H3=- 233 kJ/mol
则△H1=_______ kJ/mol。
(3)H2S分解反应2H2S(g) 2H2(g)+S2(g)在无催化剂及Al2O3催化下,H2S在反应器中不同温度时反应,每间隔相同时间测定一次H2S的转化率,其转化率与温度的关系如图所示:
2H2(g)+S2(g)在无催化剂及Al2O3催化下,H2S在反应器中不同温度时反应,每间隔相同时间测定一次H2S的转化率,其转化率与温度的关系如图所示:

①该反应的△H_______ (填“>”或“<”)0。
②在不加催化剂时,温度越高H2S的转化率越接近平衡时的转化率,原因是___________ ;在约1100 °C时,有无Al2O3催化,其转化率几乎相等,是因为___________ 。
③若起始时在恒容密闭容器中只充入H2S,在A点达到平衡时,若此时气体总压强为p,则此温度反应的平衡常数Kp=______ (Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数,列出含p的代数式)。
(1)Tretford氧化法脱H2S,包括H2S的吸收、氧化析硫、焦钒酸钠的氧化等。
①焦钒酸钠的化学式为Na2V4O9,其中钒元素的化合价为
②已知H2S、H2CO3的电离常数如下表所示:
| Ka1 | Ka2 | |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.3×10-7 | 5.61×10-11 |
纯碱溶液吸收H2S的离子方程式为
(2)Claus氧化回收硫的反应原理为:2H2S(g)+O2(g)=2S(g)+2H2O(g) △H1
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H2=-1124 kJ/mol
2H2S(g) +SO2(g)=S(g) +2H2O(g) △H3=- 233 kJ/mol
则△H1=
(3)H2S分解反应2H2S(g)
 2H2(g)+S2(g)在无催化剂及Al2O3催化下,H2S在反应器中不同温度时反应,每间隔相同时间测定一次H2S的转化率,其转化率与温度的关系如图所示:
2H2(g)+S2(g)在无催化剂及Al2O3催化下,H2S在反应器中不同温度时反应,每间隔相同时间测定一次H2S的转化率,其转化率与温度的关系如图所示:
①该反应的△H
②在不加催化剂时,温度越高H2S的转化率越接近平衡时的转化率,原因是
③若起始时在恒容密闭容器中只充入H2S,在A点达到平衡时,若此时气体总压强为p,则此温度反应的平衡常数Kp=
您最近一年使用:0次
名校
解题方法
5 . 二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
它可以分为两步,反应分别如下:
①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g),ΔH1=-205.1kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2=__ 。
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的是__ (填字母代号)。
a.降低温度 B.加入催化剂 c.缩小容器体积 D.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
问:①反应开始时正、逆反应速率的大小:v(正)__ (填“>”、“<”或“=”)v(逆)。
②平衡时n(CH3OCH3)=__ ,平衡时CO的转化率=__ 。
(1)利用水煤气合成二甲醚的总反应为:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1它可以分为两步,反应分别如下:
①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g),ΔH1=-205.1kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2=
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的是
a.降低温度 B.加入催化剂 c.缩小容器体积 D.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生反应:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率的大小:v(正)
②平衡时n(CH3OCH3)=
您最近一年使用:0次
2020-10-29更新
|
636次组卷
|
3卷引用:广西北海市北海中学2019-2020学年高二上学期期中考试化学试题
解题方法
6 . 钼(Mo)是一种难熔稀有金属,我国的钼储量居世界第二。钼及其合金在冶金,农业、电器、化工、环保等方面有着广泛的应用。
(1)Mo可被发烟硝酸氧化,产物MoOF4 和MoO2F2物质的量比为1:1,完成下列方程式:
____Mo+____HF+_____HNO3=_______MoO2F2+_______MoOF4+NO2↑+_____________,___________
(2) 已知:
①2Mo(s)+3O2(g)=2MoO3(s) ΔH1
②MoS2(s) +2O2(g)==Mo(s)+2SO2(g) ΔH2
③2MoS2(s)+7O2(g)==2MoO3(s)+4SO2(g) ΔH3
则ΔH3=_______ (用含ΔH1、ΔH2的代数式表示),在反应③中若有0.2molMoS2参加反应,则转移电子_____ mol。
(3)密闭容器中用Na2CO3(s)作固硫剂,同时用一定量的氢气还原钼矿(MoS2) 原理是:MoS2(s)+4H2(g)+2Na2CO3(s)==Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH
实验测得平衡时的有关变化曲线如图所示
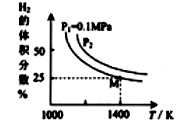
①由图可知,该反应的ΔH____ 0 (填“>”或“<”)。
②如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是_____ (选填编号)。
A.V正(H2)=V逆(H2O)
B 再加入MoS2,则H2转化率增大
C.容器内气体的密度不变时,一定达平衡状态
D.容器内压强不变时,一定达平衡状态
③由图可知M点时氢气的平衡转化率为_____ (计算结果保留0.1%) 。
④平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。求图中M点的平衡常数KP=_____ (MPa)2
(1)Mo可被发烟硝酸氧化,产物MoOF4 和MoO2F2物质的量比为1:1,完成下列方程式:
____Mo+____HF+_____HNO3=_______MoO2F2+_______MoOF4+NO2↑+_____________,
(2) 已知:
①2Mo(s)+3O2(g)=2MoO3(s) ΔH1
②MoS2(s) +2O2(g)==Mo(s)+2SO2(g) ΔH2
③2MoS2(s)+7O2(g)==2MoO3(s)+4SO2(g) ΔH3
则ΔH3=
(3)密闭容器中用Na2CO3(s)作固硫剂,同时用一定量的氢气还原钼矿(MoS2) 原理是:MoS2(s)+4H2(g)+2Na2CO3(s)==Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH
实验测得平衡时的有关变化曲线如图所示

①由图可知,该反应的ΔH
②如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是
A.V正(H2)=V逆(H2O)
B 再加入MoS2,则H2转化率增大
C.容器内气体的密度不变时,一定达平衡状态
D.容器内压强不变时,一定达平衡状态
③由图可知M点时氢气的平衡转化率为
④平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。求图中M点的平衡常数KP=
您最近一年使用:0次



