(1)已知:
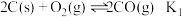

 (其中
(其中 、
、 、
、 为对应化学反应的平衡常数)
为对应化学反应的平衡常数)①则
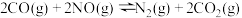 的平衡常数为K,则
的平衡常数为K,则
 、
、 、
、 表示)。
表示)。②在一个恒温恒容的密闭容器中发生反应
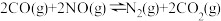 。能表明反应已达到平衡状态的标志有
。能表明反应已达到平衡状态的标志有A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量保持不变
E.
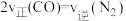 F.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应 ,
, 和
和 的物质的量变化如表所示。
的物质的量变化如表所示。| 条件 | 保持温度为 | ||||||
时间/ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
物质的量/ | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
物质的量/ | 0 | 0.30 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
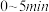 内,以
内,以 表示的平均反应速率
表示的平均反应速率
 的浓度
的浓度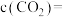
 的转化率
的转化率

 下的平衡常数
下的平衡常数
相似题推荐
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。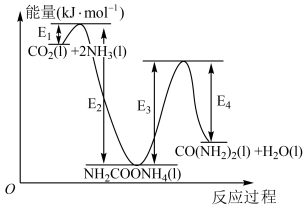
①反应物液氨
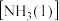 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。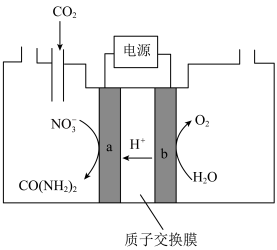
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到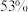 的法拉第效率
的法拉第效率 。已知:
。已知: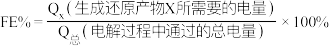 ,其中,
,其中,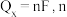 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下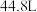 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有(1)已知:①NO2 + CO
 CO2 + NO 该反应的平衡常数为K1(下同)每1mol下列物质分解为气态基态原子消耗能量分别为
CO2 + NO 该反应的平衡常数为K1(下同)每1mol下列物质分解为气态基态原子消耗能量分别为 NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g)
 2NO(g) ΔH=+179.5 kJ/mol K2
2NO(g) ΔH=+179.5 kJ/mol K2 ③2NO(g) +O2(g)
 2NO2(g) ΔH=-112.3 kJ/mol K3
2NO2(g) ΔH=-112.3 kJ/mol K3试写出NO与CO反应生成无污染物气体的热化学方程式
(2)污染性气体NO2与CO在一定条件下的反应为:2NO2+4CO
 4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的 ,则反应开始到平衡时CO的平均反应速率v(CO)=
,则反应开始到平衡时CO的平均反应速率v(CO)=若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围
(3)电化学降解NO2-的原理如下图:
①电源的负极是
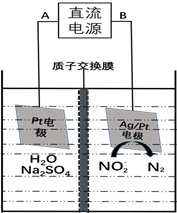
②若电解过程中转移了6mol电子,则膜两侧电解液的质量变化差
 为
为(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1mol
 (g),发生下列反应生成水煤气
(g),发生下列反应生成水煤气I.
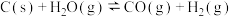
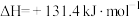
II.

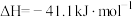
①反应I在该温度下能够自发进行的原因为
②
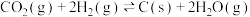

③下列说法正确的是
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应I的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时
 的体积分数可能大于
的体积分数可能大于
④反应平衡时,
 (g)的转化率为50%,CO的物质的量为0.1mol,此时反应II的平衡常数
(g)的转化率为50%,CO的物质的量为0.1mol,此时反应II的平衡常数
(2)一种脱除和利用水煤气中
 方法的示意图如下:
方法的示意图如下:
①某温度下,吸收塔中
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的pH=
,则该溶液的pH= 的
的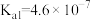 ,
,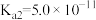 )。
)。②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理,将
 电催化还原为
电催化还原为 ,阴极上除发生AgCl转化为Ag的反应外,另一个反应式为
,阴极上除发生AgCl转化为Ag的反应外,另一个反应式为(1)某些常见化学键的键能(将
 气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成
气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成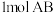 气体所放出的能量)数据如下表:
气体所放出的能量)数据如下表:| 化学键 | C—H | C=O | O—H | O=O |
键能 | 414 | 803 | 463 | 498 |
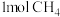 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为(2)一定条件下,通过
 加氢可以制备
加氢可以制备 ,反应方程式为
,反应方程式为 。在一定温度下,将
。在一定温度下,将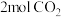 和
和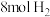 放入
放入 恒容密闭容器中,测得反应过程中
恒容密闭容器中,测得反应过程中 的浓度随时间的变化如表所示:
的浓度随时间的变化如表所示: | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
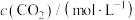 | 1 | 0.5 | 0.3 | 0.25 | 0.2 | 0.2 | 0.2 |
 内,
内,
 ,
,
 。
。②平衡时,
 的转化率为
的转化率为③T℃下,若达到平衡时的压强为
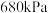 ,则T℃下该反应的压强平衡常数
,则T℃下该反应的压强平衡常数
 (
( 为用分压表示的平衡常数,分压=总压×物质的量分数)。
为用分压表示的平衡常数,分压=总压×物质的量分数)。④下列条件能判断该反应达到化学平衡状态的是
a.
 b.容器内气体的密度保持不变
b.容器内气体的密度保持不变c.容器中气体的平均摩尔质量不变 d.
 与
与 的浓度相等
的浓度相等

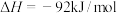 。
。(1)已知下列数据:
| 化学键 | H-H |  |
| 键能(kJ/mol) | 436 | 946 |
则N-H键的键能是
(2)T℃时,在2L的密闭容器中发生上述合成氨反应,开始投入
 和一定量的
和一定量的 ,体系中
,体系中 随时间的变化如下表:
随时间的变化如下表:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
 的物质的量(mol) 的物质的量(mol) | 0.40 | 0.20 | 0.14 | 0.12 | 0.12 | 0.12 |
①用
 表示从0~2min内该反应的平均速率
表示从0~2min内该反应的平均速率
②第4min时
 的体积分数为
的体积分数为③下列叙述中能说明上述反应达到平衡状态的是
a.该条件下生成
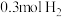 同时生成
同时生成
b.该条件下气体的平均相对分子质量保持不变
c.该条件下混合气体的密度保持不变
d.
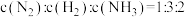
Ⅱ.如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,若两电极分别为Zn和石墨棒,则:

(3)X为
(4)Y上发生的电极反应为
(5)
 移向
移向(2)若25℃,101 kPa下,1 g CH4完全燃烧生成液态水和CO2气体,放出55.6 kJ的热量,则甲烷的燃烧热为
(3)对于下列反应:2SO2(g)+ O2(g)⇌2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
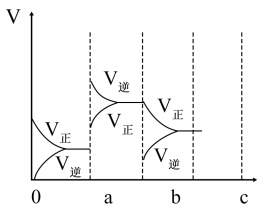
(4)下图表示在密闭容器中反应:2SO2(g)+O2(g)⇌2SO3(g) △H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是
【推荐1】CO、CO2、CH4等含碳化合物的综合利用是当今科技的重点研究对象之一。
(1)双功能催化剂的催化作用,突破了低温下水煤气转换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]时高转化率与高反应速率不能兼得的难题。反应过程示意图如下:

下列说法正确的是
A.过程I、过程II、过程皿均为吸热反应
B.图示的三个过程都与H2O有关
C.图示的三个过程中均有极性共价键的断裂和生成
D.使用催化剂降低了整个水煤气变换反应过程的ΔH
(2)已知:
①2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH=+180kJ·mol-1
表示CO燃烧热的热化学方程式为
(3)某催化剂的M型、N型均可催化反应2CO(g)+O2(g)=2CO2(g),向容积相同的恒容密闭容器中分别充入等物质的量的CO和O2,在相同时间段内,不同温度下测得CO的转化率(α)如图所示。

①图中a、b、c、d、e五个点对应状态下,反应速率最慢的是
②N型催化剂条件下,从a点到e点,CO的转化率先增大,后减小,e点时突然减小的原因为
③若b点容器中c(O2)=0.4mol·L-1,则T℃时该反应的平衡常数K=
(4)在一定条件下,CH4(g)+CO2(g)=2H2(g)+2CO(g),可制得合成气H2和CO。在2L密闭容器中充入CO2和CH4,使其物质的量浓度均为0.5mol·L-1,达到平衡时CO的体积分数为X,若恒温恒容下,向平衡体系中再充入1mol CO2和1mol CH4。回答下列问题:
①化学平衡
②再次平衡时,CO的体积分数

(1)图中条件选定的主要原因是
A.温度、压强对化学平衡的影响
B.催化剂铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(2)工业生产中氮气与氢气按物质的量之比为1∶2.8进行投料,合成塔压强p恒定。若起始时氮气通入量为x mol,一段时间后测得氮气的平衡转化率为80%,用平衡分压代替平衡浓度表示平衡常数的

(3)合成氨反应通常控制在20~50MPa的压强和500℃左右的温度,若进入合成塔的氮气和氢气的体积比为1∶3,经科学测定,在相应条件下氮气和氢气反应所得氨的平衡浓度(体积分数)如表所示:
| 压强 | 20MPa | 60MPa |
| 500℃ | 19.1 | 42.2 |
A.表中所测数据有明显误差 B.生产条件控制不当
C.氨的分解速率大于预测值 D.合成塔中的反应并未达到平衡
该流程控制含氨约为15%的原因是
(4)据统计,每年全世界在合成氨工业中向外排放
 高达40亿吨,为循环使用
高达40亿吨,为循环使用 减少浪费,常见的方法是利用合成氨的产品
减少浪费,常见的方法是利用合成氨的产品 和副产品
和副产品 合成尿素:
合成尿素:①
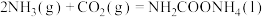
 kJ/mol
kJ/mol 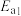
②
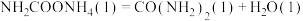
 kJ/mol
kJ/mol 
副反应:

已知活化能大小:
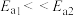 ,某科研小组模拟工业合成尿素生产,发现反应温度在140℃时生成尿素的反应速率反而比80℃小,可能原因是
,某科研小组模拟工业合成尿素生产,发现反应温度在140℃时生成尿素的反应速率反而比80℃小,可能原因是(5)工业合成尿素中,通常氨气、二氧化碳投料比大于2,请分析可能原因___________。
| A.氨易获得,成本较低 |
| B.氨过剩可提高二氧化碳的转化率,加快合成速率 |
| C.氨气可与体系内水结合,减少氨基甲酸铵水解,抑制副反应发生 |
| D.氨结合水,促进(4)中反应②正向移动 |
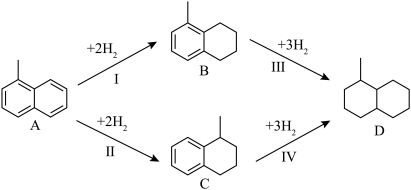
(1)以上四个反应的平衡常数随温度变化的关系如图所示:
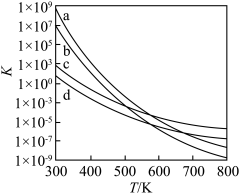
 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则
,则
 的数值范围是
的数值范围是A.<-1 B.-1~0 C.0~1 D.>1
(2)650K,以
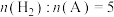 充料,反应达平衡时物质A、B、C、D的物质的量分数
充料,反应达平衡时物质A、B、C、D的物质的量分数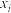 [例如:
[例如: ]随体系压强的变化关系如图所示:
]随体系压强的变化关系如图所示: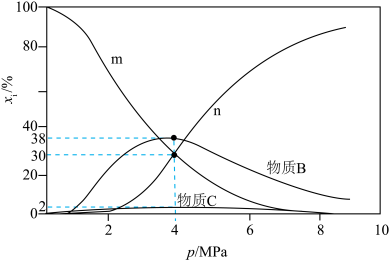
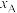 和
和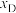 随压强p变化的曲线分别是
随压强p变化的曲线分别是②其他条件不变,若增大
 的比例,则
的比例,则 的值将
的值将③当压强
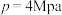 时,
时, 的平衡转化率
的平衡转化率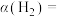
 压强平衡常数
压强平衡常数
 (列出计算式即可)。
(列出计算式即可)。
(1)
 可以与
可以与 发生反应:
发生反应: 。有研究表明该反应分为两步,中间产物是不稳定易分解的
。有研究表明该反应分为两步,中间产物是不稳定易分解的 。请写出第二步反应的化学方程式
。请写出第二步反应的化学方程式(2)
 与
与 之间存在反应
之间存在反应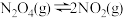 。将一定量的
。将一定量的 放入恒容密闭容器中,测得其平衡转化率[
放入恒容密闭容器中,测得其平衡转化率[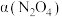 ]随温度的变化如图所示。
]随温度的变化如图所示。
①由图推测该反应的

②a点对应的温度下,已知
 的起始压强为
的起始压强为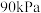 ,平衡后总压强为
,平衡后总压强为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(3)化工废水中常常含有以二甲胺(
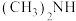 )为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。反应原理是:①
)为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。反应原理是:① 在阳极转化为
在阳极转化为 ;②
;② 在碱性溶液中歧化为
在碱性溶液中歧化为 ;③
;③ 将二甲胺氧化为
将二甲胺氧化为 ,
, 和
和 。
。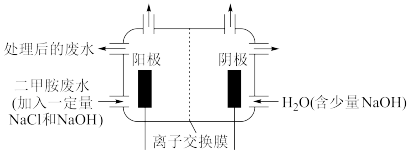
①写出电解池中阴极发生反应的方程式
②电解池中选择阴离子交换膜而不选择阳离子交换膜的原因是
③当阴极区收集到6.72L (标况下)
 时,阳极区收集到
时,阳极区收集到 的体积(标况下)是
的体积(标况下)是(1)乙烷在一定条件下可发生如下反应:C2H6(g)=C2H4(g)+H2(g) △H,相关物质的燃烧热数据如表所示:
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热△H/(kJ•mol-1) | -1560 | -1411 | -286 |
①△H=
②提高该反应平衡转化率的方法有
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=
(2)高温下,甲烷生成乙烷的反应如下:2CH4
 C2H6+H2。反应在初期阶段的速率方程为:r=k×c(CH4),其中k为反应速率常数。设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2。反应在初期阶段的速率方程为:r=k×c(CH4),其中k为反应速率常数。设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=(3)如图所示装置
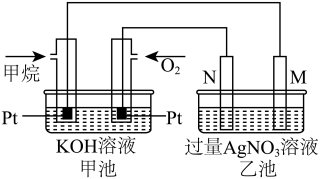
①负极的电极反应式
②乙装置电镀银,
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中发生下述反应:2SO2(g)+O2(g)
 2SO3(g)。在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。
2SO3(g)。在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。①从平衡角度分析,采用过量O2的目的是
②对于气相反应,用某组分(B)的平衡分压(PB)代替其物质的量浓度(cB)也可以表示平衡常数(记作KP),已知:B的平衡分压=总压×平衡时B的物质的量分数,则该温度下Kp=
③已知:K(300℃)>K(350℃),该反应是
(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图1。平衡状态由A变到B时,平衡常数K(A)

(3)如图2所示,保持温度不变,将2molSO2和1molO2加入甲容器中,将4molSO3加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲
②若保持乙中压强不变,向甲、乙容器中通入等质量的氦气,达到新平衡时,SO3的体积分数甲



