1 . 已知: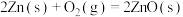
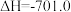 kJ·mol-1
kJ·mol-1

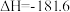 kJ·mol-1
kJ·mol-1
则反应 的
的 为
为
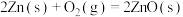
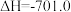 kJ·mol-1
kJ·mol-1
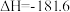 kJ·mol-1
kJ·mol-1则反应
 的
的 为
为| A.+519.4kJ⋅mol-1 | B.-259.7kJ⋅mol-1 | C.+259.7kJ⋅mol-1 | D.-519.4kJ⋅mol-1 |
您最近一年使用:0次
2024-02-07更新
|
348次组卷
|
90卷引用:黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第四次月考化学试题
黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第四次月考化学试题(已下线)2011-2012学年黑龙江省牡丹江一中高二上学期期末考试化学试卷2014-2015学年黑龙江省伊春市伊春二中高二上学期期中化学试卷黑龙江省大庆市第十中学2016-2017学年高一下学期期末考试化学试题黑龙江省哈尔滨市第三中学2017-2018届高二上学期模块考试(期末)化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2017-2018学年高一下学期期末考试(理)化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高二上学期期末考试化学试题河北省张家口市宣化一中2020-2021学年高二上学期期末考试化学试题四川省广安第二中学校2021-2022学年高二上学期第一次月考化学试题海南省鑫源中学2021-2022学年高二上学期期中考试化学试题海南省临高县新盈中学2021-2022学年高二上学期(1-4班)期中考试化学试题(已下线)2012届山东省济宁一中高三上学期第二次定时练习化学试卷(已下线)2011-2012学年浙江省杭州十四中高二上学期期末化学试卷(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷(已下线)2012届陕西省兴平市秦岭中学高三上学期期末练习化学试卷(已下线)2011-2012学年浙江省嘉兴一中高一下学期期中考试化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷(已下线)2012-2013学年江苏省如皋中学高二10月阶段练习化学试卷(已下线)2012-2013学年陕西省三原县北城中学高二第四次月考化学试卷(已下线)2012-2013学年江苏泰州二中高二上学期期中考试化学(选修)试卷(已下线)2013届广东省佛山一中高三第二次段考化学试卷(已下线)2013-2014学年天津市红桥区高二上学期期末考试化学试卷(已下线)2014陕西省西安中学高三上学期第三次质量检测化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2015届吉林省汪清县第六中学高三第三次月考化学试卷(已下线)2014秋安徽省宿州市高二上学期期中化学(理)试卷2014-2015学年内蒙古巴市一中高二10月月考化学试卷2014-2015学年云南省景洪市第四中学高二下学期期中考试化学试卷2015-2016学年山西太原五中高二上第一周考理科化学试卷2015-2016学年福建省宁德市霞浦七中高二上期中(理)化学试卷2016届福建省三明一中高三上学期第二次月考化学试卷2015-2016学年四川省南充市老林中学高二上学期9月月考化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷2015-2016学年河北省沧州一中高一下期末化学试卷2015-2016学年福建省福州市文博中学高二上期中化学试卷2017届山东省枣庄三中高三上学期9月质检化学试卷2016-2017学年贵州省湄潭县湄江中学高二上第一次月考化学试卷2016-2017学年河南省南阳市宛东五校高二上第一次联考化学试卷2017届河北邯郸市大名一中高三上学期第二次月考化学试卷2016-2017学年安徽省合肥一中高二上月考一化学试卷2017届福建省柘荣一中、宁德中学高三上联考一化学卷宁夏育才中学2017-2018学年高二9月月考化学试题山东省垦利第一中学2017-2018学年高二上学期第一次月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题湖北省武汉市武昌区2017_2018学年高二化学上学期期中化学试题安徽省滁州市(九校)2017-2018学年高二上学期期末考试化学试题人教版高二化学选修四专题:化学反应热的计算同步练习卷【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题福建省莆田市第八中学2018-2019学年高二(理)上学期期中考试化学试题北京四中2018-2019学年高一下学期期末考试化学试题海南省海口市第四中学2020届高三上学期摸底考试化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题河南省周口中英文学校2019-2020学年高二上学期第一次月考化学试题河南省郑州市106中学2019-2020学年高二9月月考化学(理)试题甘肃省永昌四中2019-2020学年高二上学期期中考试化学试题云南省曲靖市会泽县茚旺高级中学2020届高三上学期11月月考化学试题步步为赢 高二化学寒假作业:作业一 化学反应中的能量变化安徽省涡阳县第一中学2019-2020学年高二12月月考化学试题西藏自治区日喀则市南木林高级中学2019-2020学年高二上学期期中化学试题河南省周口市扶沟县包屯高中2019---2020学年高二上期期末考试化学试题甘肃省张掖市高台县第一中学2018-2019学年高二上学期期末考试理科化学试题辽宁省凌源市第三中学2019-2020学年高二下学期第一次月考化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二下期第二次月考化学试题(已下线)1.3.2 反应热的计算(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)山东省滕州市第一中学2020-2021学年高二9月开学收心考试化学试题四川省成都市蓉城高中教育联盟2019-2020学年高二上学期期中联考化学试题福建省漳州市平和县第一中学2021届高三上学期期中考试化学试题吉林油田第十一中学2020-2021学年高二上学期期中考试化学试题四川省达州市宣汉县第二中学2020-2021学年高二上学期期中考试理综化学试题广东省江门市第二中学2020-2021学年高二上学期第二次考试(期中)化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期中考试化学试题2011年普通高等学校招生全国统一考试化学(海南卷)广东省揭阳市揭西县河婆中学2020-2021学年高二上学期第一次月考化学试题四川省峨眉第二中学校2021-2022学年高二下学期5月月考化学试题北京市顺义区第一中学2022-2023学年高二上学期10月月考化学试题辽宁省阜新市第二高级中学2022-2023学年高二上学期9月月考化学试题新疆喀什第二中学2022-2023学年高二上学期期中考试化学试题青海省西宁市海湖中学2022-2023学年高二上学期期末考试化学试题第3课时 反应焓变的计算第一章 第二节 反应热的计算北京市和平街第一中学2023-2024学年高二上学期10月阶段性练习化学试题北京市首都师范大学附属中学2023-2024学年高二上学期9月检测化学试题四川省眉山市仁寿第一中学校(北校区)2023-2024学年高二上学期11月期中化学试题宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】云南省宣威市第三中学2023-2024学年高二上学期第四次月考化学试题广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题四川省泸州市泸县第四中学2023-2024学年高二下学期开学化学试题山东省菏泽市外国语学校2023-2024学年高二上学期化学10月份月考试题
名校
解题方法
2 . 在298K、101kPa时,已知:



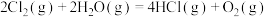

则 与
与 和
和 间的关系正确的是
间的关系正确的是




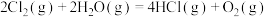

则
 与
与 和
和 间的关系正确的是
间的关系正确的是A.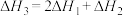 | B. |
C.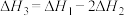 | D.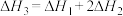 |
您最近一年使用:0次
2023-12-11更新
|
270次组卷
|
11卷引用:黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题
黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省普宁市第二中学2021-2022学年高二上学期期中考试化学试题宁夏吴忠市盐池高级中学2019-2020学年高二上学期期末检测化学试题陕西省延安市富县高级中学2021-2022学年高一下学期期中考试化学试题天津市第二南开学校2022-2023学年度高二上学期期中质量调查化学试题广东省江门市鹤山市第一中学2022-2023学年高二上学期第二阶段考试化学试题贵州省黔西南布依族苗族自治州2022-2023学年高二上学期期末考试化学试题北京市第五十中学2023-2024学年高二上学期期中考试化学试题广东省广州市第三中学、第四中学、培正中学2023-2024学年高二上学期期中考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第二次月考化学试题福建省龙岩市永定区城关中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
3 . 已知反应:①
 ,
,
②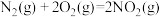
 ,
,
③
 ,
,
则反应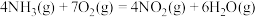 的
的 为
为

 ,
,②
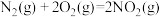
 ,
,③

 ,
,则反应
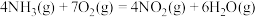 的
的 为
为A.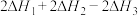 | B. |
C.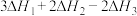 | D.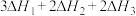 |
您最近一年使用:0次
2023-01-20更新
|
582次组卷
|
54卷引用:黑龙江省大庆中学2021-2022学年高二上学期开学考试化学试题
黑龙江省大庆中学2021-2022学年高二上学期开学考试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题(已下线)2014届黑龙江省哈六中高三上学期期中考试化学试卷【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期10月月考化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期期中考试化学试题天津市南开中学2021-2022学年高二上学期期中检测化学试题江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题吉林省延边朝鲜族自治州汪清县汪清第四中学2021-2022学年高二上学期第二次阶段考试化学试题湖南省涟源市第二中学2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2022-2023学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第七十三中学校2022-2023学年高二上学期第一次月考化学试题甘肃省靖远县第二中学2021-2022学年高二上学期期中考试化学(理)试题(已下线)2011-2012学年北京市101中学高二下学期期中考试化学试卷2015-2016学年山东省济宁任城区高二上学期统考化学试卷2017届河北省武邑中学高三上学期第一次调研化学试卷辽宁省庄河市高级中学2016-2017学年高一下学期期中考试化学试题【全国校级联考】安徽省淮北十二中、濉溪二中2017-2018学年高一下学期期中联考化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期期末考试化学试题吉林省长春市田家炳实验中学2018-2019学年高二上学期第一学程检测化学试题【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期10月月考化学试题【全国百强校】江西省金溪县第一中学2018-2019学年高二上学期12月月考化学试题吉林省乾安县第七中学2018-2019学年高一下学期第二次质量检测化学试题宁夏长庆高级中学2019-2020学年高二上学期第一次月考化学试题福建省永泰县第一中学2019-2020学年高二上学期期中考试化学试题安徽省砀山县第二中学2020届高三上学期第四次月考化学试题云南省迪庆州香格里拉中学2019-2020学年高二上学期期末考试化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期12月月考化学试题【懂做原理题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择提升24题】2020届高三化学知识点强化训练—盖斯定律(已下线)1.1.3 反应焓变的计算 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1河南省鹤壁市高中2019-2020学年高一下学期第一次段考化学试题安徽省合肥市第九中学2020-2021学年高二上学期第一次月考化学试题(已下线)【南昌新东方】9.湾里一中 梁莎(已下线)【浙江新东方】48鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时4 反应焓变的计算人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 课时1 盖斯定律安徽省六安市舒城育才学校2020-2021学年高二12月月考化学试题云南省楚雄师范学院附属中学2020-2021学年高二上学期期中考试化学试题(已下线)1.2.2 化学反应焓变的计算-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)辽宁省辽河油田第二高级中学2022-2023学年高二上学期开学考试化学试题陕西省宝鸡市千阳县中学2022-2023学年高二上学期第一次月考(理)化学试题广东省深圳实验学校高中部2022-2023学年高二上学期第一阶段考试化学试题海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(期末考)化学试题吉林省洮南市第一中学2022-2023学年高二上学期第一次(10月)月考化学试题安徽省怀宁县第二中学2021-2022学年高三上学期期末考试化学试题湖北省2022-2023学年高三上学期期末考试化学试题吉林省长春市九台区营城第一高级中学2022-2023学年高二上学期第一次月考化学试题辽宁省沈阳市郊校2022-2023学年高一下学期4月联考化学试题河北省邢台市2022-2023学年高一下学期6月月考化学试题(已下线)专题02 盖斯定律、反应热的计算【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)江西省抚州市2023-2024学年高二上学期学生学业质量监测化学试题青海省西宁北外附属新华联外国语高级中学2023-2024学年高二上学期期中考试化学试题江西省南昌十九中2022-2023学年高二上学期期末考试化学试卷 湖南省长沙市德成学校2023-2024学年高二上学期1月期末化学试题
解题方法
4 . 碳、氮是中学化学重要的非金属元素,在生产、生活中有广泛的应用。
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管道上安装一个催化转化装置,使NO与CO反应,产物都是空气中的主要成分。写出该反应的热化学方程式_______ 。
已知:①N2(g)+O2(g)=2NO(g) ∆H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g) ∆H=-112.3kJ/mol
③NO2(g)+CO(g)=NO(g)+CO2(g) ∆H=-234kJ/mol
(2)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l) C6H12O6(s)+6O2(g) ∆H=+669.62 kJ/mol;该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是_______。
C6H12O6(s)+6O2(g) ∆H=+669.62 kJ/mol;该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是_______。
(3)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。

①在转化过程中起催化作用的物质是_______ ;
②写出总反应的化学方程式_______ 。
(4)工业上以NH3和CO2为原料合成尿素[CO(NH2)2),反应的化学方程式如下:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l);根据上述反应,填写下列空白
①已知该反应可以自发进行,则∆H_______ 0。(填“>”、“<”或“=”);
②一定温度和压强下,若原料气中的NH3和CO2的物质的量之比 =x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
=x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是_______ ;B点处,NH3的平衡转化率为_______ 。

③一定温度下,在3L定容密闭容器中充入NH3和CO2,若x=2,当反应后气体压强变为起始时气体压强的 时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=_______ 。
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管道上安装一个催化转化装置,使NO与CO反应,产物都是空气中的主要成分。写出该反应的热化学方程式
已知:①N2(g)+O2(g)=2NO(g) ∆H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g) ∆H=-112.3kJ/mol
③NO2(g)+CO(g)=NO(g)+CO2(g) ∆H=-234kJ/mol
(2)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l)
 C6H12O6(s)+6O2(g) ∆H=+669.62 kJ/mol;该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是_______。
C6H12O6(s)+6O2(g) ∆H=+669.62 kJ/mol;该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是_______。| A.增大CO2的浓度 | B.取走一半C6H12O6 | C.加入催化剂 | D.适当升高温度 |

①在转化过程中起催化作用的物质是
②写出总反应的化学方程式
(4)工业上以NH3和CO2为原料合成尿素[CO(NH2)2),反应的化学方程式如下:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l);根据上述反应,填写下列空白
①已知该反应可以自发进行,则∆H
②一定温度和压强下,若原料气中的NH3和CO2的物质的量之比
 =x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
=x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
③一定温度下,在3L定容密闭容器中充入NH3和CO2,若x=2,当反应后气体压强变为起始时气体压强的
 时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
您最近一年使用:0次
5 . 控制CO2的排放是防止温室效应等不良气候现象产生的有效途径。
(1)高炉炼铁中用CO还原Fe2O3得到Fe,同时会排放大量的CO2和烟尘,必须进行严格的控制。已知:①C(石墨,s)+CO2(g)=2CO(g) ΔH=+172.5kJ⋅mol-1;②3C(石墨,s)+Fe2O3(s)=2Fe(s)+3CO(g) ΔH=+489.0kJ⋅mol-1,则CO还原Fe2O3的热化学方程式为___________ 。
(2)在恒温恒容密闭容器中充入一定量CO与Fe2O3发生该反应。
①以下能说明该可逆反应达到平衡状态的是___________ (选填字母)。
A.混合气体的密度不变 B.容器内气体压强一定
C.CO与CO2浓度比为1:1 D.Fe2O3与Fe的质量比不变
②当达到平衡后,再充入一定量CO,平衡___________ (填“正向”、“逆向”或“不”)移动,则达到新平衡后CO的转化率___________ (填“增大”、“减小”或“不变”)。
③下列措施中能使平衡时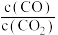 增大的是
增大的是___________ (填字母)。
A.升高温度 B.增大压强 C.充入一定量的CO2 D.再加入一定量铁粉
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g) 2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
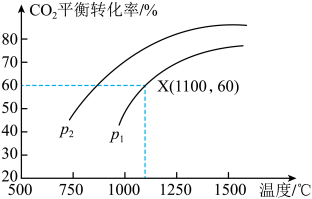
①压强:p1___________ p2(填“>”或“<”)。
②1100℃、p1条件下,20min时反应达到平衡状态,则0-20min内CO的反应速率V(CO)=___________ ,反应的平衡常数Kp=___________ (用含p1的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数);
(1)高炉炼铁中用CO还原Fe2O3得到Fe,同时会排放大量的CO2和烟尘,必须进行严格的控制。已知:①C(石墨,s)+CO2(g)=2CO(g) ΔH=+172.5kJ⋅mol-1;②3C(石墨,s)+Fe2O3(s)=2Fe(s)+3CO(g) ΔH=+489.0kJ⋅mol-1,则CO还原Fe2O3的热化学方程式为
(2)在恒温恒容密闭容器中充入一定量CO与Fe2O3发生该反应。
①以下能说明该可逆反应达到平衡状态的是
A.混合气体的密度不变 B.容器内气体压强一定
C.CO与CO2浓度比为1:1 D.Fe2O3与Fe的质量比不变
②当达到平衡后,再充入一定量CO,平衡
③下列措施中能使平衡时
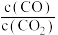 增大的是
增大的是A.升高温度 B.增大压强 C.充入一定量的CO2 D.再加入一定量铁粉
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g)
 2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
①压强:p1
②1100℃、p1条件下,20min时反应达到平衡状态,则0-20min内CO的反应速率V(CO)=
您最近一年使用:0次
解题方法
6 . 回答问题:
(1)已知C(s、金刚石)+O2(g)=CO2(g) △H=-395.4 kJ·mol-1,C(s、石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1。则石墨中C-C键键能____ (填“大于”“小于”或“等于”)金刚石中C-C键键能。
(2)已知下列反应的反应热:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为____ 。
(1)已知C(s、金刚石)+O2(g)=CO2(g) △H=-395.4 kJ·mol-1,C(s、石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1。则石墨中C-C键键能
(2)已知下列反应的反应热:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
您最近一年使用:0次
解题方法
7 . 请回答下列问题。
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH=_______ (请用含有ΔH1、ΔH2的式子表示)。
(2)若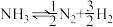 K=a,则N2+3H2
K=a,则N2+3H2 2NH3 K′=
2NH3 K′=_______ (用含a的式子表示)。
(3)在体积为3 L的恒容密闭容器中,进行合成氨N2+3H2 2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1_______ (填“>”“<”或“=”)T2。
②在T2下,经过10 min达到化学平衡状态,平衡时N2的转化率α(N2)=_______ 和K =_______ (分数表示)。
③下列图象分别代表焓变(ΔH)、混合气体平均相对分子质量(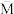 )、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是
)、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是_______ (填字母)。
A.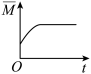 B.
B. 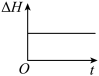 C.
C. 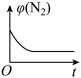 D.
D. 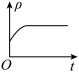
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH=
(2)若
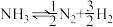 K=a,则N2+3H2
K=a,则N2+3H2 2NH3 K′=
2NH3 K′=(3)在体积为3 L的恒容密闭容器中,进行合成氨N2+3H2
 2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:| 温度/K | 平衡时NH3的物质的量/mol |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1
②在T2下,经过10 min达到化学平衡状态,平衡时N2的转化率α(N2)=
③下列图象分别代表焓变(ΔH)、混合气体平均相对分子质量(
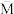 )、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是
)、N2的体积分数[φ(N2)]和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是A.
 B.
B.  C.
C.  D.
D. 
您最近一年使用:0次
名校
解题方法
8 . 不同的化学反应具有不同的反应热,人们可以通过多种方法获得反应热的数据,通常用实验进行测定,也可以进行理论推算。
Ⅰ.在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定盐酸与氢氧化钠溶液反应的反应热,则:
(1)测定中和热的装置如图1所示。
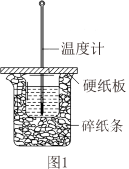
①从实验装置上看,图中尚缺少的一种仪器是____ 。
②做一次完整的中和热测定实验,温度计需使用____ 次。
③现用50mL0.5mol/L的稀盐酸与50mL0.55mol/L氢氧化钠溶液反应测定,以下操作可能会导致测得的中和热数值偏大的是____ 。
A.实验装置保温、隔热效果差
B.量取稀盐酸的体积时仰视读数
C.分多次把氢氧化钠溶液倒入盛有盐酸的小烧杯中
D.用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验
(2)在25mL1.00mol/LHCl溶液中逐滴加入未知浓度NaOH溶液VmL,将溶液搅拌均匀后,在保温隔热的条件下测量并记录混合溶液的温度,实验结果如图2所示。
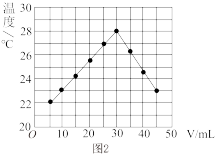
①做该实验时环境温度____ 22℃(填“<”、“>”或“=”)。
②NaOH溶液的物质的量浓度约为____ (保留小数点后两位)。
Ⅱ.并不是所有反应的反应热均可通过实验直接测定。
(3)已知:由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。部分化学键键能数据如表:
反应N2(g)+3H2(g) 2NH3(g)ΔH=akJ/mol,根据所列键能数据计算a=
2NH3(g)ΔH=akJ/mol,根据所列键能数据计算a=____ kJ/mol。
(4)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+akJ/mol
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g)ΔH=-bkJ/mol
O2(g)=CO2(g)+2H2(g)ΔH=-bkJ/mol
又知③H2O(g)=H2O(l)ΔH=-ckJ/mol
则甲醇蒸气燃烧的热化学方程式:____ (ΔH用a、b、c表示)。
Ⅰ.在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定盐酸与氢氧化钠溶液反应的反应热,则:
(1)测定中和热的装置如图1所示。
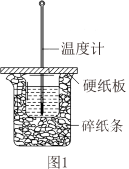
①从实验装置上看,图中尚缺少的一种仪器是
②做一次完整的中和热测定实验,温度计需使用
③现用50mL0.5mol/L的稀盐酸与50mL0.55mol/L氢氧化钠溶液反应测定,以下操作可能会导致测得的中和热数值偏大的是
A.实验装置保温、隔热效果差
B.量取稀盐酸的体积时仰视读数
C.分多次把氢氧化钠溶液倒入盛有盐酸的小烧杯中
D.用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验
(2)在25mL1.00mol/LHCl溶液中逐滴加入未知浓度NaOH溶液VmL,将溶液搅拌均匀后,在保温隔热的条件下测量并记录混合溶液的温度,实验结果如图2所示。

①做该实验时环境温度
②NaOH溶液的物质的量浓度约为
Ⅱ.并不是所有反应的反应热均可通过实验直接测定。
(3)已知:由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。部分化学键键能数据如表:
| 化学键 | H—H | N—H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
 2NH3(g)ΔH=akJ/mol,根据所列键能数据计算a=
2NH3(g)ΔH=akJ/mol,根据所列键能数据计算a=(4)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+akJ/mol
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g)ΔH=-bkJ/mol
O2(g)=CO2(g)+2H2(g)ΔH=-bkJ/mol又知③H2O(g)=H2O(l)ΔH=-ckJ/mol
则甲醇蒸气燃烧的热化学方程式:
您最近一年使用:0次
2022-03-16更新
|
200次组卷
|
3卷引用:黑龙江省八校2022届高三上学期期中联合考试化学试题
名校
解题方法
9 . “绿水青山就是金山银山”,研究消除氮氧化物污染对建设美丽家乡,打造宜居环境有重要意义。
(1)已知:2NO(g)+O2(g)=2NO2(g) △H1=-114kJ/mol
C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
N2(g)+O2(g)=2NO(g) △H3=+181kJ/mol
若某反应的平衡常数表达式为K= ,该反应的热化学方程式为
,该反应的热化学方程式为___________ 。
(2)T℃时,存在如下平衡:2NO2(g) N2O4(g)。该反应正、逆反应速率与NO2、N2O4的浓度关系为:v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆是速率常数),且lgv正~lgc(NO2)与lgv逆~lgc(N2O4)的关系如图所示。
N2O4(g)。该反应正、逆反应速率与NO2、N2O4的浓度关系为:v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆是速率常数),且lgv正~lgc(NO2)与lgv逆~lgc(N2O4)的关系如图所示。
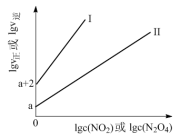
①图中表示lgv正~lgc(NO2)的线是___________ (填“I”或“II”)。
②T℃时,往刚性容器中充入一定量NO2,平衡后测得c(N2O4)为1.0mol/L,则平衡时,v逆=______ (用含a的表达式表示)。
③T℃时,该反应的平衡常数K=___________ L/mol。
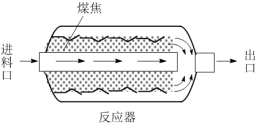
(3)原煤经热解、冷却得到的煤焦可用于NO的脱除。将浓度恒定的NO废气以固定流速通过下图的反应器。分别用两种不同热解温度的煤焦,测定NO的脱除率。
已知:i.两种不同热解温度500℃、900℃下获得的煤焦分别用S—500、S—900表示。
ii.煤焦表面存在的官能团有利于NO的吸附。热解温度高,煤焦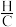 比值小,表面官能团少。
比值小,表面官能团少。
iii.NO的脱除主要含吸附和化学还原两个过程。
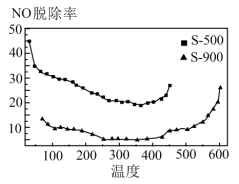
①由图可知:相同温度下,S—500对NO的脱除率比S—900的高,结合表格数据分析其可能原因是_______ 、______ 。
②由图可知:350℃后,随着温度升高,NO的脱除率增大的原因是___________ 。
(1)已知:2NO(g)+O2(g)=2NO2(g) △H1=-114kJ/mol
C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
N2(g)+O2(g)=2NO(g) △H3=+181kJ/mol
若某反应的平衡常数表达式为K=
 ,该反应的热化学方程式为
,该反应的热化学方程式为(2)T℃时,存在如下平衡:2NO2(g)
 N2O4(g)。该反应正、逆反应速率与NO2、N2O4的浓度关系为:v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆是速率常数),且lgv正~lgc(NO2)与lgv逆~lgc(N2O4)的关系如图所示。
N2O4(g)。该反应正、逆反应速率与NO2、N2O4的浓度关系为:v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆是速率常数),且lgv正~lgc(NO2)与lgv逆~lgc(N2O4)的关系如图所示。
①图中表示lgv正~lgc(NO2)的线是
②T℃时,往刚性容器中充入一定量NO2,平衡后测得c(N2O4)为1.0mol/L,则平衡时,v逆=
③T℃时,该反应的平衡常数K=
(3)原煤经热解、冷却得到的煤焦可用于NO的脱除。将浓度恒定的NO废气以固定流速通过下图的反应器。分别用两种不同热解温度的煤焦,测定NO的脱除率。

已知:i.两种不同热解温度500℃、900℃下获得的煤焦分别用S—500、S—900表示。
ii.煤焦表面存在的官能团有利于NO的吸附。热解温度高,煤焦
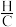 比值小,表面官能团少。
比值小,表面官能团少。iii.NO的脱除主要含吸附和化学还原两个过程。

①由图可知:相同温度下,S—500对NO的脱除率比S—900的高,结合表格数据分析其可能原因是
| 煤焦 | 元素分析(%) | 比表面积 (cm2∙g-1) | |
| H | C | ||
| S-500 | 2.76 | 80.79 | 105.69 |
| S-900 | 0.82 | 84.26 | 8.98 |
②由图可知:350℃后,随着温度升高,NO的脱除率增大的原因是
您最近一年使用:0次
2022-01-03更新
|
314次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学2021-2022学年高三上学期期末考试理科综合化学试题
解题方法
10 . CO、H2、C2H5OH三种物质燃烧的热化学方程式如下:
①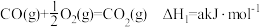
②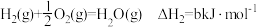
③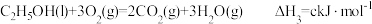 。下列说法正确的是
。下列说法正确的是
①
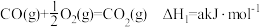
②
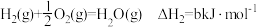
③
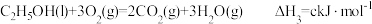 。下列说法正确的是
。下列说法正确的是| A.a>0 |
B.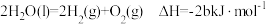 |
| C.由反应③可知乙醇的燃烧热为c kJ/mol |
D.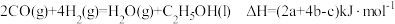 |
您最近一年使用:0次



