解题方法
1 . H2O2广泛应用于医疗卫生、化学合成等领域。
(1)已知2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:
i.H2O2(l)+I-(aq)= H2O(l)+IO-(aq) △H1 = +a kJ/moL(a > 0)
ii.H2O2(l)+_______。
则ii中反应机理用热化学方程式表示为_______ 。
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
Ⅰ.实验①和②的目的是_______ 。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下 较稳定,不易分解,为达到实验目的,你对原方案的改进是
较稳定,不易分解,为达到实验目的,你对原方案的改进是_______ 。
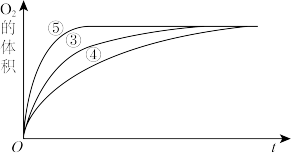
Ⅱ. 实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?
实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?_______ 。
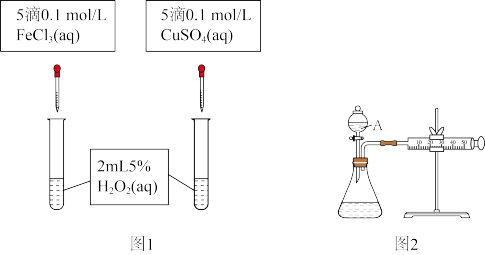
Ⅲ.为比较 和
和 对
对 分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
①写出 在
在 作用下发生反应的化学方程式:
作用下发生反应的化学方程式: _______ 
②利用图1实验,可通过观察产生气泡的快慢定性比较得出结论 有同学提出将
有同学提出将 改为
改为 更为合理,其理由是
更为合理,其理由是 _______ ,
③若利用图2实验可进行定理分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是_______ 。
④将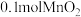 粉末加入50mL
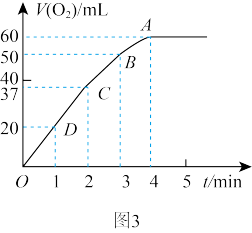
粉末加入50mL  溶液中,在标准状况下放出气体的体积和时间的关系如图3所示,解释反应速率变化的原因:
溶液中,在标准状况下放出气体的体积和时间的关系如图3所示,解释反应速率变化的原因: _______ , 初始物质的量浓度为
初始物质的量浓度为 _______ (保留两位有效数字)。
(1)已知2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:
i.H2O2(l)+I-(aq)= H2O(l)+IO-(aq) △H1 = +a kJ/moL(a > 0)
ii.H2O2(l)+_______。
则ii中反应机理用热化学方程式表示为
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① |  溶液 溶液 | 无 |
| ② | 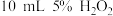 溶液 溶液 | 无 |
| ③ | 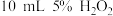 溶液 溶液 | 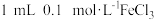 溶液 溶液 |
| ④ | 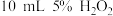 溶液 溶液 少量 HCl溶液 少量 HCl溶液 | 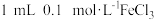 溶液 溶液 |
| ⑤ | 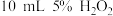 溶液 溶液 少量 NaOH溶液 少量 NaOH溶液 | 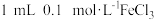 溶液 溶液 |
 较稳定,不易分解,为达到实验目的,你对原方案的改进是
较稳定,不易分解,为达到实验目的,你对原方案的改进是Ⅱ.
 实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?
实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?
Ⅲ.为比较
 和
和 对
对 分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
①写出
 在
在 作用下发生反应的化学方程式:
作用下发生反应的化学方程式: 
②利用图1实验,可通过观察产生气泡的快慢定性比较得出结论
 有同学提出将
有同学提出将 改为
改为 更为合理,其理由是
更为合理,其理由是 ③若利用图2实验可进行定理分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
④将
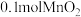 粉末加入50mL
粉末加入50mL  溶液中,在标准状况下放出气体的体积和时间的关系如图3所示,解释反应速率变化的原因:
溶液中,在标准状况下放出气体的体积和时间的关系如图3所示,解释反应速率变化的原因:  初始物质的量浓度为
初始物质的量浓度为 
您最近一年使用:0次
2 . 2NO(g) + O2(g) 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
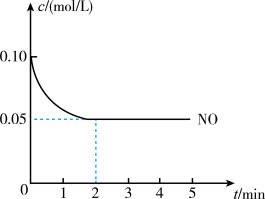
请回答:
(1)2 min内,v(O2) =_______ mol/(L·min)。
(2)800℃时,该反应的化学平衡常数数值为_______ 。
(3)平衡时,NO的转化率是_______ 。
(4)下列能说明反应达平衡状态的是_______(填字母)。
(5)NO会造成大气污染,在工业上采用多种方法进行处理。
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:
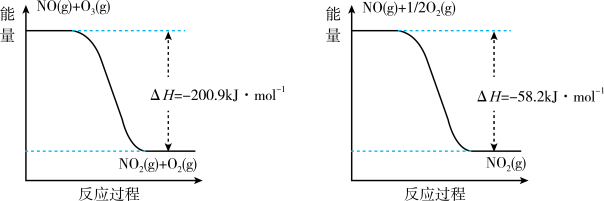
①请写出反应过程Ⅰ的热化学方程式_______ 。
②反应3NO(g) + O3(g)=3NO2(g) ΔH=_______ kJ•mol-1
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为_______ 。
 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
请回答:
(1)2 min内,v(O2) =
(2)800℃时,该反应的化学平衡常数数值为
(3)平衡时,NO的转化率是
(4)下列能说明反应达平衡状态的是_______(填字母)。
| A.单位时间内生成a mol O2的同时生成2a mol NO2 |
| B.混合气体的颜色不再改变 |
| C.混合气体的密度不再改变 |
| D.混合气体的平均相对分子质量不再改变 |
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:

①请写出反应过程Ⅰ的热化学方程式
②反应3NO(g) + O3(g)=3NO2(g) ΔH=
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为
您最近一年使用:0次
解题方法
3 . 煤的综合利用是合理利用资源,实现“绿色发展”的重要途径。图是某煤化工产业链的一部分
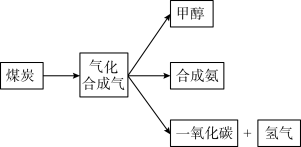
(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
①计算反应a消耗24 g C(s)时,反应放出的热量为_______ kJ。
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有_______ 。
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是_______ 。
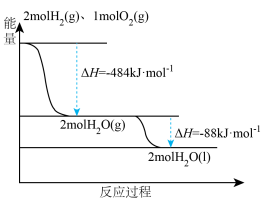
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为_______
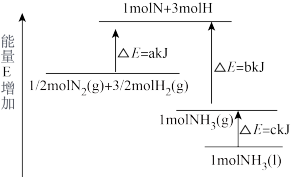
(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式_______ 。

(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1①计算反应a消耗24 g C(s)时,反应放出的热量为
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为

(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式

您最近一年使用:0次



