1 . 氢能是一种清洁能源,按照生产过程中的碳排放情况分为灰氢、蓝氢和绿氢。
(1)煤的气化制得灰氢 : 。该反应的平衡常数表达式K=
。该反应的平衡常数表达式K=_______ 。该方法生产过程有CO2排放。
(2)甲烷水蒸气催化重整制得蓝氢 ,步骤如下。
ⅰ.H2的制取:
 。为提高CH4的平衡转化率,可采取的措施有
。为提高CH4的平衡转化率,可采取的措施有_______ (写出两条即可)。
ⅱ.H2的富集:
 。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应
。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应_______ (填“已达到”或“未达到”)化学平衡状态,理由是_______ ,反应达平衡时CO的转化率为_______ 。
(3)热化学硫碘循环分解水制得绿氢 ,全程零碳排放。反应如下:
反应ⅰ: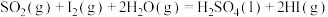
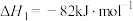
反应ⅱ: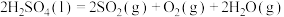
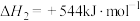
反应ⅲ:……
反应ⅰ~ⅲ循环可实现分解水:
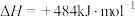
①已知破坏1 mol H2和破坏1 mol O2中化学键所消耗能量分别是436 kJ和498 kJ,则H2O中H-O键比H2中H-H键_______ (填“强”或“弱”)。
②写出反应ⅲ的热化学方程式_______ 。
(1)煤的气化制得
 。该反应的平衡常数表达式K=
。该反应的平衡常数表达式K=(2)甲烷水蒸气催化重整制得
ⅰ.H2的制取:

 。为提高CH4的平衡转化率,可采取的措施有
。为提高CH4的平衡转化率,可采取的措施有ⅱ.H2的富集:

 。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应
。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应(3)热化学硫碘循环分解水制得
反应ⅰ:
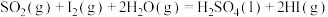
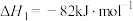
反应ⅱ:
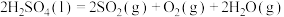
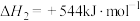
反应ⅲ:……
反应ⅰ~ⅲ循环可实现分解水:

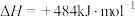
①已知破坏1 mol H2和破坏1 mol O2中化学键所消耗能量分别是436 kJ和498 kJ,则H2O中H-O键比H2中H-H键
②写出反应ⅲ的热化学方程式
您最近一年使用:0次
2023-01-14更新
|
142次组卷
|
2卷引用:北京市丰台区2022-2023学年高二上学期期中考试化学(A卷)试题
名校
解题方法
2 . 利用工业废气中的 合成基础化工原料甲醇
合成基础化工原料甲醇 ,是
,是 资源化的重要方法,涉及的主要化学反应有:
资源化的重要方法,涉及的主要化学反应有:
反应ⅰ: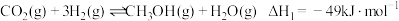
反应ⅱ: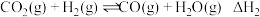
(1)反应ⅱ的化学平衡常数表达式为_______ 。
(2)已知: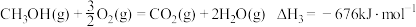 。利用
。利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的 。通过计算得出
。通过计算得出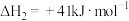 。
。
(3)控制反应条件(均使用了催化剂),研究投料比(反应物的物质的量之比)、压强、温度对反应体系的影响。
产率 和选择性S的定义:
和选择性S的定义: ,
,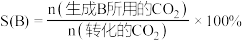
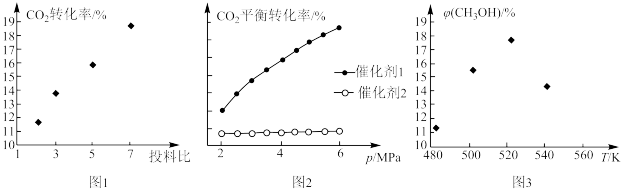
①图1中,投料比是指_______ (填“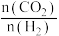 ”或“
”或“ ”);当投料比为5时,
”);当投料比为5时, 的转化率约为16%,
的转化率约为16%,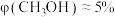 ,则
,则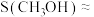
_______ 。
②图2中,在催化剂2的作用下,发生的主要反应是_______ (填“ⅰ”或“ⅱ”)。
③图3中,当温度高于 时,甲醇的产率随温度升高而减小,原因可能有
时,甲醇的产率随温度升高而减小,原因可能有_______ (写出2条)。
(4)一定条件下,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入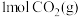 和
和 ,发生上述反应,t秒后达到平衡。此时容器中
,发生上述反应,t秒后达到平衡。此时容器中 为
为 ,
, 为
为 。
。
①平衡后 的浓度为
的浓度为_______  (用含a、b、V的代数式表示,下同)。
(用含a、b、V的代数式表示,下同)。
②用 的浓度变化表示
的浓度变化表示 秒内反应ⅱ的反应速率,
秒内反应ⅱ的反应速率,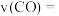
_______  。
。
③该条件下反应ⅰ的化学平衡常数为_______ 。
 合成基础化工原料甲醇
合成基础化工原料甲醇 ,是
,是 资源化的重要方法,涉及的主要化学反应有:
资源化的重要方法,涉及的主要化学反应有:反应ⅰ:
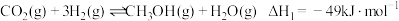
反应ⅱ:
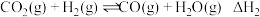
(1)反应ⅱ的化学平衡常数表达式为
(2)已知:
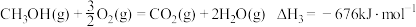 。利用
。利用 和
和 计算
计算 时,还需要利用
时,还需要利用 。通过计算得出
。通过计算得出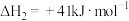 。
。(3)控制反应条件(均使用了催化剂),研究投料比(反应物的物质的量之比)、压强、温度对反应体系的影响。
产率
 和选择性S的定义:
和选择性S的定义: ,
,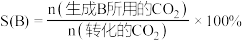

①图1中,投料比是指
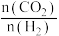 ”或“
”或“ ”);当投料比为5时,
”);当投料比为5时, 的转化率约为16%,
的转化率约为16%,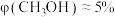 ,则
,则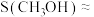
②图2中,在催化剂2的作用下,发生的主要反应是
③图3中,当温度高于
 时,甲醇的产率随温度升高而减小,原因可能有
时,甲醇的产率随温度升高而减小,原因可能有(4)一定条件下,向体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入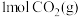 和
和 ,发生上述反应,t秒后达到平衡。此时容器中
,发生上述反应,t秒后达到平衡。此时容器中 为
为 ,
, 为
为 。
。①平衡后
 的浓度为
的浓度为 (用含a、b、V的代数式表示,下同)。
(用含a、b、V的代数式表示,下同)。②用
 的浓度变化表示
的浓度变化表示 秒内反应ⅱ的反应速率,
秒内反应ⅱ的反应速率,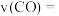
 。
。③该条件下反应ⅰ的化学平衡常数为
您最近一年使用:0次
2023-01-06更新
|
195次组卷
|
3卷引用:北京市丰台区2022-2023学年高二上学期期末考试化学试题
名校
解题方法
3 . 乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
I.工业用H2和CO2在一定条件下合成乙烯:
已知:①

②

③

(1)
_______ 。
(2)在密闭容器中充入体积比为 的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示,下列说法正确的是_______。
的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示,下列说法正确的是_______。

II.工业用甲烷催化法制取乙烯:
 , ,
, , 时,向2L的恒容反应器中充入
时,向2L的恒容反应器中充入 ,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图2所示。
,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图2所示。

(3)实验测得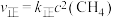 ,
, ,
,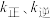 为速率常数,只与温度有关,T℃时
为速率常数,只与温度有关,T℃时 与
与 的比值为
的比值为_______ (用含x的代数式表示);若将温度升高,速率常数增大的倍数:
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
III.电化学法还原二氧化碳制乙烯原理如图3所示。

(4)阴极电极反应式为:_______ ;电路中转移0.3mol电子,两极共收集气体_______ L(标准状况)。
I.工业用H2和CO2在一定条件下合成乙烯:

已知:①


②


③


(1)

(2)在密闭容器中充入体积比为
 的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示,下列说法正确的是_______。
的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示,下列说法正确的是_______。
| A.为了提高乙烯的产率应尽可能选择低温 |
B.生成乙烯的速率: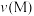 可能小于 可能小于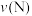 |
| C.M点时的压强一定小于N点时的压强 |
D.平衡常数: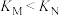 |
II.工业用甲烷催化法制取乙烯:

 , ,
, , 时,向2L的恒容反应器中充入
时,向2L的恒容反应器中充入 ,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图2所示。
,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图2所示。
(3)实验测得
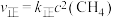 ,
, ,
,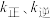 为速率常数,只与温度有关,T℃时
为速率常数,只与温度有关,T℃时 与
与 的比值为
的比值为
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。III.电化学法还原二氧化碳制乙烯原理如图3所示。

(4)阴极电极反应式为:
您最近一年使用:0次
名校
4 . 氧、硫、硒( )、碲(
)、碲( )、钋(
)、钋(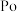 )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
(1) 在周期表中的位置为
在周期表中的位置为_______ 。
(2)某温度时,该族单质与 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下:
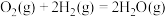

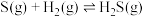


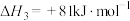
①硫和硒的氢化物的热稳定性:H2S_____ H2Se (填>、=或<);用原子结构知识解释你的判断结果_______ 。
②写出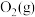 与
与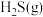 反应生成
反应生成 和
和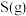 的热化学方程式
的热化学方程式_______ 。
(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为_______ 。
②生物浸出时的总反应的氧化剂是_______ 。
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: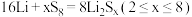 。下列说法
。下列说法错误 的是_______
 )、碲(
)、碲( )、钋(
)、钋( )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:(1)
 在周期表中的位置为
在周期表中的位置为(2)某温度时,该族单质与
 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下: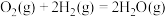

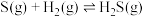


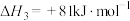
①硫和硒的氢化物的热稳定性:H2S
②写出
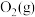 与
与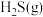 反应生成
反应生成 和
和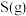 的热化学方程式
的热化学方程式(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为
②生物浸出时的总反应的氧化剂是
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极
 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: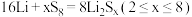 。下列说法
。下列说法
A.电池工作时,正极可发生反应: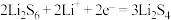 |
B.电池工作时,外电路中流过 电子,负极材料减重 电子,负极材料减重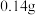 |
C.石墨烯的作用主要是提高电极 的导电性 的导电性 |
D.电池充电时间越长,电池中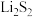 的量越多 的量越多 |
您最近一年使用:0次
2022-07-05更新
|
130次组卷
|
2卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
名校
解题方法
5 .  分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用
分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用 作为碳源,通过
作为碳源,通过 催化加氢方式,不仅可以减少温室气体的排放,还可以将
催化加氢方式,不仅可以减少温室气体的排放,还可以将 转化为高附加值的化学产品,具有重要的战略意义。
转化为高附加值的化学产品,具有重要的战略意义。
(1) 的结构与
的结构与 相似,写出
相似,写出 的电子式
的电子式_______ 。
(2)一种 直接加氢的反应机理如图a所示。
直接加氢的反应机理如图a所示。

①写出总反应的化学方程式_______ 。
②a、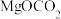 也可以写成
也可以写成 (难溶),写出
(难溶),写出 溶于乙酸的离子方程式
溶于乙酸的离子方程式_______ ;
b、 比
比 更难溶,加热
更难溶,加热 的水溶液可以生成
的水溶液可以生成 ,写出反应的化学方程式
,写出反应的化学方程式_______ 。
(3)①已知:主反应 催化加氢制甲醇是放热反应
催化加氢制甲醇是放热反应

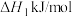

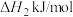
写出 催化加氢制甲醇的热化学方程式
催化加氢制甲醇的热化学方程式_______ ( 用含
用含 和
和 的代数式表示)。
的代数式表示)。
②已知
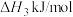 ,则
,则
_______  (填>、<或=)。
(填>、<或=)。
③我国科学家设计了离子液体电还原 合成
合成 工艺,写出碱性条件下
工艺,写出碱性条件下 生成甲醇的电极反应式
生成甲醇的电极反应式_______ 。
 分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用
分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用 作为碳源,通过
作为碳源,通过 催化加氢方式,不仅可以减少温室气体的排放,还可以将
催化加氢方式,不仅可以减少温室气体的排放,还可以将 转化为高附加值的化学产品,具有重要的战略意义。
转化为高附加值的化学产品,具有重要的战略意义。(1)
 的结构与
的结构与 相似,写出
相似,写出 的电子式
的电子式(2)一种
 直接加氢的反应机理如图a所示。
直接加氢的反应机理如图a所示。
①写出总反应的化学方程式
②a、
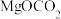 也可以写成
也可以写成 (难溶),写出
(难溶),写出 溶于乙酸的离子方程式
溶于乙酸的离子方程式b、
 比
比 更难溶,加热
更难溶,加热 的水溶液可以生成
的水溶液可以生成 ,写出反应的化学方程式
,写出反应的化学方程式(3)①已知:主反应
 催化加氢制甲醇是放热反应
催化加氢制甲醇是放热反应
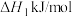

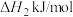
写出
 催化加氢制甲醇的热化学方程式
催化加氢制甲醇的热化学方程式 用含
用含 和
和 的代数式表示)。
的代数式表示)。②已知

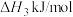 ,则
,则
 (填>、<或=)。
(填>、<或=)。③我国科学家设计了离子液体电还原
 合成
合成 工艺,写出碱性条件下
工艺,写出碱性条件下 生成甲醇的电极反应式
生成甲醇的电极反应式
您最近一年使用:0次
2022-06-19更新
|
146次组卷
|
2卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
名校
6 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

分析反应I:
反应I: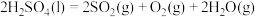

(1)它由两步反应组成:i.

ii. 分解,热化学方程式为
分解,热化学方程式为_______ 。
分析反应II:
(2)反应II的化学方程式是_______ 。
(3)反应II得到的产物用 进行分离。该产物的溶液在过量
进行分离。该产物的溶液在过量 的存在下会分成两层——含低浓度
的存在下会分成两层——含低浓度 的
的 层和高浓度的
层和高浓度的 的
的 层。
层。
①区分两层溶液可加入的试剂为_______ (填序号)。
A.淀粉溶液B.氯化钡溶液(资料: 易溶于水)
易溶于水)
C.硝酸银溶液D.氯化亚铁溶液
②根据上述事实,下列说法正确的是_______ (填序号)。
A.两层溶液的密度存在差异
B.加 前,
前, 溶液和
溶液和 溶液不互溶
溶液不互溶
C. 在
在 溶液中比在
溶液中比在 溶液中易溶
溶液中易溶
③经检测, 层中
层中 。其比值大于2的原因是
。其比值大于2的原因是_______ 。
分析反应Ⅲ:
(4)如表所示的数据是破坏1mol气态物质中的化学键所消耗的能量,请在下图中画出反应Ⅲ: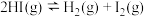 的能量变化示意图
的能量变化示意图_______ (不必标注具体数值)。


分析反应I:
反应I:
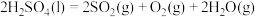

(1)它由两步反应组成:i.


ii.
 分解,热化学方程式为
分解,热化学方程式为分析反应II:
(2)反应II的化学方程式是
(3)反应II得到的产物用
 进行分离。该产物的溶液在过量
进行分离。该产物的溶液在过量 的存在下会分成两层——含低浓度
的存在下会分成两层——含低浓度 的
的 层和高浓度的
层和高浓度的 的
的 层。
层。①区分两层溶液可加入的试剂为
A.淀粉溶液B.氯化钡溶液(资料:
 易溶于水)
易溶于水)C.硝酸银溶液D.氯化亚铁溶液
②根据上述事实,下列说法正确的是
A.两层溶液的密度存在差异
B.加
 前,
前, 溶液和
溶液和 溶液不互溶
溶液不互溶C.
 在
在 溶液中比在
溶液中比在 溶液中易溶
溶液中易溶③经检测,
 层中
层中 。其比值大于2的原因是
。其比值大于2的原因是分析反应Ⅲ:
(4)如表所示的数据是破坏1mol气态物质中的化学键所消耗的能量,请在下图中画出反应Ⅲ:
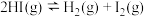 的能量变化示意图
的能量变化示意图
| 物质 |  |  |  |
| 能量(kJ) | 151 | 298 | 436 |
您最近一年使用:0次
名校
解题方法
7 . 依据图示关系,下列说法不正确 的是


A. |
| B.1 mol S(g)完全燃烧释放的能量小于2968 kJ |
C. |
| D.16 g S(s)完全燃烧释放的能量为1484 kJ |
您最近一年使用:0次
2022-03-25更新
|
1022次组卷
|
10卷引用:北京市丰台区2022届高三一模化学试题
北京市丰台区2022届高三一模化学试题辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)上海市上海中学2021-2022学年高一下学期期末考试化学试题北京市北京师范大学附属实验中学2022-2023学年高二上学期期中考试化学试题(已下线)第2讲 盖斯定律 反应热的计算北京市第二十二中学2023-2024学年高二上学期10月月考化学试题北京市中关村中学2023-2024学年高二上学期期中考试化学试题河南省郑州学森实验学校2023-2024学年高二上学期期中考试 化学试题
名校
解题方法
8 . 工业上制硫酸的主要反应之一为: ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
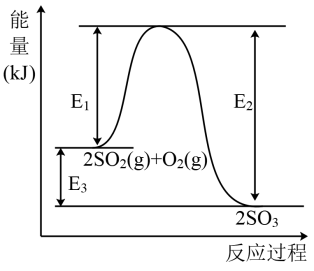
(1)向反应体系中加入催化剂后,图中
_______ (填“增大”、“减小”或“不变”,下同),
_______ 。
(2)已知:
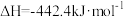

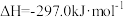
若 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为_______ 。
(3)某温度下,反应的起始浓度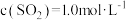 ,
,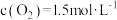 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为_______ 。
(4)在 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和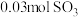 ,则反应开始时正反应速率
,则反应开始时正反应速率_______ (填“>”、“=”或“<”)逆反应速率。
(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
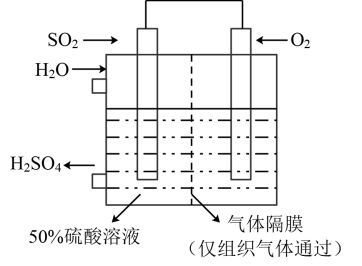
(6)若以如图所示装置生产硫酸,将 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为_______ 。
 ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
(1)向反应体系中加入催化剂后,图中


(2)已知:

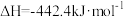

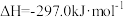
若
 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为(3)某温度下,反应的起始浓度
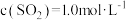 ,
,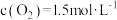 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为(4)在
 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和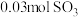 ,则反应开始时正反应速率
,则反应开始时正反应速率(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
A. 的体积分数不再发生变化 的体积分数不再发生变化 |
| B.恒容时,容器内压强不再发生变化 |
| C.容器内,气体原子总数不再发生变化 |
D.相同时间内消耗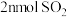 的同时生成 的同时生成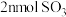 |
 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为
您最近一年使用:0次
2022-01-21更新
|
283次组卷
|
2卷引用:北京市丰台区2021~2022学年高二上学期期末考试化学试题
名校
9 . 某天然气含CH4和一定量的CO2。以天然气为原料制备苯和氢气的工艺流程如下图所示:_______ 。
(2)由甲烷制备苯的过程中存在如下反应:
芳构化反应:6CH4(g) C6H6(g)+9H2(g) ΔH1
C6H6(g)+9H2(g) ΔH1
积碳反应:CH4(g) C(s)+2H2(g) ΔH2
C(s)+2H2(g) ΔH2
若要用ΔH1计算ΔH2,则还需要利用_______ 反应的ΔH。
(3)已知不同温度和压强下,甲烷芳构化反应中甲烷的平衡转化率如图所示:_______ 0(填“>”或“<”)
②P1、P2的大小关系是_______ ,理由是_______ 。
(4)在适宜温度下,以金属Mo作催化剂,由甲烷制备苯,几个小时后,单位时间内苯的产量迅速下降,主要原因是_______ 。

(2)由甲烷制备苯的过程中存在如下反应:
芳构化反应:6CH4(g)
 C6H6(g)+9H2(g) ΔH1
C6H6(g)+9H2(g) ΔH1积碳反应:CH4(g)
 C(s)+2H2(g) ΔH2
C(s)+2H2(g) ΔH2若要用ΔH1计算ΔH2,则还需要利用
(3)已知不同温度和压强下,甲烷芳构化反应中甲烷的平衡转化率如图所示:

②P1、P2的大小关系是
(4)在适宜温度下,以金属Mo作催化剂,由甲烷制备苯,几个小时后,单位时间内苯的产量迅速下降,主要原因是
您最近一年使用:0次
2022-01-14更新
|
369次组卷
|
5卷引用:北京市丰台区2021-2022学年高三上学期期末考试化学试题
北京市丰台区2021-2022学年高三上学期期末考试化学试题(已下线)二轮拔高卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)北京市东城区一六六中学2022-2023学年高三上学期期中考试化学试题山东省临沂市沂水县2022-2023学年高二上学期学科素养(期中)检测化学试题北京市第五十五中学2023-2024学年高二下学期期中调研化学试题
名校
10 . 氧化亚铜是一种重要的工业原料。已知1 g C(s)燃烧生成一氧化碳放出9.2 kJ的热量,氧化亚铜与氧气反应的能量变化如图所示。下列有关判断正确的是


| A.碳[C(s)]的燃烧热△H = -110.4 kJ·mol-1 |
| B.氧化亚铜与氧气的反应为吸热反应 |
| C.氧化亚铜与氧气反应的活化能为292 kJ·mol-1 |
| D.C(s)+2CuO(s)=Cu2O(s)+CO(g) △H= +35.6 kJ·mol-1 |
您最近一年使用:0次
2020-11-06更新
|
333次组卷
|
5卷引用:北京市第八十中学2022-2023学年高二上学期期末适应测试化学试题



