解题方法
1 . 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。下图是1mol NO2(g)和 1mol CO(g)反应生成 1mol CO2(g)和 1mol NO(g)过程中能量变化示意图。
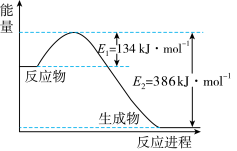
(1)请写出反应的热化学方程式___________ 。
(2)若在该反应体系中加入催化剂对反应热___________ (填“有”或“没有”)影响。原因是 ___________ 。

(1)请写出反应的热化学方程式
(2)若在该反应体系中加入催化剂对反应热
您最近一年使用:0次
2 . 甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
I.甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为___________ 。
(2)已知:25℃、101 kPa时,CH3OH(l) + 3/2 O2(g) = CO2 (g) + 2H2O(l) Δ H=-726.5 kJ/mol,相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是___________ 。
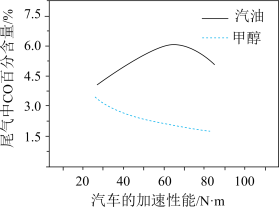
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如下图所示。根据下图信息分析,与汽油相比,甲醇作为燃料的优点是___________ 。
II.甲醇的合成
(4)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
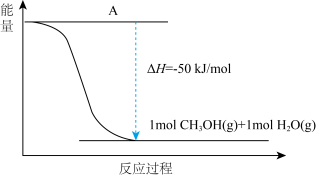
①补全上图:图中A处应填入___________ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH___________ 。(填“变大”“变小”或“不变”)
(5)为了合成甲醇反应:CO(g) + 2H2(g) = CH3OH(g) ΔH =-91kJ/mol
已知:i.CO(g)+1/2 O2(g) = CO2(g) Δ H1=-283 kJ/mol
ii. ∙∙∙∙∙∙ ΔH2
iii.CH3OH(g) + 3/2 O2(g) = CO2 (g) + 2H2O(g) ΔH3=-676 kJ/mol
还需要利用反应ii,请写出该反应的热化学反应方程式_______________________ 。
(6)用稀硫酸作电解质溶液,电解CO2也可制取CH3OH,装置如下图所示,电极b为电解池的___________ 极(填“阴”或“阳”),生成 的电极反应式是
的电极反应式是___________ 。

I.甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为
(2)已知:25℃、101 kPa时,CH3OH(l) + 3/2 O2(g) = CO2 (g) + 2H2O(l) Δ H=-726.5 kJ/mol,相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如下图所示。根据下图信息分析,与汽油相比,甲醇作为燃料的优点是

II.甲醇的合成
(4)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

①补全上图:图中A处应填入
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH
(5)为了合成甲醇反应:CO(g) + 2H2(g) = CH3OH(g) ΔH =-91kJ/mol
已知:i.CO(g)+1/2 O2(g) = CO2(g) Δ H1=-283 kJ/mol
ii. ∙∙∙∙∙∙ ΔH2
iii.CH3OH(g) + 3/2 O2(g) = CO2 (g) + 2H2O(g) ΔH3=-676 kJ/mol
还需要利用反应ii,请写出该反应的热化学反应方程式
(6)用稀硫酸作电解质溶液,电解CO2也可制取CH3OH,装置如下图所示,电极b为电解池的
 的电极反应式是
的电极反应式是
您最近一年使用:0次
解题方法
3 . 研究CO2的回收和综合利用对航天建设有重要意义。
Ⅰ.载人航天器中,利用萨巴蒂尔反应可将航天员呼出的CO2转化为 H2O,再通过电解H2O 获得 O2,实现O2的再生,同时还能制备CH4。已知:
反应①:CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H = −252.9kJ/mol
反应②:2H2O(l)=2H2(g)+O2(g) ∆H = +571.6kJ/mol
请回答下列问题:
(1)反应①属于___________ (填“吸热”或“放热”)反应。
(2)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
已知2CH4(g)=C2H4(g)+2H2(g) ΔH =+167kJ/mol,则a=___________ 。
Ⅱ.回收利用CO2是目前解决长期载人航天舱内(如空间站)供氧问题的有效途径,科研人员研究出其物质转化途径如下图:
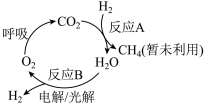
(3)反应A为CO2(g)+4H2(g) CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
已知:2H2(g) + O2(g) = 2H2O(g) ΔH = −483.6 kJ·mol−1
CH4(g) + 2O2(g) = 2H2O(g) + CO2(g) ΔH = −802.3 kJ·mol−1
反应A的ΔH =___________ kJ·mol−1
(4)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。
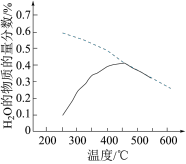
①理论上,能提高CO2平衡转化率的措施有___________ (写出一条即可)。
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是___________ 。
(5)下列关于空间站内物质和能量变化的说法中,不正确 的是___________ (填字母)。
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(6)用CO2(g)+2H2(g) C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是___________ 。
Ⅰ.载人航天器中,利用萨巴蒂尔反应可将航天员呼出的CO2转化为 H2O,再通过电解H2O 获得 O2,实现O2的再生,同时还能制备CH4。已知:
反应①:CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H = −252.9kJ/mol
反应②:2H2O(l)=2H2(g)+O2(g) ∆H = +571.6kJ/mol
请回答下列问题:
(1)反应①属于
(2)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
Ⅱ.回收利用CO2是目前解决长期载人航天舱内(如空间站)供氧问题的有效途径,科研人员研究出其物质转化途径如下图:

(3)反应A为CO2(g)+4H2(g)
 CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。已知:2H2(g) + O2(g) = 2H2O(g) ΔH = −483.6 kJ·mol−1
CH4(g) + 2O2(g) = 2H2O(g) + CO2(g) ΔH = −802.3 kJ·mol−1
反应A的ΔH =
(4)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。

①理论上,能提高CO2平衡转化率的措施有
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是
(5)下列关于空间站内物质和能量变化的说法中,
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(6)用CO2(g)+2H2(g)
 C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近一年使用:0次
解题方法
4 . 工业上可以利用水煤气( 、
、 )合成二甲醚(
)合成二甲醚( ),同时生成
),同时生成 。合成过程中,主要发生三个反应,
。合成过程中,主要发生三个反应, ℃时,有关反应及相关数据如下。
℃时,有关反应及相关数据如下。

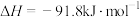
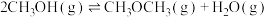
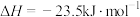


保持原料气组成、压强、反应时间等因素不变,进行实验,测得 转化率随温度变化曲线如下图。下列说法不正确的是
转化率随温度变化曲线如下图。下列说法不正确的是
 、
、 )合成二甲醚(
)合成二甲醚( ),同时生成
),同时生成 。合成过程中,主要发生三个反应,
。合成过程中,主要发生三个反应, ℃时,有关反应及相关数据如下。
℃时,有关反应及相关数据如下。
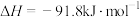
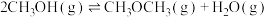
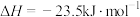


保持原料气组成、压强、反应时间等因素不变,进行实验,测得
 转化率随温度变化曲线如下图。下列说法不正确的是
转化率随温度变化曲线如下图。下列说法不正确的是
A. ℃时,水煤气合成二甲醚的热化学方程式: ℃时,水煤气合成二甲醚的热化学方程式:  |
B. ℃时,增大压强、加入催化剂均可提高 ℃时,增大压强、加入催化剂均可提高 的平衡转化率 的平衡转化率 |
C.220℃~240℃时,温度升高反应速率加快, 转化率升高 转化率升高 |
D.温度高于240℃时,温度升高 转化率降低的原因可能是平衡逆向移动 转化率降低的原因可能是平衡逆向移动 |
您最近一年使用:0次
名校
解题方法
5 . 将天然气(主要成分为 )中的
)中的 、
、 资源化转化在能源利用。环境保护等方面意义重大。
资源化转化在能源利用。环境保护等方面意义重大。
(1) 转化为CO、
转化为CO、 转化为S的反应如下:
转化为S的反应如下:
i.
 kJ/mol
kJ/mol
ii.
 kJ/mol
kJ/mol
iii. 、
、 转化生成CO、S等物质的热化学方程是
转化生成CO、S等物质的热化学方程是___________ 。
(2) 性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低反应的
性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低反应的___________ ,提高反应速率。
a.活化能 b. c.平衡常数
c.平衡常数
(3)我国科学家通过研制新型催化剂,设计协同转化装置实现反应,工作原理如图所示。
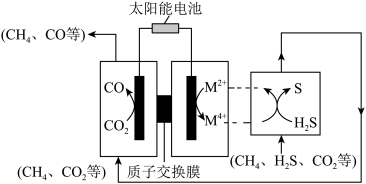
【方案1】若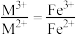
①结合化学用语说明生成S、CO的原理:___________ 。
【方案2】若
电流效率 的定义
的定义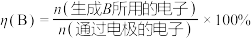
②测得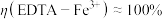 ,
,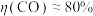 ,阴极放电的物质有
,阴极放电的物质有___________ ;
③为进一步确认 、
、 能协同转化,对CO的来源分析如下:
能协同转化,对CO的来源分析如下:
来源1: 通过电极反应产生CO;
通过电极反应产生CO;
来源2:电解质(含碳元素)等碳基材料发生降解,产生CO。
设计实验探究,证实来源2不成立。实验方案是___________ 。
结论:方案2明显优于方案1。该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
 )中的
)中的 、
、 资源化转化在能源利用。环境保护等方面意义重大。
资源化转化在能源利用。环境保护等方面意义重大。(1)
 转化为CO、
转化为CO、 转化为S的反应如下:
转化为S的反应如下:i.

 kJ/mol
kJ/molii.

 kJ/mol
kJ/moliii.
 、
、 转化生成CO、S等物质的热化学方程是
转化生成CO、S等物质的热化学方程是(2)
 性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低反应的
性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低反应的a.活化能 b.
 c.平衡常数
c.平衡常数(3)我国科学家通过研制新型催化剂,设计协同转化装置实现反应,工作原理如图所示。

【方案1】若
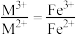
①结合化学用语说明生成S、CO的原理:
【方案2】若

电流效率
 的定义
的定义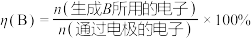
②测得
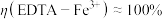 ,
,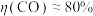 ,阴极放电的物质有
,阴极放电的物质有③为进一步确认
 、
、 能协同转化,对CO的来源分析如下:
能协同转化,对CO的来源分析如下:来源1:
 通过电极反应产生CO;
通过电极反应产生CO;来源2:电解质(含碳元素)等碳基材料发生降解,产生CO。
设计实验探究,证实来源2不成立。实验方案是
结论:方案2明显优于方案1。该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
名校
6 . 下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说法正确的是
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
①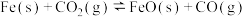  |  | 1.47 | 2.15 |
②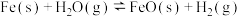  |  | 2.38 | 1.67 |
③  |  | a | b |
A.1173K时,反应①起始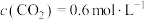 ,平衡时 ,平衡时 约为0.4 约为0.4 |
B.反应②是吸热反应, |
| C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动 |
D.相同温度下, ; ;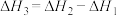 |
您最近一年使用:0次
2023-03-24更新
|
727次组卷
|
7卷引用:北京市丰台区2022-2023学年高三下学期第一次模拟练习化学试题
北京市丰台区2022-2023学年高三下学期第一次模拟练习化学试题(已下线)专题15 化学反应速率和化学平衡海南省海南中学2023届高三下学期第三次模拟考试化学试题湖北省黄冈市重点校2022-2023学年高一下学期期末综合选拔性联考化学试题北京市第一六一中学2023-2024学年高三上学期12月月考化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)北京市顺义区第二中学2023-2024学年高三下学期3月月考化学试题
7 .  资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:
反应I:

反应II: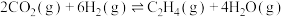

(1)基态镍原子核外电子的轨道表示式为____________
(2)将反应后气体通入______ (填试剂名称),可证明反应II发生。
(3)计算

______ (用 和
和 表示)
表示)
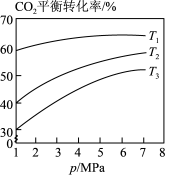
(4)相同投料比时,体系内 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为________ 。
(5)向1 L恒压、密闭容器中通入1 mol 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
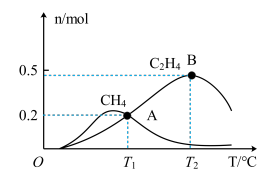
①催化剂在较低温度时主要选择______ (填“反应I”或“反应II”)
② 时
时 的转化率为
的转化率为______ ,反应I的平衡常数
______ 。
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:
 +75 kJ/mol
+75 kJ/mol
消碳反应:
 -173 kJ/mol
-173 kJ/mol
其他条件相同时,催化剂表面积碳量与温度的关系如图所示, ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是______ 。

 资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:反应I:


反应II:
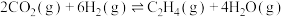

(1)基态镍原子核外电子的轨道表示式为
(2)将反应后气体通入
(3)计算


 和
和 表示)
表示)(4)相同投料比时,体系内
 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
(5)向1 L恒压、密闭容器中通入1 mol
 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
①催化剂在较低温度时主要选择
②
 时
时 的转化率为
的转化率为
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:

 +75 kJ/mol
+75 kJ/mol消碳反应:

 -173 kJ/mol
-173 kJ/mol其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
 ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是
您最近一年使用:0次
名校
解题方法
8 . 富钴结壳浸出液分离 制备
制备 的工业流程如下。
的工业流程如下。
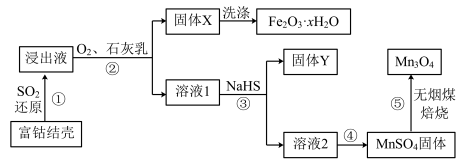
已知:i.浸出液中主要含有的金属离子为: 、
、 、
、 、
、 、
、
ii.25℃时,金属硫化物的溶度积常数。
(1)过程①中, 还原得到的浸出液中含硫元素的阴离子主要为
还原得到的浸出液中含硫元素的阴离子主要为_______ 。
(2)过程②中, 转化为
转化为 时,氧气和石灰乳的作用分别是
时,氧气和石灰乳的作用分别是_______ 。
(3)固体Y中主要物质的化学式为_______ 。
(4)已知, 在
在 时完全沉淀转化为
时完全沉淀转化为 。过程③中沉淀剂不选择
。过程③中沉淀剂不选择 的原因可能是
的原因可能是_______ 。
(5)已知,温度高于20℃时, 在水中的溶解度随温度升高迅速降低。过程④中,采用的操作是
在水中的溶解度随温度升高迅速降低。过程④中,采用的操作是_______ 。
(6)过程⑤中发生下列反应。



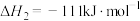
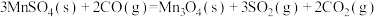

利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的 。
。
(7)流程中可循环使用的物质是_______ 。
 制备
制备 的工业流程如下。
的工业流程如下。
已知:i.浸出液中主要含有的金属离子为:
 、
、 、
、 、
、 、
、
ii.25℃时,金属硫化物的溶度积常数。
| 金属硫化物 | NiS | CoS | CuS | MnS |
 | 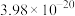 | 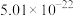 | 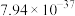 | 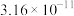 |
 还原得到的浸出液中含硫元素的阴离子主要为
还原得到的浸出液中含硫元素的阴离子主要为(2)过程②中,
 转化为
转化为 时,氧气和石灰乳的作用分别是
时,氧气和石灰乳的作用分别是(3)固体Y中主要物质的化学式为
(4)已知,
 在
在 时完全沉淀转化为
时完全沉淀转化为 。过程③中沉淀剂不选择
。过程③中沉淀剂不选择 的原因可能是
的原因可能是(5)已知,温度高于20℃时,
 在水中的溶解度随温度升高迅速降低。过程④中,采用的操作是
在水中的溶解度随温度升高迅速降低。过程④中,采用的操作是(6)过程⑤中发生下列反应。



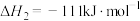
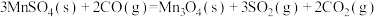

利用
 和
和 计算
计算 时,还需要利用
时,还需要利用 。
。(7)流程中可循环使用的物质是
您最近一年使用:0次
2023-01-05更新
|
317次组卷
|
2卷引用:北京市丰台区2022-2023学年高三上学期期末考试化学试题
名校
解题方法
9 .  与
与 能发生反应:
能发生反应:
 。
。
已知:
①该反应由两个基元反应分步完成,第一步为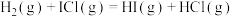

②两步反应的活化能分别为 、
、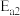 ,且
,且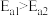
下列判断不正确 的是
 与
与 能发生反应:
能发生反应:
 。
。已知:
①该反应由两个基元反应分步完成,第一步为
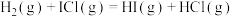

②两步反应的活化能分别为
 、
、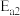 ,且
,且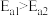
下列判断
| A.第一步为氧化还原反应 |
| B.第一步的化学反应速率大于第二步的化学反应速率 |
C.已知键能: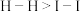 ,可推知键能: ,可推知键能: |
D.第二步的热化学方程式为 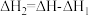 |
您最近一年使用:0次
2022-01-14更新
|
454次组卷
|
5卷引用:北京市第十二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 .  催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。

下列说法不正确 的是
 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法
| A.由图1推知反应物断键吸收的能量小于生成物成键释放的能量 |
B.图2中,若生成的 为液态,则能量变化曲线为① 为液态,则能量变化曲线为① |
C. |
D.制备 的反应使用催化剂时,其 的反应使用催化剂时,其 不变 不变 |
您最近一年使用:0次
2021-05-10更新
|
792次组卷
|
8卷引用:北京市第十二中学2023-2024学年高二上学期期中考试化学试题
北京市第十二中学2023-2024学年高二上学期期中考试化学试题(已下线)题型14 从吸热与放热角度突破反应热图像北京交通大学附属中学2023-2024学年高三上学期12月月考化学试题 北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)北京一零一中学2020-2021学年高一下学期期末考试化学试题湖南省五市十校教研教改共同体2021-2022学年高一下学期期末考试化学试题河南省中原名校2022-2023学年高二上学期第一次联考化学试题



