名校
解题方法
1 . 我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和。而研发 的碳捕捉和碳利用技术则是关键。通过各国科技工作者的努力,已经开发出许多将
的碳捕捉和碳利用技术则是关键。通过各国科技工作者的努力,已经开发出许多将 回收利用的技术。回答下列问题:
回收利用的技术。回答下列问题:
(1) 在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。



获取乙二醇的反应历程可分为如下2步:
I. ;
;
II. 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。
步骤II的热化学方程式是___________ 。
(2)通过人工光合作用,以 和
和 为原料制备
为原料制备 和
和 的工作原理如图所示。
的工作原理如图所示。
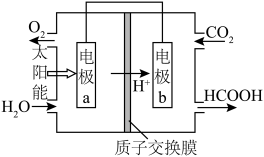
电极 上的电极反应式为
上的电极反应式为___________ 。
(3)研究表明,在电解质水溶液中, 气体可被电化学还原。
气体可被电化学还原。 在碱性介质中电还原为正丙醇
在碱性介质中电还原为正丙醇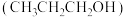 的电极反应式为
的电极反应式为___________ 。
(4)一种聚合物锂电池通过充、放电可实现“大气固碳”(工作原理如图所示)。该电池在充电时,通过催化剂的选择性控制,只有 发生氧化释放出
发生氧化释放出 和
和 。图中
。图中 的移动方向是
的移动方向是___________ (填“充电”或“放电”)时的移动方向;充电时,阳极的电极反应式为___________ ;该电池每循环充、放电子各 ,理论上可固定
,理论上可固定
___________ L(标准状况下)。

 的碳捕捉和碳利用技术则是关键。通过各国科技工作者的努力,已经开发出许多将
的碳捕捉和碳利用技术则是关键。通过各国科技工作者的努力,已经开发出许多将 回收利用的技术。回答下列问题:
回收利用的技术。回答下列问题:(1)
 在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。


获取乙二醇的反应历程可分为如下2步:
I.
 ;
;II.
 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。步骤II的热化学方程式是
(2)通过人工光合作用,以
 和
和 为原料制备
为原料制备 和
和 的工作原理如图所示。
的工作原理如图所示。
电极
 上的电极反应式为
上的电极反应式为(3)研究表明,在电解质水溶液中,
 气体可被电化学还原。
气体可被电化学还原。 在碱性介质中电还原为正丙醇
在碱性介质中电还原为正丙醇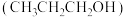 的电极反应式为
的电极反应式为(4)一种聚合物锂电池通过充、放电可实现“大气固碳”(工作原理如图所示)。该电池在充电时,通过催化剂的选择性控制,只有
 发生氧化释放出
发生氧化释放出 和
和 。图中
。图中 的移动方向是
的移动方向是 ,理论上可固定
,理论上可固定

您最近半年使用:0次
名校
解题方法
2 .  是空气的主要污染物之一,有效去除大气中的
是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。含氮废水氨氮(以
可以保护大气环境。含氮废水氨氮(以 存在)和硝态氮(以
存在)和硝态氮(以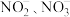 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。
(1)空气中污染物 可在催化剂作用下用
可在催化剂作用下用 还原。
还原。
已知: ;
;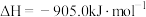
 ;
;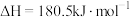
有氧条件下, 与
与 反应生成
反应生成 ,相关热化学方程式为
,相关热化学方程式为
 ;
;
___________  。
。
(2)工业上含氮化合物污染物处理
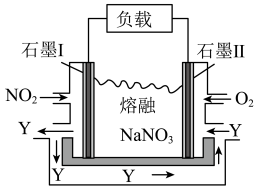
①以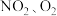 、熔融
、熔融 组成的燃料电池装置如图所示,在使用过程中石墨I电极反应生成一种氧化物
组成的燃料电池装置如图所示,在使用过程中石墨I电极反应生成一种氧化物 ,则该电池的正极反应式为
,则该电池的正极反应式为___________ 。
②纳米铁粉可用于处理含氮废水。用纳米铁粉处理水体中的 ,反应的离子方程式为
,反应的离子方程式为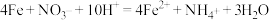 。研究发现,若
。研究发现,若 偏低将会导致
偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是___________ 。相同条件下,纳米铁粉去除不同水样中 的速率有较大差异(如图),产生该差异的可能原因是
的速率有较大差异(如图),产生该差异的可能原因是___________ 。

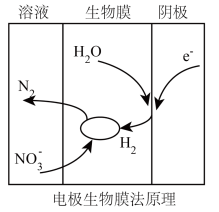
③电极生物膜法也能有效去除水体中的 ,进行生物的反硝化反应,其可能反应机理如图所示。以必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应,其可能反应机理如图所示。以必要的化学用语及文字来描述此过程为___________ 。
 是空气的主要污染物之一,有效去除大气中的
是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。含氮废水氨氮(以
可以保护大气环境。含氮废水氨氮(以 存在)和硝态氮(以
存在)和硝态氮(以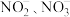 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。(1)空气中污染物
 可在催化剂作用下用
可在催化剂作用下用 还原。
还原。已知:
 ;
;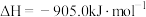
 ;
;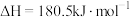
有氧条件下,
 与
与 反应生成
反应生成 ,相关热化学方程式为
,相关热化学方程式为 ;
;
 。
。(2)工业上含氮化合物污染物处理
①以
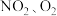 、熔融
、熔融 组成的燃料电池装置如图所示,在使用过程中石墨I电极反应生成一种氧化物
组成的燃料电池装置如图所示,在使用过程中石墨I电极反应生成一种氧化物 ,则该电池的正极反应式为
,则该电池的正极反应式为
②纳米铁粉可用于处理含氮废水。用纳米铁粉处理水体中的
 ,反应的离子方程式为
,反应的离子方程式为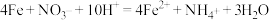 。研究发现,若
。研究发现,若 偏低将会导致
偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是 的速率有较大差异(如图),产生该差异的可能原因是
的速率有较大差异(如图),产生该差异的可能原因是
③电极生物膜法也能有效去除水体中的
 ,进行生物的反硝化反应,其可能反应机理如图所示。以必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应,其可能反应机理如图所示。以必要的化学用语及文字来描述此过程为
您最近半年使用:0次
3 . 下列说法正确的是
已知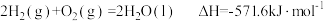
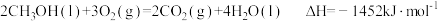
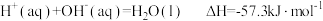
已知
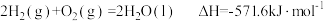
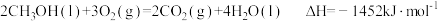
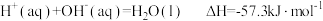
| A.H2(g)的燃烧热ΔH=-571.6kJ•mol-1 |
B.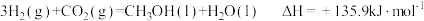 |
C.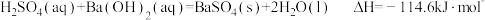 |
| D.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
您最近半年使用:0次
2023-10-05更新
|
63次组卷
|
2卷引用:江苏省常州市前黄高级中学2022-2023学年高二上学期第二次阶段考试化学试题
4 . 推动 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。
(1) 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:
反应Ⅰ:
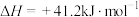
反应Ⅱ:
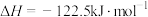
①反应

_____  。
。
②下列有关反应Ⅱ:
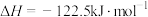 的说法正确的是
的说法正确的是_____ 。
A.升高温度逆反应速率加快,正反应速率减慢
B.反应体系中 浓度不再变化,说明反应达到平衡状态
浓度不再变化,说明反应达到平衡状态
C.恒温恒容下达到平衡后,再通入 ,平衡向正反应方向移动
,平衡向正反应方向移动
D.平衡时,若改变体积增大压强,则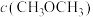 、
、 均变大
均变大
在恒压、 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性=
的选择性=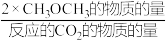 ×100%
×100%
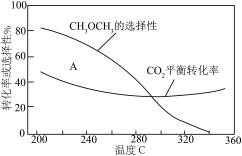
③温度高于300℃, 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是_____ 。
④220℃时,在催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:48%(图中A点)。不改变反应时间和温度,一定能提高
的选择性为:48%(图中A点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:_____ 。
(2) 催化还原法。
催化还原法。
如图表示的是利用 “直接电子传递机理”。在催化剂铜表面进行转化。当有
“直接电子传递机理”。在催化剂铜表面进行转化。当有 反应时,直接传递的电子物质的量为
反应时,直接传递的电子物质的量为_____ mol。
(3) 电化学催化重整法。
电化学催化重整法。
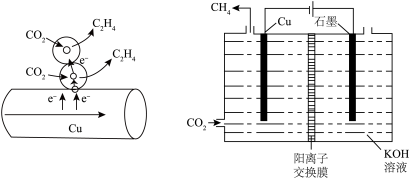
①如图表示以 溶液作电解质溶液进行电解的示意图,
溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为_____ 。
②电解一段时间后,阳极区溶液pH减小,其原因是_____ 。
(4)甲酸 是重要的液态储氢原料。将温室气体
是重要的液态储氢原料。将温室气体 转化为甲酸既具有经济技术意义,又具有环保意义。在实践中,
转化为甲酸既具有经济技术意义,又具有环保意义。在实践中, 制备甲酸的一种流程如下:
制备甲酸的一种流程如下:

①写出过程Ⅱ的离子方程式_____ 。
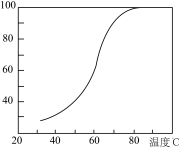
②过程Ⅱ中,其他条件不变, 转化为
转化为 的转化率如图所示。则在40℃~80℃范围内转化率迅速上升,其主要原因可能是
的转化率如图所示。则在40℃~80℃范围内转化率迅速上升,其主要原因可能是_____ 。
 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。(1)
 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:反应Ⅰ:

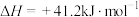
反应Ⅱ:

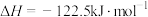
①反应


 。
。②下列有关反应Ⅱ:

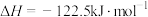 的说法正确的是
的说法正确的是A.升高温度逆反应速率加快,正反应速率减慢
B.反应体系中
 浓度不再变化,说明反应达到平衡状态
浓度不再变化,说明反应达到平衡状态C.恒温恒容下达到平衡后,再通入
 ,平衡向正反应方向移动
,平衡向正反应方向移动D.平衡时,若改变体积增大压强,则
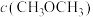 、
、 均变大
均变大在恒压、
 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性=
的选择性=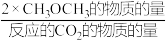 ×100%
×100%
③温度高于300℃,
 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是④220℃时,在催化剂作用下
 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:48%(图中A点)。不改变反应时间和温度,一定能提高
的选择性为:48%(图中A点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:(2)
 催化还原法。
催化还原法。如图表示的是利用
 “直接电子传递机理”。在催化剂铜表面进行转化。当有
“直接电子传递机理”。在催化剂铜表面进行转化。当有 反应时,直接传递的电子物质的量为
反应时,直接传递的电子物质的量为(3)
 电化学催化重整法。
电化学催化重整法。
①如图表示以
 溶液作电解质溶液进行电解的示意图,
溶液作电解质溶液进行电解的示意图, 在Cu电极上可以转化为
在Cu电极上可以转化为 ,该电极反应的方程式为
,该电极反应的方程式为②电解一段时间后,阳极区溶液pH减小,其原因是
(4)甲酸
 是重要的液态储氢原料。将温室气体
是重要的液态储氢原料。将温室气体 转化为甲酸既具有经济技术意义,又具有环保意义。在实践中,
转化为甲酸既具有经济技术意义,又具有环保意义。在实践中, 制备甲酸的一种流程如下:
制备甲酸的一种流程如下:
①写出过程Ⅱ的离子方程式
②过程Ⅱ中,其他条件不变,
 转化为
转化为 的转化率如图所示。则在40℃~80℃范围内转化率迅速上升,其主要原因可能是
的转化率如图所示。则在40℃~80℃范围内转化率迅速上升,其主要原因可能是
您最近半年使用:0次
5 . 我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。研发CO2资源化利用技术,降低空气中CO2含量成为世界各国研究热点。
(1)CO2和CH4重整可制合成气(主要成分为CO和H2),其热化学反应方程式:
CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247kJ·mol-1
已知下列热化学反应方程式:
反应1:C(s)+2H2(g) = CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2 =-40.0kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3 =+132.0kJ·mol-1
①ΔH1 =_______ kJ·mol-1
②CO(g)+H2O(l)=CO2(g)+H2(g) ΔH_______ -40.0kJ·mol-1(填“<”“>”或“=”)
③反应3中加入催化剂,ΔH3_______ (填“减小”“增大”或“不变”)
(2)二甲醚(CH3OCH3)被认为是最具潜力的燃料。在密闭容器中充入CO2与H2反应可以制得CH3OCH3:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);采用催化剂A和催化剂B分别发生上述反应,测得反应进行相同时间时H2的转化率α(H2)随反应温度T的变化曲线如图所示(忽略温度对催化剂活性的影响):
CH3OCH3(g)+3H2O(g);采用催化剂A和催化剂B分别发生上述反应,测得反应进行相同时间时H2的转化率α(H2)随反应温度T的变化曲线如图所示(忽略温度对催化剂活性的影响):

①该反应为_______ 反应(填“吸热”或“放热”)
②下列哪种情况的活化能更大_______
a. 催化剂A作用下的反应 b. 催化剂B作用下的反应
③600K达到平衡时,反应在催化剂A作用下的转化率_______ (填“高于”、“低于”或“等于”)在催化剂B作用下的转化率。
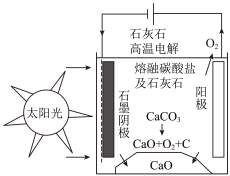
(3)研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示。温度小于900℃时进行电解反应,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO - 4e-= 2CO2↑ + O2↑,则阴极的电极反应式为
- 4e-= 2CO2↑ + O2↑,则阴极的电极反应式为_______ 。
(1)CO2和CH4重整可制合成气(主要成分为CO和H2),其热化学反应方程式:
CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247kJ·mol-1
已知下列热化学反应方程式:
反应1:C(s)+2H2(g) = CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2 =-40.0kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3 =+132.0kJ·mol-1
①ΔH1 =
②CO(g)+H2O(l)=CO2(g)+H2(g) ΔH
③反应3中加入催化剂,ΔH3
(2)二甲醚(CH3OCH3)被认为是最具潜力的燃料。在密闭容器中充入CO2与H2反应可以制得CH3OCH3:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g);采用催化剂A和催化剂B分别发生上述反应,测得反应进行相同时间时H2的转化率α(H2)随反应温度T的变化曲线如图所示(忽略温度对催化剂活性的影响):
CH3OCH3(g)+3H2O(g);采用催化剂A和催化剂B分别发生上述反应,测得反应进行相同时间时H2的转化率α(H2)随反应温度T的变化曲线如图所示(忽略温度对催化剂活性的影响):
①该反应为
②下列哪种情况的活化能更大
a. 催化剂A作用下的反应 b. 催化剂B作用下的反应
③600K达到平衡时,反应在催化剂A作用下的转化率
(3)研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示。温度小于900℃时进行电解反应,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO
 - 4e-= 2CO2↑ + O2↑,则阴极的电极反应式为
- 4e-= 2CO2↑ + O2↑,则阴极的电极反应式为
您最近半年使用:0次
解题方法
6 . 含N元素的部分物质对环境有影响。含NO、 的废气会引起空气污染,含
的废气会引起空气污染,含 、
、 、
、 的废水会引起水体富营养化,都需要经过处理后才能排放。
的废水会引起水体富营养化,都需要经过处理后才能排放。
(1)氢气催化还原含NO烟气:
主反应:
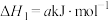
副反应: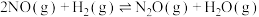

①已知NO也能与 反应生成
反应生成 ,写出该反应的热化学方程式
,写出该反应的热化学方程式___________ 。
②某温度下 的体积分数对
的体积分数对 还原NO反应的影响如图1所示。当
还原NO反应的影响如图1所示。当 的体积分数大于
的体积分数大于 时,
时, 的体积分数呈下降趋势,原因是
的体积分数呈下降趋势,原因是___________ 。
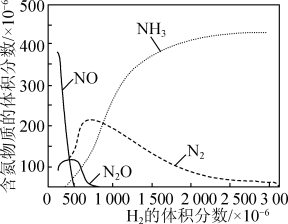
图1
(2)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图2所示,写出电解时铁电极的电极反应式___________ 。随后,铁电极附近有无色气体产生,写出有关反应的离子方程式___________ 。
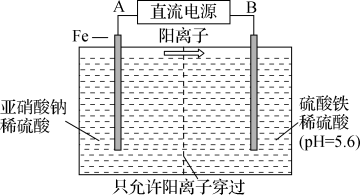
图2
(3)工业上以钛基氧化物涂层材料为阳极,碳纳米管修饰的石墨为阴极,电解硝酸钠和硫酸钠混合溶液,可使 转变为
转变为 ,后续再将
,后续再将 反应除去。已知:电极(电催化剂)所处的环境对其催化活性起重要作用。
反应除去。已知:电极(电催化剂)所处的环境对其催化活性起重要作用。
①若在酸性介质中电解混合溶液,将 转变为
转变为 的电极反应式为
的电极反应式为___________ ;其他条件不变,只改变混合溶液的pH, 去除率如图3所示,pH越小,
去除率如图3所示,pH越小, 去除率上升可能原因是
去除率上升可能原因是___________ 。
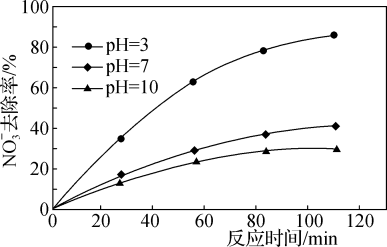
图3
②其他条件不变,只向混合溶液中投入一定量 ,后续去除
,后续去除 的效果明显提高,溶液中氮元素含量显著降低。可能原因是
的效果明显提高,溶液中氮元素含量显著降低。可能原因是___________ 。
 的废气会引起空气污染,含
的废气会引起空气污染,含 、
、 、
、 的废水会引起水体富营养化,都需要经过处理后才能排放。
的废水会引起水体富营养化,都需要经过处理后才能排放。(1)氢气催化还原含NO烟气:
主反应:

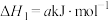
副反应:
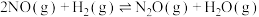

①已知NO也能与
 反应生成
反应生成 ,写出该反应的热化学方程式
,写出该反应的热化学方程式②某温度下
 的体积分数对
的体积分数对 还原NO反应的影响如图1所示。当
还原NO反应的影响如图1所示。当 的体积分数大于
的体积分数大于 时,
时, 的体积分数呈下降趋势,原因是
的体积分数呈下降趋势,原因是
图1
(2)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图2所示,写出电解时铁电极的电极反应式

图2
(3)工业上以钛基氧化物涂层材料为阳极,碳纳米管修饰的石墨为阴极,电解硝酸钠和硫酸钠混合溶液,可使
 转变为
转变为 ,后续再将
,后续再将 反应除去。已知:电极(电催化剂)所处的环境对其催化活性起重要作用。
反应除去。已知:电极(电催化剂)所处的环境对其催化活性起重要作用。①若在酸性介质中电解混合溶液,将
 转变为
转变为 的电极反应式为
的电极反应式为 去除率如图3所示,pH越小,
去除率如图3所示,pH越小, 去除率上升可能原因是
去除率上升可能原因是
图3
②其他条件不变,只向混合溶液中投入一定量
 ,后续去除
,后续去除 的效果明显提高,溶液中氮元素含量显著降低。可能原因是
的效果明显提高,溶液中氮元素含量显著降低。可能原因是
您最近半年使用:0次
2023-07-23更新
|
159次组卷
|
2卷引用:江苏省扬州市高邮市2022-2023学年高二上学期10月月考化学试题
解题方法
7 .  催化加氢合成二甲醚是一种
催化加氢合成二甲醚是一种 转化方法,其过程中主要发生下列反应:
转化方法,其过程中主要发生下列反应:
反应Ⅰ:
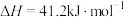
反应Ⅱ:
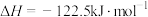
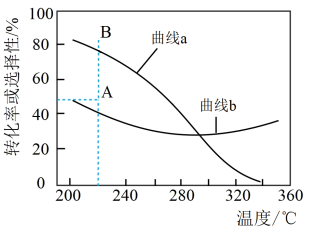
在恒压、 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性 ),下列说法正确的是
),下列说法正确的是
 催化加氢合成二甲醚是一种
催化加氢合成二甲醚是一种 转化方法,其过程中主要发生下列反应:
转化方法,其过程中主要发生下列反应:反应Ⅰ:

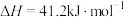
反应Ⅱ:

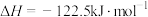
在恒压、
 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性 ),下列说法正确的是
),下列说法正确的是
A.曲线a代表 平衡转化率 平衡转化率 |
B.为提高 选择性需研发高温条件下对反应Ⅱ催化活性更高的催化剂 选择性需研发高温条件下对反应Ⅱ催化活性更高的催化剂 |
| C.200~360℃范围内,体系中主要发生反应Ⅱ |
D.反应一段时间后,在220℃测得 的选择性48%(图中A点),增大压强可能将 的选择性48%(图中A点),增大压强可能将 的选择性提升到B点 的选择性提升到B点 |
您最近半年使用:0次
8 . 下列说法正确的是
A.已知  , ,  ; ; , , |
B.已知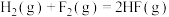 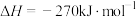 ,则 ,则 氢气与 氢气与 氟气反应生成 氟气反应生成 液态氟化氢时放热大于 液态氟化氢时放热大于 |
C.已知  ,则 ,则 燃烧热为 燃烧热为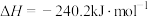 |
D.已知中和热可表示为  ,则 ,则 与 与 完全反应放出的热量为 完全反应放出的热量为 |
您最近半年使用:0次
9 . 传统尿素的合成与核燃料的处理。
(1)传统工业以 与
与 为原料合成尿素的反应在进行时分为如下两步:
为原料合成尿素的反应在进行时分为如下两步:
第一步: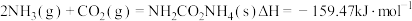
第二步: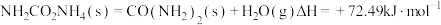
写出以 与
与 为原料合成尿素的热化学方程式
为原料合成尿素的热化学方程式___________ 。
(2)铀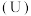 可用作核燃料。核废料中
可用作核燃料。核废料中 价的铀
价的铀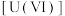 可以通过电化学还原法处理,
可以通过电化学还原法处理,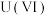 还原为
还原为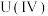 的电化学装置如图所示:
的电化学装置如图所示:
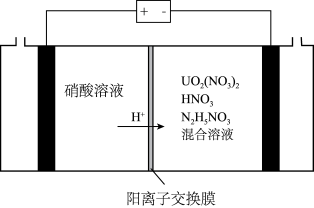
阴极上发生反应: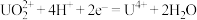 、
、
阴极区溶液中发生反应: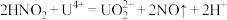 、
、
①反应 中,每生成
中,每生成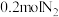 转移电子
转移电子_______  。
。
②阴极区溶液中加入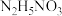 的目的是
的目的是___________ 。
③以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图所示:

i.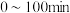 ,电路中每转移
,电路中每转移 ,阴极区
,阴极区 减少
减少___________  。
。
ii.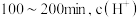 下降速率低于
下降速率低于 前,原因是
前,原因是___________ 。
(1)传统工业以
 与
与 为原料合成尿素的反应在进行时分为如下两步:
为原料合成尿素的反应在进行时分为如下两步:第一步:
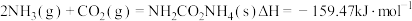
第二步:
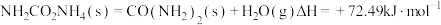
写出以
 与
与 为原料合成尿素的热化学方程式
为原料合成尿素的热化学方程式(2)铀
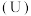 可用作核燃料。核废料中
可用作核燃料。核废料中 价的铀
价的铀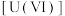 可以通过电化学还原法处理,
可以通过电化学还原法处理,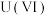 还原为
还原为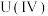 的电化学装置如图所示:
的电化学装置如图所示:
阴极上发生反应:
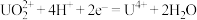 、
、
阴极区溶液中发生反应:
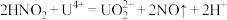 、
、
①反应
 中,每生成
中,每生成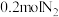 转移电子
转移电子 。
。②阴极区溶液中加入
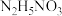 的目的是
的目的是③以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图所示:

i.
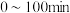 ,电路中每转移
,电路中每转移 ,阴极区
,阴极区 减少
减少 。
。ii.
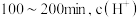 下降速率低于
下降速率低于 前,原因是
前,原因是
您最近半年使用:0次
名校
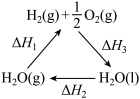
10 . 某科学家利用二氧化铈 在太阳能作用下将
在太阳能作用下将 转变成
转变成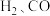 。其过程如下:
。其过程如下:
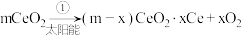
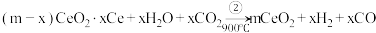
下列说法不正确 的是
 在太阳能作用下将
在太阳能作用下将 转变成
转变成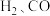 。其过程如下:
。其过程如下: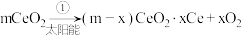
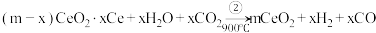
下列说法

A.该过程中 起到了催化作用 起到了催化作用 |
| B.该过程实现了太阳能向化学能的转化 |
C.如图中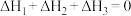 |
D.以 和 和 构成的碱性燃料电池的负极反应式为 构成的碱性燃料电池的负极反应式为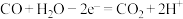 |
您最近半年使用:0次
2023-07-17更新
|
152次组卷
|
2卷引用:江苏省徐州市铜山区2022-2023学年高二上学期11月期中考试(选择考)化学试题



