1 . 固硫技术(通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中)可有效降低燃煤废气中 的含量,同时对产生的废弃物进行回收再利用具有重要的环保意义。
的含量,同时对产生的废弃物进行回收再利用具有重要的环保意义。
Ⅰ.石灰石固硫:固硫过程中涉及的部分反应如下:
①

②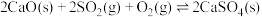

③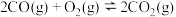

④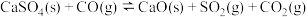

(1)
_______  。
。
(2)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),分析其原因:_______ 。
Ⅱ.石灰石回收:利用 和浓氨水的混合溶液浸取I中固体废渣(主要含
和浓氨水的混合溶液浸取I中固体废渣(主要含 )可回收得到
)可回收得到 ,反应装置如图-1所示。
,反应装置如图-1所示。

(3)写出浸取中发生反应的离子方程式:_______ 。
(4)浸取废渣时,向 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是_______ 。
Ⅲ.石灰乳脱硫:燃煤废气中的 也可用石灰乳吸收,得到的
也可用石灰乳吸收,得到的 浆料可用于制备
浆料可用于制备 溶液。
溶液。
(5)写出实验方案:_______ 。已知: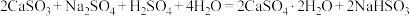 ;
; 难溶于水;室温下,溶液中
难溶于水;室温下,溶液中 的物质的量分数随
的物质的量分数随 的分布如图-2所示。实验中可选用的试剂:
的分布如图-2所示。实验中可选用的试剂: 。
。

 的含量,同时对产生的废弃物进行回收再利用具有重要的环保意义。
的含量,同时对产生的废弃物进行回收再利用具有重要的环保意义。Ⅰ.石灰石固硫:固硫过程中涉及的部分反应如下:
①


②
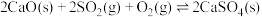

③
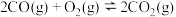

④
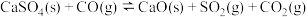

(1)

 。
。(2)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),分析其原因:
Ⅱ.石灰石回收:利用
 和浓氨水的混合溶液浸取I中固体废渣(主要含
和浓氨水的混合溶液浸取I中固体废渣(主要含 )可回收得到
)可回收得到 ,反应装置如图-1所示。
,反应装置如图-1所示。
(3)写出浸取中发生反应的离子方程式:
(4)浸取废渣时,向
 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是Ⅲ.石灰乳脱硫:燃煤废气中的
 也可用石灰乳吸收,得到的
也可用石灰乳吸收,得到的 浆料可用于制备
浆料可用于制备 溶液。
溶液。(5)写出实验方案:
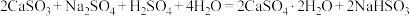 ;
; 难溶于水;室温下,溶液中
难溶于水;室温下,溶液中 的物质的量分数随
的物质的量分数随 的分布如图-2所示。实验中可选用的试剂:
的分布如图-2所示。实验中可选用的试剂: 。
。
您最近一年使用:0次
解题方法
2 . 硫化氢的转化是资源利用和环境保护的重要研究课题。
(1)去除废气中 的相关热化学方程式如下:
的相关热化学方程式如下:


①反应
_______  。
。
②废气中的 和空气(
和空气( 的体积分数约为
的体积分数约为 )的体积比一般控制在0.4,可有效去除废气中的
)的体积比一般控制在0.4,可有效去除废气中的 ,原因是
,原因是_______ 。
(2)甲烷与 重整制氢:
重整制氢: ,为了研究甲烷对
,为了研究甲烷对 制氢的影响,原料初始组成
制氢的影响,原料初始组成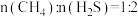 ,保持体系压强为
,保持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图-1所示:
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图-1所示:

①图中曲线a表示物质_______ 。
②某温度下,反应达平衡的标志是_______ (填标号)。
a. b.
b. 的体积分数不再变化
的体积分数不再变化
c. 不再变化 d.混合气体的密度不再改变
不再变化 d.混合气体的密度不再改变
③为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_____ (列举一条)。
(3)太阳能光电催化—化学耦合分解H2S的装置如题图-2所示。

①b极为_______ 极。
②该太阳能光电催化—化学耦合分解H2S的过程可描述为_______ 。
(1)去除废气中
 的相关热化学方程式如下:
的相关热化学方程式如下:

①反应

 。
。②废气中的
 和空气(
和空气( 的体积分数约为
的体积分数约为 )的体积比一般控制在0.4,可有效去除废气中的
)的体积比一般控制在0.4,可有效去除废气中的 ,原因是
,原因是(2)甲烷与
 重整制氢:
重整制氢: ,为了研究甲烷对
,为了研究甲烷对 制氢的影响,原料初始组成
制氢的影响,原料初始组成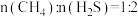 ,保持体系压强为
,保持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图-1所示:
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图-1所示:
①图中曲线a表示物质
②某温度下,反应达平衡的标志是
a.
 b.
b. 的体积分数不再变化
的体积分数不再变化c.
 不再变化 d.混合气体的密度不再改变
不再变化 d.混合气体的密度不再改变③为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(3)太阳能光电催化—化学耦合分解H2S的装置如题图-2所示。

①b极为
②该太阳能光电催化—化学耦合分解H2S的过程可描述为
您最近一年使用:0次
名校
解题方法
3 . 工厂烟气(主要污染物有SO2、NO)直接排放会造成空气污染,需要处理才能排放。
(1)尿素[CO(NH2)2]溶液吸收。
CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2。
若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。
脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为____ 。
(2)Na2SO3溶液吸收。
烟气中的SO2可用Na2SO3溶液吸收。
室温下,吸收过程中,吸收液pH随n(SO ):n(HSO
):n(HSO )变化关系如表:
)变化关系如表:
当吸收液呈中性时,溶液中离子浓度由大到小 的顺序为____ 。
(3)O3氧化。
O3氧化过程中部分反应的能量变化如图1所示。

已知2SO2(g)+O2(g) 2SO3(g) △H=-198kJ·mol-1。
2SO3(g) △H=-198kJ·mol-1。
则反应2O3(g) 3O2(g)的△H=
3O2(g)的△H=____ kJ·mol-1。
(4)NaClO2氧化。
40℃时向一定量NaClO2溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图2所示。烟气中含有少量SO2,能提高NO的脱除率,可能的原因是____ 。

(1)尿素[CO(NH2)2]溶液吸收。
CO(NH2)2溶液脱硫的反应为:SO2+CO(NH2)2+2H2O=(NH4)2SO3+CO2。
若吸收烟气时通入少量ClO2,可同时实现脱硫、脱硝。
脱硝的反应分为两步。
第一步:5NO+2ClO2+H2O=5NO2+2HCl
第二步:NO2和CO(NH2)2反应生成N2、CO2和水。
请写出第二步反应的化学方程式为
(2)Na2SO3溶液吸收。
烟气中的SO2可用Na2SO3溶液吸收。
室温下,吸收过程中,吸收液pH随n(SO
 ):n(HSO
):n(HSO )变化关系如表:
)变化关系如表:n(SO ):n(HSO ):n(HSO ) ) | 99∶1 | 1∶1 | 1∶99 |
| pH | 8.2 | 7.2 | 6.2 |
(3)O3氧化。
O3氧化过程中部分反应的能量变化如图1所示。

已知2SO2(g)+O2(g)
 2SO3(g) △H=-198kJ·mol-1。
2SO3(g) △H=-198kJ·mol-1。则反应2O3(g)
 3O2(g)的△H=
3O2(g)的△H=(4)NaClO2氧化。
40℃时向一定量NaClO2溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图2所示。烟气中含有少量SO2,能提高NO的脱除率,可能的原因是

您最近一年使用:0次
2022-06-29更新
|
234次组卷
|
2卷引用:江苏省江阴市普通高中2021-2022学年高一下学期期末考试化学试题
名校
解题方法
4 . 将 转化为有机燃料是实现碳资源可持续利用的有效途径。
转化为有机燃料是实现碳资源可持续利用的有效途径。
(1)催化加氢制甲醇。向容积为2L的恒容、绝热密闭容器中通入2.0 mol 和3.0 mol
和3.0 mol ,发生反应如下:
,发生反应如下:
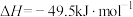
①反应在5min时达平衡,测得此时容器内 与
与 的物质的量之比为
的物质的量之比为 ,则前5min内,该反应的平均反应速率
,则前5min内,该反应的平均反应速率
___________ 。
②下列可用来判断该反应已达到平衡状态的有___________ (填标号)。
A. B.容器中
B.容器中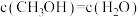
C.混合气体的密度保持不变 D.容器内的温度保持不变
③两分子甲醇可进一步脱水制得二甲醚:
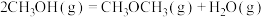
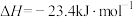
则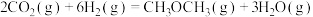 的
的
___________ 。
(2)催化加氢制甲烷。向恒压、密闭容器中通入1mol 和4mol
和4mol ,在催化剂作用下发生如下反应:
,在催化剂作用下发生如下反应:
反应Ⅰ:

反应Ⅱ:
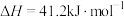
反应Ⅲ:
上述反应达平衡时,容器中 、
、 和CO的物质的量随温度的变化关系如图所示。
和CO的物质的量随温度的变化关系如图所示。
①曲线A表示___________ 的物质的量随温度的变化。
②800℃时曲线B代表物质的物质的量远大于400℃时的物质的量,其原因是___________ 。
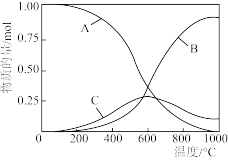
③曲线C代表物质的物质的量随温度的升高,先逐渐增大后逐渐减小。在200-600℃间,曲线C逐渐上升的原因是___________ 。
 转化为有机燃料是实现碳资源可持续利用的有效途径。
转化为有机燃料是实现碳资源可持续利用的有效途径。(1)催化加氢制甲醇。向容积为2L的恒容、绝热密闭容器中通入2.0 mol
 和3.0 mol
和3.0 mol ,发生反应如下:
,发生反应如下:
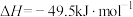
①反应在5min时达平衡,测得此时容器内
 与
与 的物质的量之比为
的物质的量之比为 ,则前5min内,该反应的平均反应速率
,则前5min内,该反应的平均反应速率
②下列可用来判断该反应已达到平衡状态的有
A.
 B.容器中
B.容器中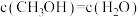
C.混合气体的密度保持不变 D.容器内的温度保持不变
③两分子甲醇可进一步脱水制得二甲醚:
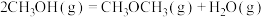
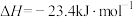
则
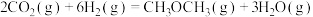 的
的
(2)催化加氢制甲烷。向恒压、密闭容器中通入1mol
 和4mol
和4mol ,在催化剂作用下发生如下反应:
,在催化剂作用下发生如下反应:反应Ⅰ:


反应Ⅱ:

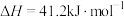
反应Ⅲ:

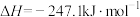
上述反应达平衡时,容器中
 、
、 和CO的物质的量随温度的变化关系如图所示。
和CO的物质的量随温度的变化关系如图所示。①曲线A表示
②800℃时曲线B代表物质的物质的量远大于400℃时的物质的量,其原因是

③曲线C代表物质的物质的量随温度的升高,先逐渐增大后逐渐减小。在200-600℃间,曲线C逐渐上升的原因是
您最近一年使用:0次
2022-06-29更新
|
322次组卷
|
2卷引用:江苏省常州市教育学会2021-2022学年高二下学期期末学业水平监测化学试题
名校
解题方法
5 . 利用 加氢制甲醇等清洁燃料,是实现
加氢制甲醇等清洁燃料,是实现 减排较为可行的方法。一定温度下,
减排较为可行的方法。一定温度下, 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:
反应Ⅰ:

反应Ⅱ:

(1)相同温度下,反应 的
的
_______ 。
(2)在催化、恒压条件下,向密闭容器中投入一定量 和
和 。其他条件相同,升高温度,判断甲醇选择性以及
。其他条件相同,升高温度,判断甲醇选择性以及 的平衡转化率的变化,并说明理由:
的平衡转化率的变化,并说明理由:_______ 。已知: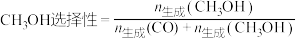 。
。
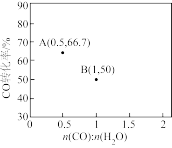
(3)氢气可通过水煤气法获得,原理为 。在进气比
。在进气比 不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系: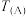
_______ 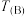 (填“<”、“>”、或“=”),判断的理由是
(填“<”、“>”、或“=”),判断的理由是_______ 。
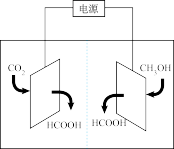
(4)如图装置可将 和甲醇转化为甲酸。阳极的电极反应式为
和甲醇转化为甲酸。阳极的电极反应式为_______ 。
(5) 加氢制甲醇的部分反应机理如图所示。
加氢制甲醇的部分反应机理如图所示。

“ ”表示物质在催化剂表面被吸附,“
”表示物质在催化剂表面被吸附,“ ”表示自由基中未成对电子。已知
”表示自由基中未成对电子。已知 在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
①根据元素的电负性变化规律分析,过程ⅰ中参与反应的显正电性与显负电性氢原子的数目比为_______ ;
②结合化学键的断裂和形成,过程ⅱ可描述为_______ 。
 加氢制甲醇等清洁燃料,是实现
加氢制甲醇等清洁燃料,是实现 减排较为可行的方法。一定温度下,
减排较为可行的方法。一定温度下, 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:反应Ⅰ:


反应Ⅱ:


(1)相同温度下,反应
 的
的
(2)在催化、恒压条件下,向密闭容器中投入一定量
 和
和 。其他条件相同,升高温度,判断甲醇选择性以及
。其他条件相同,升高温度,判断甲醇选择性以及 的平衡转化率的变化,并说明理由:
的平衡转化率的变化,并说明理由: 。
。(3)氢气可通过水煤气法获得,原理为
 。在进气比
。在进气比 不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系: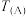
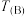 (填“<”、“>”、或“=”),判断的理由是
(填“<”、“>”、或“=”),判断的理由是
(4)如图装置可将
 和甲醇转化为甲酸。阳极的电极反应式为
和甲醇转化为甲酸。阳极的电极反应式为
(5)
 加氢制甲醇的部分反应机理如图所示。
加氢制甲醇的部分反应机理如图所示。
“
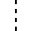 ”表示物质在催化剂表面被吸附,“
”表示物质在催化剂表面被吸附,“ ”表示自由基中未成对电子。已知
”表示自由基中未成对电子。已知 在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。①根据元素的电负性变化规律分析,过程ⅰ中参与反应的显正电性与显负电性氢原子的数目比为
②结合化学键的断裂和形成,过程ⅱ可描述为
您最近一年使用:0次
2022-06-28更新
|
246次组卷
|
2卷引用:江苏省扬州市2021-2022学年高二下学期期末测试化学试题
6 . 为了减少碳排放,可在催化条件下将 和
和 转化为CO和
转化为CO和 ,其主要反应如下为
,其主要反应如下为 ,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
积碳反应:
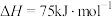
消碳反应:

积碳会影响催化剂的的活性。反应相同时间,测得积碳量与反应温度的关系如图2。

下列说法正确的是
 和
和 转化为CO和
转化为CO和 ,其主要反应如下为
,其主要反应如下为 ,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:积碳反应:

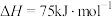
消碳反应:


积碳会影响催化剂的的活性。反应相同时间,测得积碳量与反应温度的关系如图2。

下列说法正确的是
A.消碳反应的 |
B.增大 与 与 的物质的量之比有助于减少积碳 的物质的量之比有助于减少积碳 |
| C.温度高于600℃,积碳反应的速率减慢,积碳量减少 |
D. 和 和 反应的快慢由反应物→过渡态Ⅰ的速率决定 反应的快慢由反应物→过渡态Ⅰ的速率决定 |
您最近一年使用:0次
7 .  催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
CO岐化: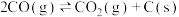

 裂解:
裂解:
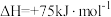
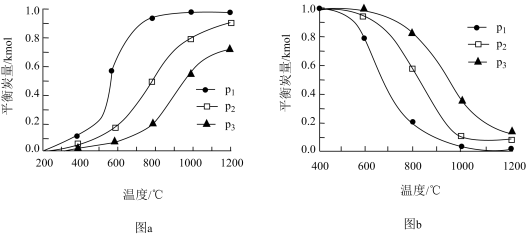
积炭反应中,温度和压强与平衡炭量的关系如下图a所示。
下列说法正确的是
 催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。CO岐化:
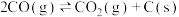

 裂解:
裂解:
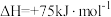
积炭反应中,温度和压强与平衡炭量的关系如下图a所示。

下列说法正确的是
A.重整反应 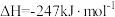 |
B.图中压强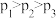 |
C.表示温度和压强对 裂解反应中平衡炭量影响的是图b 裂解反应中平衡炭量影响的是图b |
| D.在重整反应中,低温、高压时会有显著积炭产生,积炭主要由CO岐化反应产生 |
您最近一年使用:0次
解题方法
8 . 工业废水中的六价铬[Cr(VI)]常采用还原沉淀法、离子交换法和微生物法等方法进行处理。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO ΔH1
ΔH1
HCrO ⇌H++CrO
⇌H++CrO ΔH2
ΔH2
2HCrO ⇌
⇌ +H2O ΔH3
+H2O ΔH3
室温下,反应2CrO +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=_______ (用含ΔH1、ΔH2或ΔH3的代数式表示)。
(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力, 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为_______ 。
②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是_______ 。
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是_______ 。
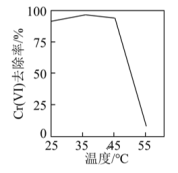
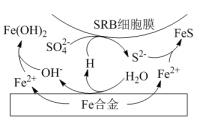
②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,_______ 。
(4)离子交换法:用强碱性离子交换树脂(ROH)与 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:
ROH(s)+HCrO (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)
2ROH(s)+ (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)
其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是_______ 。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO
 ΔH1
ΔH1HCrO
 ⇌H++CrO
⇌H++CrO ΔH2
ΔH22HCrO
 ⇌
⇌ +H2O ΔH3
+H2O ΔH3室温下,反应2CrO
 +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力,
 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,

(4)离子交换法:用强碱性离子交换树脂(ROH)与
 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:ROH(s)+HCrO
 (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)2ROH(s)+
 (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是
您最近一年使用:0次
9 . SO2、NOx是空气的主要污染物,有效去除大气中的SO2、NOx可以保护大气环境。含氮废水氨态氮(以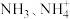 存在)和硝态氨(以
存在)和硝态氨(以 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。
(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:



反应 的∆H=
的∆H=_____ 
(2)已知拆开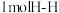 键,
键,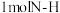 键,
键, 键分别需要的能量是
键分别需要的能量是 、
、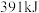 、
、 ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为_______
(3)SO2和NOx是主要大气污染物,利用如图装置可同时吸收SO2和NO。

①a是直流电源的_______ 极
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______
③写出电解池中发生反应的离子方程式:_______
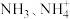 存在)和硝态氨(以
存在)和硝态氨(以 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:



反应
 的∆H=
的∆H=
(2)已知拆开
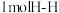 键,
键,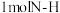 键,
键, 键分别需要的能量是
键分别需要的能量是 、
、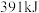 、
、 ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为(3)SO2和NOx是主要大气污染物,利用如图装置可同时吸收SO2和NO。

①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③写出电解池中发生反应的离子方程式:
您最近一年使用:0次
名校
解题方法
10 . 研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
反应III:S(s)+O2(g)=SO2(g) ΔH2=-297kJ/mol
写出反应II的热化学方程式:____ 。
(2)I-可作为水溶液中SO2歧化反应的催化剂(可能的催化过程如下。写出反应ii的离子方程式:i.SO2+4I-+4H+=S↓+2I2+2H2O;ii.____ 。
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。已知:I2易溶解在KI溶液中。
①A是B的对照实验,则a=____ 。
②比较A、B、C实验现象可知:H+____ (填“是”或“不是”)SO2歧化反应的催化剂。
③实验表明,SO2的歧化反应速率D>A,结合i、ii的反应速率解释原因____ 。

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
反应III:S(s)+O2(g)=SO2(g) ΔH2=-297kJ/mol
写出反应II的热化学方程式:
(2)I-可作为水溶液中SO2歧化反应的催化剂(可能的催化过程如下。写出反应ii的离子方程式:i.SO2+4I-+4H+=S↓+2I2+2H2O;ii.
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。已知:I2易溶解在KI溶液中。
| A | B | C | D | |
| 试剂组成 | 0.4mol·L-1KI | amol·L-1KI 0.2mol·L-1H2SO4 | 0.2mol·L-1H2SO4 | 0.2mol·L-1KI 0.0002molI2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
②比较A、B、C实验现象可知:H+
③实验表明,SO2的歧化反应速率D>A,结合i、ii的反应速率解释原因
您最近一年使用:0次



