1 . 甲烷是一种能量密度低、难液化、运输成本较高的能源。将甲烷转化成能量密度较高的液体燃料已成为重要的课题。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1: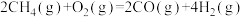

反应2: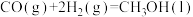
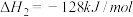
写出甲烷氧化法制甲醇的热化学方程式:______ 。
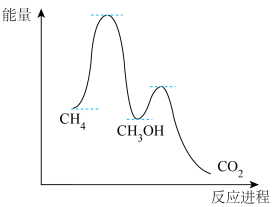
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是______ 。
Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为______ 。

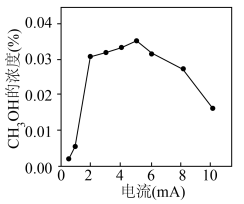
(4)钒(V)物种被认为是形成活性氧物质(如 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是______ 。
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
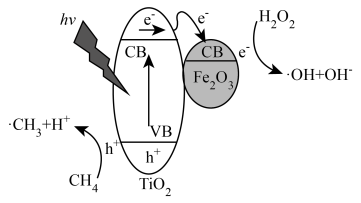
(5)光照时,表面形成的空穴(h+)具有强______ (填“氧化性”或“还原性”)。
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式______ 。
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是______ 。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1:
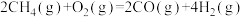

反应2:
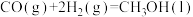
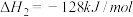
写出甲烷氧化法制甲醇的热化学方程式:
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是

Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为

(4)钒(V)物种被认为是形成活性氧物质(如
 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性
 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
(5)光照时,表面形成的空穴(h+)具有强
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是
您最近一年使用:0次
名校
2 . 苯乙烯是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。
I.直接催化脱氢
(1)已知:①C6H5C2H5(g)+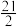 O2(g)=8CO2(g)+5H2O(g) △H1=-4386.9kJ•mol-1
O2(g)=8CO2(g)+5H2O(g) △H1=-4386.9kJ•mol-1
②C6H5CH=CH2(g)+10O2(g)=8CO2(g)+4H2O(g) △H2=-4263.1kJ•mol-1
③H2(g)+ O2(g)=H2O(g) △H3=-241.8kJ•mol-1
O2(g)=H2O(g) △H3=-241.8kJ•mol-1
反应C6H5C2H5(g) C6H5CH=CH2(g)+H2(g)的△H=
C6H5CH=CH2(g)+H2(g)的△H=______ kJ•mol-1。
(2)向密闭容器中充入乙苯蒸气和高温水蒸气,在0.1MPa和催化条件下,不同温度时乙苯的平衡转化率和苯乙烯的平衡选择性如图1所示。
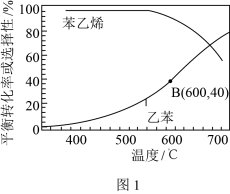
(已知:高温水蒸气不参与乙苯催化脱氢反应;苯乙烯的平衡选择性指除了H2以外的产物中苯乙烯的物质的量分数;乙苯可能会裂解产生积碳覆盖在催化剂表面,使催化剂“中毒”。)
①加入高温水蒸气的作用是______ 。
②实际生产中控制反应温度为600℃的理由是______ 。
II.CO2氧化乙苯脱氢
 (g)+CO2(g)
(g)+CO2(g)
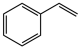 (g)+CO(g)+H2O(g) △H=+158.8kJ•mol-1
(g)+CO(g)+H2O(g) △H=+158.8kJ•mol-1
(3)CO2氧化乙苯脱氢反应的机理如下:
①晶格氧机理
Ar气氛围下,以高价态钒镁氧化物晶体作催化剂进行乙苯脱氢,并将CO2转化为CO,催化循环可表示为图2,图中物质 为
为______ (填“MgVmOn+1”或“MgVmOn”)
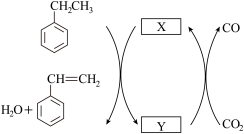
图2
②酸碱位协同催化机理
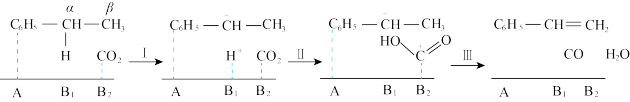
由图可知,酸性位(A)和碱性位(B)都是反应的活性中心,酸性位上发生乙苯的吸附活化;弱碱性位(B1)参与脱去α-H,而强碱性位(B2)活化CO2,被活化的CO2很容易和β-H反应,生成苯乙烯。由于催化剂的碱性不同,在Al2O3上发生的是乙苯直接脱氢,而在Na2O/Al2O3上发生的基本上是CO2耦合乙苯脱氢的原因是______ 。
(4)从资源综合利用角度分析,CO2氧化乙苯脱氢制苯乙烯的优点是______ 。
I.直接催化脱氢
(1)已知:①C6H5C2H5(g)+
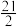 O2(g)=8CO2(g)+5H2O(g) △H1=-4386.9kJ•mol-1
O2(g)=8CO2(g)+5H2O(g) △H1=-4386.9kJ•mol-1②C6H5CH=CH2(g)+10O2(g)=8CO2(g)+4H2O(g) △H2=-4263.1kJ•mol-1
③H2(g)+
 O2(g)=H2O(g) △H3=-241.8kJ•mol-1
O2(g)=H2O(g) △H3=-241.8kJ•mol-1反应C6H5C2H5(g)
 C6H5CH=CH2(g)+H2(g)的△H=
C6H5CH=CH2(g)+H2(g)的△H=(2)向密闭容器中充入乙苯蒸气和高温水蒸气,在0.1MPa和催化条件下,不同温度时乙苯的平衡转化率和苯乙烯的平衡选择性如图1所示。

(已知:高温水蒸气不参与乙苯催化脱氢反应;苯乙烯的平衡选择性指除了H2以外的产物中苯乙烯的物质的量分数;乙苯可能会裂解产生积碳覆盖在催化剂表面,使催化剂“中毒”。)
①加入高温水蒸气的作用是
②实际生产中控制反应温度为600℃的理由是
II.CO2氧化乙苯脱氢
 (g)+CO2(g)
(g)+CO2(g)
 (g)+CO(g)+H2O(g) △H=+158.8kJ•mol-1
(g)+CO(g)+H2O(g) △H=+158.8kJ•mol-1(3)CO2氧化乙苯脱氢反应的机理如下:
①晶格氧机理
Ar气氛围下,以高价态钒镁氧化物晶体作催化剂进行乙苯脱氢,并将CO2转化为CO,催化循环可表示为图2,图中物质
 为
为
图2
②酸碱位协同催化机理
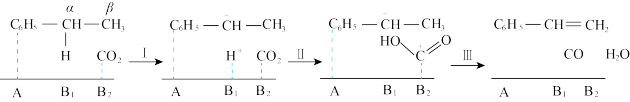
由图可知,酸性位(A)和碱性位(B)都是反应的活性中心,酸性位上发生乙苯的吸附活化;弱碱性位(B1)参与脱去α-H,而强碱性位(B2)活化CO2,被活化的CO2很容易和β-H反应,生成苯乙烯。由于催化剂的碱性不同,在Al2O3上发生的是乙苯直接脱氢,而在Na2O/Al2O3上发生的基本上是CO2耦合乙苯脱氢的原因是
(4)从资源综合利用角度分析,CO2氧化乙苯脱氢制苯乙烯的优点是
您最近一年使用:0次
名校
3 . 含氮化合物( 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。
Ⅰ.苯酚( )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在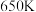 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。
(1)已知



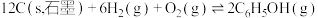
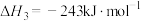
则

___________ 。
Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
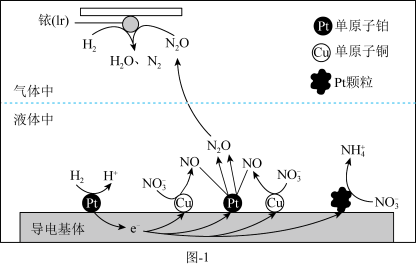
(2) 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,___________ 。
(3)若导电基体上的Pt颗粒增多,造成的后果是___________ 。
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有___________ 。
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(5)该装置可以生成大量氧化性更强的 ,
, 去除
去除 的离子方程式为
的离子方程式为___________ 。
(6)相比于传统的二维电极反应系统,三维电极的优点有___________ 。
 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。Ⅰ.苯酚(
 )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在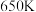 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。(1)已知




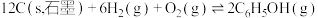
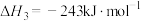
则


Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的
 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2)
 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,(3)若导电基体上的Pt颗粒增多,造成的后果是
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(5)该装置可以生成大量氧化性更强的
 ,
, 去除
去除 的离子方程式为
的离子方程式为(6)相比于传统的二维电极反应系统,三维电极的优点有
您最近一年使用:0次
名校
解题方法
4 . 烟气(主要污染物SO2、NOx)经O3预处理后用碱液吸收,可减少烟气中SO2、NOx的含量。常温下,O3是一种有特殊臭味、稳定性较差的淡蓝色气体。O3氧化烟气中NOx时主要反应的热化学方程式为:
2NO(g) +O2(g)=2NO2(g) H1= a kJ·mol-1
NO(g) +O3(g)=NO2(g) +O2(g) H2= b kJ·mol-1
4NO2(g) +O2(g) =2N2O5(g) H3= c kJ·mol-1
(1)反应6NO2 (g) +O3(g)=3N2O5(g) H=____ kJ·mol-1。
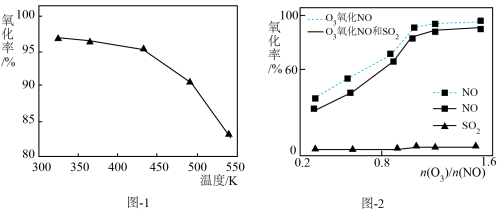
(2)O3氧化NO的氧化率随温度变化情况如图-1。随着温度升高NO的氧化率下降的原因可能是____ 。NO也可被O3氧化为 NO2、NO3,用NaOH溶液吸收若只生成一种盐,该盐的化学式为____ 。
(3)一定条件下,向NOx/O3混合物中加入一定浓度的SO2气体,进行同时脱硫脱硝实验。实验结果如图-2。同时脱硫脱硝时NO的氧化率略低的原因是____ ;由图可知SO2对 NO的氧化率影响很小,下列选项中能解释该结果的是____ (填序号)。
a.O3氧化SO2反应的活化能较大
b.O3与NO反应速率比O3与SO2反应速率快
c.等物质的量的O3与NO反应放出的热量比与SO2反应的多
(4)尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为____ 。也可将该反应设计成碱性燃料电池除去烟气中的氮氧化物,该燃料电池负极的电极反应式是____ 。
2NO(g) +O2(g)=2NO2(g) H1= a kJ·mol-1
NO(g) +O3(g)=NO2(g) +O2(g) H2= b kJ·mol-1
4NO2(g) +O2(g) =2N2O5(g) H3= c kJ·mol-1
(1)反应6NO2 (g) +O3(g)=3N2O5(g) H=
(2)O3氧化NO的氧化率随温度变化情况如图-1。随着温度升高NO的氧化率下降的原因可能是
(3)一定条件下,向NOx/O3混合物中加入一定浓度的SO2气体,进行同时脱硫脱硝实验。实验结果如图-2。同时脱硫脱硝时NO的氧化率略低的原因是
a.O3氧化SO2反应的活化能较大
b.O3与NO反应速率比O3与SO2反应速率快
c.等物质的量的O3与NO反应放出的热量比与SO2反应的多

(4)尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为
您最近一年使用:0次
2018-12-04更新
|
218次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高二上学期10月月考化学试题
5 . 化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cρV总△T计算获得。
(1)盐酸浓度的测定:移取20.00mL特测液,加入指示利,用0.500mol/LNaOH溶液滴定至终点消耗NaOH溶液22.00mL。该盐酸浓度为_____ mol/L。
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,则该过程放出的热量为_____ J(c和ρ分别取4.18J/g·℃和1.0g/mL,忽略水以外各物质吸收的热量,下同)。
(3)借鉴(2)的方法,甲同学测量放热反应Fe(s)+CuSO4 (aq)=FeSO4(aq)+Cu(s)的焓变△H(忽略温度对焓变的影响,下同)。实验结果见如表。
①温度:b_____ c(填“>”“<”或“=”)。
②△H=_____ (选择表中一组数据计算)。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应A:Fe(s)+Fe2(SO4)3(aq)=3FeSO4(aq)的焓变。
查阅资料:配制Fe2(SO4)3溶液时需加入酸。加酸的目的是抑制Fe3+水解。
提出猜想:Fe粉与Fe2(SO4)3溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
验证猜想:用pH试纸测得Fe2(SO4)3溶液的pH不大于1;向少量Fe2(SO4)3溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和_____ (用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为_____ 。
(5)化学能可转化为热能,写出其在生产或生活中的一种应用_____ 。
(1)盐酸浓度的测定:移取20.00mL特测液,加入指示利,用0.500mol/LNaOH溶液滴定至终点消耗NaOH溶液22.00mL。该盐酸浓度为
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,则该过程放出的热量为
(3)借鉴(2)的方法,甲同学测量放热反应Fe(s)+CuSO4 (aq)=FeSO4(aq)+Cu(s)的焓变△H(忽略温度对焓变的影响,下同)。实验结果见如表。
| 反应试剂 | 体系温度/℃ | |||
| 反应前 | 反应后 | |||
| ⅰ | 0.20mol/LCuSO4溶液100mL | 1.20gFe粉 | A | b |
| ⅱ | 0.56gFe粉 | a | C | |
②△H=
(4)乙同学也借鉴(2)的方法,测量反应A:Fe(s)+Fe2(SO4)3(aq)=3FeSO4(aq)的焓变。
查阅资料:配制Fe2(SO4)3溶液时需加入酸。加酸的目的是抑制Fe3+水解。
提出猜想:Fe粉与Fe2(SO4)3溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
验证猜想:用pH试纸测得Fe2(SO4)3溶液的pH不大于1;向少量Fe2(SO4)3溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为
(5)化学能可转化为热能,写出其在生产或生活中的一种应用
您最近一年使用:0次
解题方法
6 . 肼(N2H4)是一种无色油状液体,沸点113.5℃,具有强还原性。能与NaClO剧烈反应生成N2。
(1)N2H4分子中N的化合价为___________
(2)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)、沸点(114℃)分别远高于O2的熔点(-218℃)、沸点(-183℃),原因是___________ 。
(3)由碱性NaClO溶液和尿素 反应可获得
反应可获得 ,反应原理为:
,反应原理为: 。实验中反应物的加料方式为
。实验中反应物的加料方式为___________ (填序号)。
A.将尿素滴加到碱性NaClO溶液中 B.将碱性NaClO溶液滴加到尿素中
(4)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应生成氮气与水蒸气。已知32g液态肼在上述反应中放出64.22kJ的热量,该反应的热化学方程式为___________ 。
(5)肼-空气燃料电池是一种新型环保电池,(用KOH溶液作电解液),该电池负极的电极反应式为___________ 。
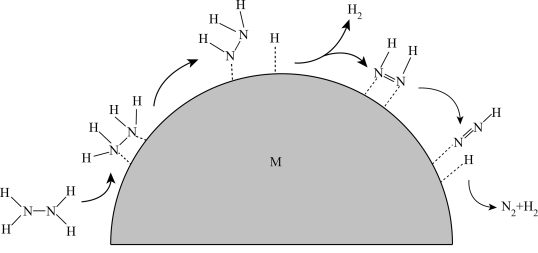
(6)H2是一种理想的绿色清洁能源,N2H4催化分解制氢是能源利用领域的研究热点。在温和条件下,负载型双金属合金M催化N2H4迅速分解,并且制氢选择性可达100%,可能机理如图所示(图中“虚线”表示吸附在催化剂上)。请将N2H4催化分解制氢的机理补充完整:N2H4吸附在(催化剂)M表面,连续断裂___________ 键,形成N2H3、___________ 和N2H等中间产物,直至H原子全部脱去,最终生成___________ 。
(1)N2H4分子中N的化合价为
(2)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)、沸点(114℃)分别远高于O2的熔点(-218℃)、沸点(-183℃),原因是
(3)由碱性NaClO溶液和尿素
 反应可获得
反应可获得 ,反应原理为:
,反应原理为: 。实验中反应物的加料方式为
。实验中反应物的加料方式为A.将尿素滴加到碱性NaClO溶液中 B.将碱性NaClO溶液滴加到尿素中
(4)发射火箭时,肼为燃料,双氧水为氧化剂,两者反应生成氮气与水蒸气。已知32g液态肼在上述反应中放出64.22kJ的热量,该反应的热化学方程式为
(5)肼-空气燃料电池是一种新型环保电池,(用KOH溶液作电解液),该电池负极的电极反应式为
(6)H2是一种理想的绿色清洁能源,N2H4催化分解制氢是能源利用领域的研究热点。在温和条件下,负载型双金属合金M催化N2H4迅速分解,并且制氢选择性可达100%,可能机理如图所示(图中“虚线”表示吸附在催化剂上)。请将N2H4催化分解制氢的机理补充完整:N2H4吸附在(催化剂)M表面,连续断裂

您最近一年使用:0次
7 . 我国提出“碳达峰”目标是在2030年前达到最高值,2060年前达到“碳中和”。因此,二氧化碳的综合利用尤为重要。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚( )也有广泛的应用。
)也有广泛的应用。
反应Ⅰ:
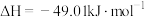
反应Ⅱ:
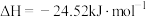
反应Ⅲ:
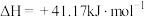
①结合计算分析反应 的自发性:
的自发性:___________ 。
②恒压、投料比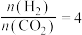 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如下图所示:
消耗总量的百分比)如下图所示:
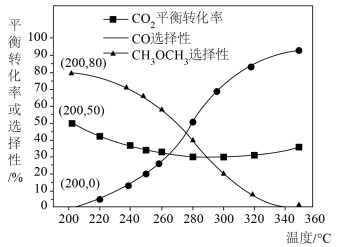
当温度超过 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是___________ 。
③工业实际设计温度一般在 范围内变化,不能过高的原因是
范围内变化,不能过高的原因是___________ 。
(2)研究表明,在电解质水溶液中, 气体可被电化学还原。
气体可被电化学还原。
① 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(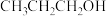 )的电极反应方程式为
)的电极反应方程式为___________ 。
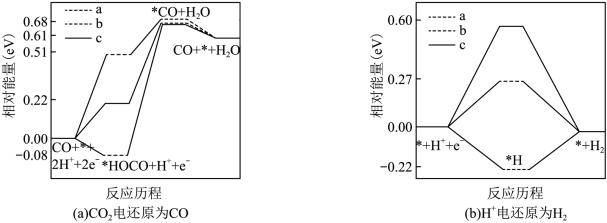
②在电解质水溶液中,三种不同催化剂( 、
、 、
、 )上
)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为___________ (用 、
、 、
、 字母排序)。
字母排序)。
(3) 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( 、
、 表示乙苯分子中
表示乙苯分子中 或
或 原子的位置;
原子的位置; 、
、 为催化剂的活性位点,其中
为催化剂的活性位点,其中 位点带部分正电荷,
位点带部分正电荷,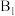 、
、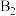 位点带部分负电荷)。
位点带部分负电荷)。

图中所示反应机理中步骤Ⅰ和步骤Ⅱ可描述为___________ 。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(
 )也有广泛的应用。
)也有广泛的应用。反应Ⅰ:

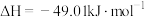
反应Ⅱ:

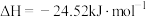
反应Ⅲ:

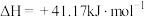
①结合计算分析反应
 的自发性:
的自发性:②恒压、投料比
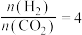 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如下图所示:
消耗总量的百分比)如下图所示:
当温度超过
 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是③工业实际设计温度一般在
 范围内变化,不能过高的原因是
范围内变化,不能过高的原因是(2)研究表明,在电解质水溶液中,
 气体可被电化学还原。
气体可被电化学还原。①
 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(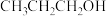 )的电极反应方程式为
)的电极反应方程式为②在电解质水溶液中,三种不同催化剂(
 、
、 、
、 )上
)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为 、
、 、
、 字母排序)。
字母排序)。
(3)
 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( 、
、 表示乙苯分子中
表示乙苯分子中 或
或 原子的位置;
原子的位置; 、
、 为催化剂的活性位点,其中
为催化剂的活性位点,其中 位点带部分正电荷,
位点带部分正电荷,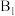 、
、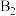 位点带部分负电荷)。
位点带部分负电荷)。
图中所示反应机理中步骤Ⅰ和步骤Ⅱ可描述为
您最近一年使用:0次
名校
8 . Ⅰ.我国要在2030年前实现碳达峰、2060年前实现碳中和的目标, 的捕集与转化是研究的重要课题。
的捕集与转化是研究的重要课题。
(1) 和
和 重整可制合成气
重整可制合成气 和
和 ,其热化学方程式为
,其热化学方程式为
已知下列热化学方程式:
反应1:
反应2:
反应3: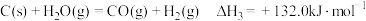
则
___________ 
(2)一种电化学法将 转化为乙烯的原理如图所示,电解所用电极材料均为惰性电极。
转化为乙烯的原理如图所示,电解所用电极材料均为惰性电极。
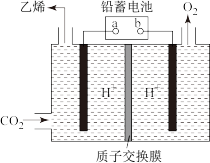
①阴极上的电极反应式为___________ 。
②以铅蓄电池为电源,每生成 乙烯,理论上需消耗铅蓄电池中的硫酸的物质的量为
乙烯,理论上需消耗铅蓄电池中的硫酸的物质的量为___________ 。
Ⅱ.过量含磷物质的排放会致使水体富营养化,因此发展水体除磷技术非常重要。常用的除磷技术有化学沉淀法,吸附法等。
(3)铁炭混合物在水溶液中形成微电池,铁转化为 进一步被氧化为
进一步被氧化为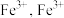 与
与 结合成
结合成 沉淀。铁炭总质量一定,反应时间相同,测得磷去除率随铁炭质量比的变化如图所示。
沉淀。铁炭总质量一定,反应时间相同,测得磷去除率随铁炭质量比的变化如图所示。

①当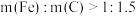 时,随着
时,随着 增加,磷去除率降低,原因是
增加,磷去除率降低,原因是___________ 。
②当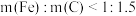 时,随着
时,随着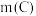 增加,磷去除率也降低。但降低幅度低于
增加,磷去除率也降低。但降低幅度低于 增加时的降低幅度,原因是
增加时的降低幅度,原因是___________ 。
(4)次磷酸根( )具有较强的还原性。利用
)具有较强的还原性。利用 联合除去废水中次磷酸根,转化过程如图所示。
联合除去废水中次磷酸根,转化过程如图所示。

①转化(Ⅰ)除生成 和羟基自由基
和羟基自由基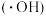 外,还生成一种离子,其化学式为
外,还生成一种离子,其化学式为___________ 。
②利用 联合除去废水中
联合除去废水中 的过程可描述为
的过程可描述为___________ 。
 的捕集与转化是研究的重要课题。
的捕集与转化是研究的重要课题。(1)
 和
和 重整可制合成气
重整可制合成气 和
和 ,其热化学方程式为
,其热化学方程式为
已知下列热化学方程式:
反应1:

反应2:

反应3:
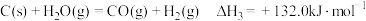
则


(2)一种电化学法将
 转化为乙烯的原理如图所示,电解所用电极材料均为惰性电极。
转化为乙烯的原理如图所示,电解所用电极材料均为惰性电极。
①阴极上的电极反应式为
②以铅蓄电池为电源,每生成
 乙烯,理论上需消耗铅蓄电池中的硫酸的物质的量为
乙烯,理论上需消耗铅蓄电池中的硫酸的物质的量为Ⅱ.过量含磷物质的排放会致使水体富营养化,因此发展水体除磷技术非常重要。常用的除磷技术有化学沉淀法,吸附法等。
(3)铁炭混合物在水溶液中形成微电池,铁转化为
 进一步被氧化为
进一步被氧化为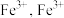 与
与 结合成
结合成 沉淀。铁炭总质量一定,反应时间相同,测得磷去除率随铁炭质量比的变化如图所示。
沉淀。铁炭总质量一定,反应时间相同,测得磷去除率随铁炭质量比的变化如图所示。
①当
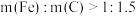 时,随着
时,随着 增加,磷去除率降低,原因是
增加,磷去除率降低,原因是②当
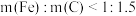 时,随着
时,随着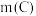 增加,磷去除率也降低。但降低幅度低于
增加,磷去除率也降低。但降低幅度低于 增加时的降低幅度,原因是
增加时的降低幅度,原因是(4)次磷酸根(
 )具有较强的还原性。利用
)具有较强的还原性。利用 联合除去废水中次磷酸根,转化过程如图所示。
联合除去废水中次磷酸根,转化过程如图所示。
①转化(Ⅰ)除生成
 和羟基自由基
和羟基自由基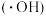 外,还生成一种离子,其化学式为
外,还生成一种离子,其化学式为②利用
 联合除去废水中
联合除去废水中 的过程可描述为
的过程可描述为
您最近一年使用:0次
解题方法
9 . 工业废水和废渣中会产生含硫(-2价)污染物,需经处理后排放。
Ⅰ.含硫废水(硫元素的主要存在形式为 ),需要回收处理并加以利用。
),需要回收处理并加以利用。
(1)用 、
、 处理含硫废水有关反应如下:
处理含硫废水有关反应如下:
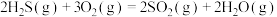





则 热分解反应
热分解反应 的△H=
的△H=_______ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)用 处理含硫废水,硫元素易被氧化为S或
处理含硫废水,硫元素易被氧化为S或 。已知:
。已知: 溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
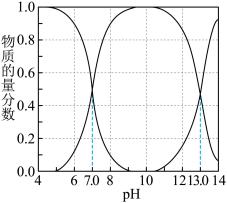
①向含硫废水中加入稀 调节溶液的pH为6,废水中
调节溶液的pH为6,废水中
_______ 。
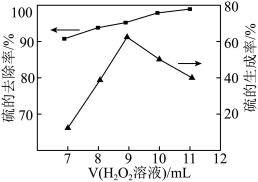
②向含硫废水中加入 溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入
溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入 溶液体积的关系如图所示。当加入
溶液体积的关系如图所示。当加入 溶液体积大于9mL时,硫的生成率随
溶液体积大于9mL时,硫的生成率随 溶液加入而降低,可能的原因是
溶液加入而降低,可能的原因是_______ 。
(3)催化氧化法。 可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
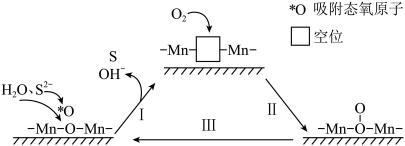
①该反应过程Ⅰ、Ⅱ可描述为_______ 。
②催化剂使用一段时间后催化效率会下降,处理的方法是用氯仿( )浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是
)浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是_______ 。
Ⅱ.含硫废渣(硫元素的主要存在形式为 ),可以回收处理并加以利用。
),可以回收处理并加以利用。
(4)沉积物-微生物燃料电池可以将沉积物中的化学能直接转化为电能,同时加速沉积物中污染物的去除,燃料电池处理含硫废水的工作原理如图所示。
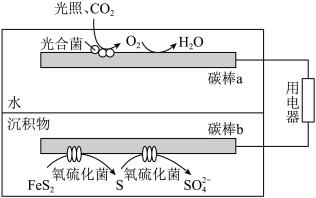
①碳棒b处S生成 的电极反应式为
的电极反应式为_______ 。
②工作一段时间后,电池效率降低的可能原因为_______ 。
Ⅰ.含硫废水(硫元素的主要存在形式为
 ),需要回收处理并加以利用。
),需要回收处理并加以利用。(1)用
 、
、 处理含硫废水有关反应如下:
处理含硫废水有关反应如下: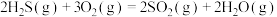





则
 热分解反应
热分解反应 的△H=
的△H= 、
、 、
、 的式子表示)。
的式子表示)。(2)用
 处理含硫废水,硫元素易被氧化为S或
处理含硫废水,硫元素易被氧化为S或 。已知:
。已知: 溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
①向含硫废水中加入稀
 调节溶液的pH为6,废水中
调节溶液的pH为6,废水中
②向含硫废水中加入
 溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入
溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入 溶液体积的关系如图所示。当加入
溶液体积的关系如图所示。当加入 溶液体积大于9mL时,硫的生成率随
溶液体积大于9mL时,硫的生成率随 溶液加入而降低,可能的原因是
溶液加入而降低,可能的原因是
(3)催化氧化法。
 可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
①该反应过程Ⅰ、Ⅱ可描述为
②催化剂使用一段时间后催化效率会下降,处理的方法是用氯仿(
 )浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是
)浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是Ⅱ.含硫废渣(硫元素的主要存在形式为
 ),可以回收处理并加以利用。
),可以回收处理并加以利用。(4)沉积物-微生物燃料电池可以将沉积物中的化学能直接转化为电能,同时加速沉积物中污染物的去除,燃料电池处理含硫废水的工作原理如图所示。

①碳棒b处S生成
 的电极反应式为
的电极反应式为②工作一段时间后,电池效率降低的可能原因为
您最近一年使用:0次
名校
解题方法
10 . 我国要在2030年前实现碳达峰、2060年前实现碳中和的目标, 的捕集与转化是研究的重要课题。
的捕集与转化是研究的重要课题。

(1) 和
和 重整可制合成气CO和
重整可制合成气CO和 ,其热化学反应方程式为
,其热化学反应方程式为
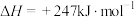 。已知下列热化学反应方程式:
。已知下列热化学反应方程式:
反应1: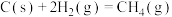

反应2:
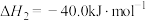
反应3:
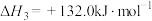
则
_____  。
。
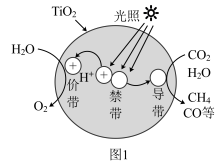
(2)光催化还原法实现 甲烷化可能的反应机理如图1所示。该过程可简述为:光照条件下,催化剂
甲烷化可能的反应机理如图1所示。该过程可简述为:光照条件下,催化剂 表面的价带(VB)中失去的电子(图中电子以
表面的价带(VB)中失去的电子(图中电子以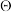 表示)激发至导带(CB)中,价带中形成电子空穴
表示)激发至导带(CB)中,价带中形成电子空穴 (图中
(图中 以
以 表示,
表示, 具有强氧化性),
具有强氧化性), 在VB端,
在VB端, 在CB端发生类似于电解原理的反应。
在CB端发生类似于电解原理的反应。
①在价带的电极反应式为_____ 。
②在催化剂 表面,每生成
表面,每生成 ,则价带产生的空穴
,则价带产生的空穴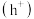 数为
数为_____  。
。
(3)一种电化学法将 转化为乙烯的原理如图2所示。
转化为乙烯的原理如图2所示。
①阴极上的电极反应式为_____ 。
②已知铅蓄电池发生的总反应为: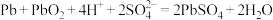 。以铅蓄电池为电源,每生成
。以铅蓄电池为电源,每生成 乙烯,理论上需消耗铅蓄电池中硫酸的物质的量为
乙烯,理论上需消耗铅蓄电池中硫酸的物质的量为_____ 。
(4) 和
和 可合成甲烷,合成过程中发生如下反应:
可合成甲烷,合成过程中发生如下反应:

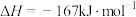


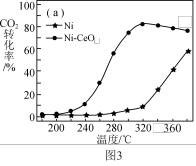
反应的压强和 与
与 气体比例一定,在两种不同催化剂条件下反应相同时间,测得
气体比例一定,在两种不同催化剂条件下反应相同时间,测得 的转化率随温度变化关系如图3所示。高于320℃后,以
的转化率随温度变化关系如图3所示。高于320℃后,以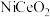 为催化剂,
为催化剂, 转化率略有下降,以Ni为催化剂,
转化率略有下降,以Ni为催化剂, 转化率大幅上升,其原因是
转化率大幅上升,其原因是_____ 。
 的捕集与转化是研究的重要课题。
的捕集与转化是研究的重要课题。


(1)
 和
和 重整可制合成气CO和
重整可制合成气CO和 ,其热化学反应方程式为
,其热化学反应方程式为
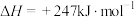 。已知下列热化学反应方程式:
。已知下列热化学反应方程式:反应1:
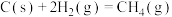

反应2:

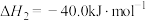
反应3:

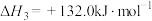
则

 。
。(2)光催化还原法实现
 甲烷化可能的反应机理如图1所示。该过程可简述为:光照条件下,催化剂
甲烷化可能的反应机理如图1所示。该过程可简述为:光照条件下,催化剂 表面的价带(VB)中失去的电子(图中电子以
表面的价带(VB)中失去的电子(图中电子以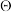 表示)激发至导带(CB)中,价带中形成电子空穴
表示)激发至导带(CB)中,价带中形成电子空穴 (图中
(图中 以
以 表示,
表示, 具有强氧化性),
具有强氧化性), 在VB端,
在VB端, 在CB端发生类似于电解原理的反应。
在CB端发生类似于电解原理的反应。①在价带的电极反应式为
②在催化剂
 表面,每生成
表面,每生成 ,则价带产生的空穴
,则价带产生的空穴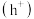 数为
数为 。
。(3)一种电化学法将
 转化为乙烯的原理如图2所示。
转化为乙烯的原理如图2所示。①阴极上的电极反应式为
②已知铅蓄电池发生的总反应为:
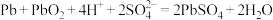 。以铅蓄电池为电源,每生成
。以铅蓄电池为电源,每生成 乙烯,理论上需消耗铅蓄电池中硫酸的物质的量为
乙烯,理论上需消耗铅蓄电池中硫酸的物质的量为(4)
 和
和 可合成甲烷,合成过程中发生如下反应:
可合成甲烷,合成过程中发生如下反应:
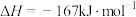


反应的压强和
 与
与 气体比例一定,在两种不同催化剂条件下反应相同时间,测得
气体比例一定,在两种不同催化剂条件下反应相同时间,测得 的转化率随温度变化关系如图3所示。高于320℃后,以
的转化率随温度变化关系如图3所示。高于320℃后,以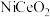 为催化剂,
为催化剂, 转化率略有下降,以Ni为催化剂,
转化率略有下降,以Ni为催化剂, 转化率大幅上升,其原因是
转化率大幅上升,其原因是
您最近一年使用:0次



