21-22高一下·浙江·期中
1 . 我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。碳中和是指CO2的排放总量和减少总量相当。
(1)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
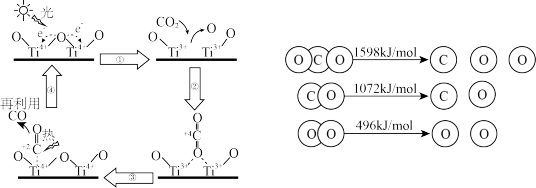
①上述过程中,能量的变化形式是由____ 转化为____ 。
②根据数据计算,将1molCO2分解为CO和O2需____ (填“吸收”或“放出”)____ kJ的能量。
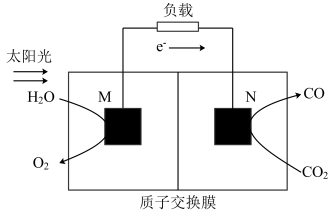
(2)近年科学家提出“绿色自由”构想。利用如图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N极为____ 极,其电极反应方程式为____ 。
(3)在催化剂存在下,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),既能保护环境,又能利用资源。在容积为2L的恒温密闭容器中,充入lmolCO2和3molH2,一定条件下测得CO2和CH3OH(g)的物质的量随时间的变化情况如表。
CH3OH(g)+H2O(g),既能保护环境,又能利用资源。在容积为2L的恒温密闭容器中,充入lmolCO2和3molH2,一定条件下测得CO2和CH3OH(g)的物质的量随时间的变化情况如表。
①下列说法正确的是____ 。
a.反应达到平衡后,反应不再进行
b.使用催化剂是可以增大反应速率,提高生产效率
c.改变条件,CO2可以100%地转化为CH3OH
d.反应达平衡时断裂C-H键的数目与断裂H-H键的数目比为1∶1
e.混合气体的密度和平均相对分子量不再改变,均可以说明反应已达平衡状态
②a=____ ;3~6min内,v(CO2)=____ ;第3min时v正(CH3OH)_____ (填“>”、“<”或“=”)第9min时v逆(CH3OH)。
(1)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。

①上述过程中,能量的变化形式是由
②根据数据计算,将1molCO2分解为CO和O2需
(2)近年科学家提出“绿色自由”构想。利用如图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N极为

(3)在催化剂存在下,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),既能保护环境,又能利用资源。在容积为2L的恒温密闭容器中,充入lmolCO2和3molH2,一定条件下测得CO2和CH3OH(g)的物质的量随时间的变化情况如表。
CH3OH(g)+H2O(g),既能保护环境,又能利用资源。在容积为2L的恒温密闭容器中,充入lmolCO2和3molH2,一定条件下测得CO2和CH3OH(g)的物质的量随时间的变化情况如表。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH)/mol | 0 | 0.50 | 0.65 | 0.75 | 0.75 |
| n(CO2)/mol | 1 | 0.50 | 0.35 | a | 0.25 |
a.反应达到平衡后,反应不再进行
b.使用催化剂是可以增大反应速率,提高生产效率
c.改变条件,CO2可以100%地转化为CH3OH
d.反应达平衡时断裂C-H键的数目与断裂H-H键的数目比为1∶1
e.混合气体的密度和平均相对分子量不再改变,均可以说明反应已达平衡状态
②a=
您最近一年使用:0次
解题方法
2 . 化学反应中的能量变化和化学反应条件的控制与人类的生产、生活密切相关。回答下列问题:
Ⅰ.已知在25℃和101kPa时,断裂1molH-H键吸收的能量为436kJ,断裂1molN-H键吸收的能量为391kJ,断裂1mol 键吸收的能量为945.6kJ。
键吸收的能量为945.6kJ。
(1)根据以上数据判断氨分解反应 是
是_______ (填“吸热”或“放热”)反应。
(2)在25℃时,取1mol 和3mol
和3mol 放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为
放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为_______ kJ。实际生产中,放出或吸收的热量为Q2,则Q1与Q2的大小关系为:Q1_______ Q2 (填“>”“<”或“=”)。
Ⅱ.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇( )微生物燃料电池(如图所示)中,电解质溶液呈酸性。
)微生物燃料电池(如图所示)中,电解质溶液呈酸性。

(3)该电池中,外电路电流的流动方向为_______ (填“从A到B”或“从B到A”)。
(4)B电极附近氧气发生的电极反应为_______ 。
(5)该燃料电池的总反应为_______ 。
Ⅲ.某可逆反应在体积为2L的恒温恒容密闭容器中进行,0~3min各物质的物质的量的变化情况如图所示(A、C均为气体,B为固体)。
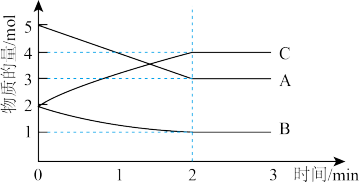
(6)该反应的化学方程式为_______ 。
(7)下列说法错误的是_______(填标号)。
Ⅰ.已知在25℃和101kPa时,断裂1molH-H键吸收的能量为436kJ,断裂1molN-H键吸收的能量为391kJ,断裂1mol
 键吸收的能量为945.6kJ。
键吸收的能量为945.6kJ。(1)根据以上数据判断氨分解反应
 是
是(2)在25℃时,取1mol
 和3mol
和3mol 放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为
放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为Ⅱ.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇(
 )微生物燃料电池(如图所示)中,电解质溶液呈酸性。
)微生物燃料电池(如图所示)中,电解质溶液呈酸性。
(3)该电池中,外电路电流的流动方向为
(4)B电极附近氧气发生的电极反应为
(5)该燃料电池的总反应为
Ⅲ.某可逆反应在体积为2L的恒温恒容密闭容器中进行,0~3min各物质的物质的量的变化情况如图所示(A、C均为气体,B为固体)。

(6)该反应的化学方程式为
(7)下列说法错误的是_______(填标号)。
A.2min内A表示的反应速率为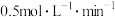 |
| B.增加B的物质的量,可使反应速率加快 |
| C.当容器内混合气体的密度保持不变时,该反应达到平衡状态 |
| D.当容器内压强保持不变时,该反应达到平衡状态 |
您最近一年使用:0次
解题方法
3 . 50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:________ 。烧杯间填满碎泡沫塑料的作用是________ 。大烧杯上如不盖硬纸板,求得的中和热数值________ ,(填“偏大”“偏小”“无影响”下同),用50mL浓硫酸代替盐酸溶液进行上述实验,测得的中和热的数值会________ 。
(2)向盛装稀盐酸的烧杯中加入NaOH溶液的正确操作是________ 。
A.沿玻璃棒缓慢加入 B.一次性迅速加入 C.分三次加入
(3)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________ (填“相等”、“不相等”),所求中和热________ 。(填“相等”、“不相等”)
(4)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是________ (填序号)。
a. Ba(OH)2·8H2O与NH4Cl混合搅拌 b. 高温煅烧石灰石 c. 铝与盐酸反应

(2)向盛装稀盐酸的烧杯中加入NaOH溶液的正确操作是
A.沿玻璃棒缓慢加入 B.一次性迅速加入 C.分三次加入
(3)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(4)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是
a. Ba(OH)2·8H2O与NH4Cl混合搅拌 b. 高温煅烧石灰石 c. 铝与盐酸反应
您最近一年使用:0次
解题方法
4 . Ⅰ.反应Fe+H2SO4=FeSO4+H2↑的能量变化如图所示:
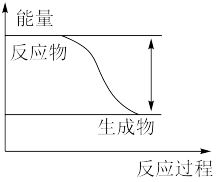
(1)该反应为_______ 反应(填“吸热”或“放热”)。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_______ (填“正”或“负”)极,电极反应式为_______ 。外电路中电流由_______ 流出。(填电极材料名称)。
(3)若要使该反应的反应速率加快,下生成物列措施可行的是_______。
Ⅱ.在一定温度下将2molA气体和4molB气体在2L密闭容器中混合并发生反应:A(g)+2B(g) 3C(g)+D(s)若经2min后测得C的浓度为0.6mol·L-1,则:
3C(g)+D(s)若经2min后测得C的浓度为0.6mol·L-1,则:
(4)用物质A表示的反应速率为_______ 。
(5)2min时物质B的浓度为_______ 。B的转化率为_______ 。
(6)当下列哪些项不再发生变化时,表明上述反应已达到平衡状态_______ 。
A.混合气体的压强
B.混合气体的密度
C.单位时间内消耗1molB同时生成1.5molC
D.混合气体的总物质的量
E.混合气体的平均相对分子质量
F.用A、B、C表示的速率比为1:2:3

(1)该反应为
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
(3)若要使该反应的反应速率加快,下生成物列措施可行的是_______。
| A.改铁片为铁粉 | B.改稀硫酸为98%的硫酸 |
| C.增大压强 | D.滴加几滴CuSO4溶液 |
Ⅱ.在一定温度下将2molA气体和4molB气体在2L密闭容器中混合并发生反应:A(g)+2B(g)
 3C(g)+D(s)若经2min后测得C的浓度为0.6mol·L-1,则:
3C(g)+D(s)若经2min后测得C的浓度为0.6mol·L-1,则:(4)用物质A表示的反应速率为
(5)2min时物质B的浓度为
(6)当下列哪些项不再发生变化时,表明上述反应已达到平衡状态
A.混合气体的压强
B.混合气体的密度
C.单位时间内消耗1molB同时生成1.5molC
D.混合气体的总物质的量
E.混合气体的平均相对分子质量
F.用A、B、C表示的速率比为1:2:3
您最近一年使用:0次
名校
解题方法
5 . 研究化学反应的原理,对掌握物质的应用有重要的意义。
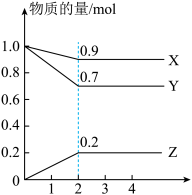
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为___________ 。反应开始至2min,Z的平均反应速率为___________ 。
(2)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
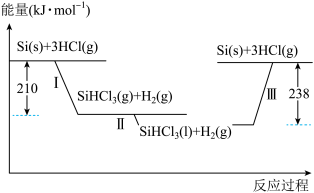
反应I的热化学方程式为___________ 。反应III为___________ (选填“吸热”或“放热”)反应。
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3 +Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为___________ ,正极的电极材料为___________ ,电解质溶液为___________ ,负极的电极反应式为___________ 。
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为

(2)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

反应I的热化学方程式为
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3 +Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为
您最近一年使用:0次
2022-09-25更新
|
153次组卷
|
2卷引用:江苏省盐城市滨海县八滩中学2021-2022学年高一下学期第一次月考化学(选修)试题
解题方法
6 . 1905年哈伯实现了以氨气和氢气为原料合成氨气,生产的氮制造氨肥服务于农业,养活了地球三分之一的人口,哈伯也因此获得了1918年的诺贝尔化学奖。一百多年过去了,对合成氨的研究依然没有止步。
(1)工业合成氨的反应如下: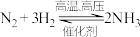 。已知断裂1mol
。已知断裂1mol  中的共价键吸收的能量为946kJ,断裂1mol
中的共价键吸收的能量为946kJ,断裂1mol  中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由
中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由 和
和 生成2mol
生成2mol 的能量变化为
的能量变化为_______ kJ。下图能正确表示该反应中能量变化的是_______ (填“A”或“B”)。
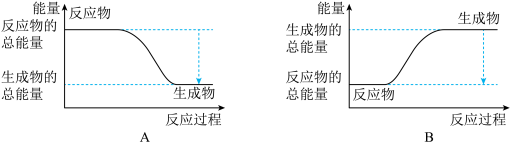
(2)反应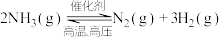 在三种不同条件下进行,
在三种不同条件下进行, 、
、 的起始浓度为0,反应物
的起始浓度为0,反应物 的浓度
的浓度 随时间(min)的变化情况如下表所示。
随时间(min)的变化情况如下表所示。
根据上表数据回答:
①实验I、II中,有一个实验使用了催化剂,它是实验_______ (填序号);在实验Ⅱ中,从0~20min用 表示的速率
表示的速率
_______  。
。
②在不同条件下进行的氨的分解反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是_______ (填字母)。
A. B.
B.
C. D.
D.
③在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_______ (填字母)。
a. 的正反应速率等于逆反应速率 b.混合气体的密度不变
的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.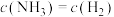
(1)工业合成氨的反应如下:
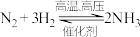 。已知断裂1mol
。已知断裂1mol  中的共价键吸收的能量为946kJ,断裂1mol
中的共价键吸收的能量为946kJ,断裂1mol  中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由
中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由 和
和 生成2mol
生成2mol 的能量变化为
的能量变化为
(2)反应
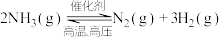 在三种不同条件下进行,
在三种不同条件下进行, 、
、 的起始浓度为0,反应物
的起始浓度为0,反应物 的浓度
的浓度 随时间(min)的变化情况如下表所示。
随时间(min)的变化情况如下表所示。| 序号 | 温度 | 时间 | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| I | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| II | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| III | 500℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上表数据回答:
①实验I、II中,有一个实验使用了催化剂,它是实验
 表示的速率
表示的速率
 。
。②在不同条件下进行的氨的分解反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是
A.
 B.
B.
C.
 D.
D.
③在恒温恒容条件下,判断该反应达到化学平衡状态的标志是
a.
 的正反应速率等于逆反应速率 b.混合气体的密度不变
的正反应速率等于逆反应速率 b.混合气体的密度不变c.混合气体的压强不变 d.
您最近一年使用:0次
名校
解题方法
7 . Ⅰ、反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:

(1)该反应为_______ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是_______ (填字母)。
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_______ (填“正”或“负”)极。铜片上产生的现象为_______ ,该极上发生的电极反应为_______ ,外电路中电子由_______ (填“正”或“负”,下同)极向_______ 极移动。
Ⅱ、汽车尾气中CO、NO2在一定条件下可发生反应4CO(g)+2NO2(g) 4CO2(g)+N2(g),一定温度下,向容积固定的2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
4CO2(g)+N2(g),一定温度下,向容积固定的2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。

(4)0~10 min内该反应的平均速率v(CO)=_______ 。
(5)恒温恒容条件下,不能说明该反应已经达到平衡状态的是_______ (填字母)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变

(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
Ⅱ、汽车尾气中CO、NO2在一定条件下可发生反应4CO(g)+2NO2(g)
 4CO2(g)+N2(g),一定温度下,向容积固定的2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
4CO2(g)+N2(g),一定温度下,向容积固定的2 L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
(4)0~10 min内该反应的平均速率v(CO)=
(5)恒温恒容条件下,不能说明该反应已经达到平衡状态的是
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
您最近一年使用:0次
名校
解题方法
8 . 化学反应中不仅有物质变化而且伴随着能量变化。
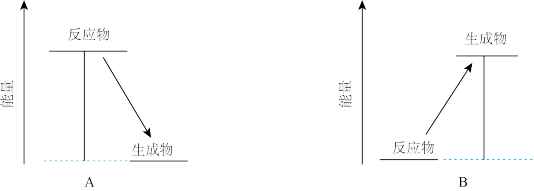
(1)图中,表示放热反应能量变化的是_______ (填字母)。
(2)从微观角度分析化学反应中能量变化的原因:
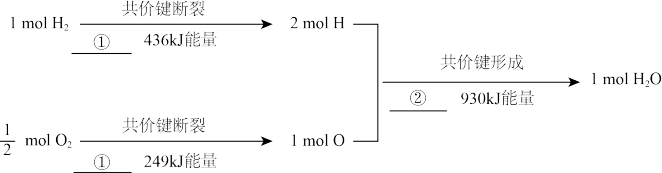
图①过程_______ (填“吸收”或“释放”)热量。氢气与氧气反应生成1mol水蒸气时,释放_______ kJ能量。
(3)原电池是一种可将化学能直接转化为电能的装置。如图所示的原电池装置中,锌片发生_______ (填“氧化”或“还原”)反应,电极反应式_______ ;铜片上能够观察到的现象是_______ ;电子流向_______ (填“锌片-导线-铜片”或“铜片-导线-锌片”)。
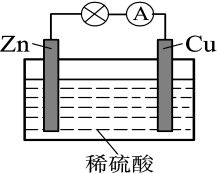
(1)图中,表示放热反应能量变化的是

(2)从微观角度分析化学反应中能量变化的原因:

图①过程
(3)原电池是一种可将化学能直接转化为电能的装置。如图所示的原电池装置中,锌片发生
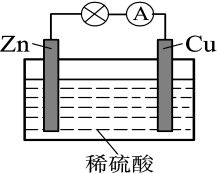
您最近一年使用:0次
2022-08-25更新
|
235次组卷
|
2卷引用:北京市顺义区杨镇第一中学2021-2022学年高一下学期期中考试化学试题
9 . 如图是某同学设计的放热反应的观察装置,其实验操作是:①按图所示将实验装置连接好;②在U形管内加入少量红墨水,打开T形管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹;③在中间的试管里盛1g氧化钙,当滴入2mL左右的蒸馏水后,即可观察。试回答:

(1)实验中观察到的现象是____ 。
(2)该实验之前必须进行的一步操作是____ 。
(3)实验中发生反应的化学方程式为_____ 。
(4)说明反应物CaO与H2O的总能量_____ 生成物Ca(OH)2的能量(填“>”或“<”或“=”)。

(1)实验中观察到的现象是
(2)该实验之前必须进行的一步操作是
(3)实验中发生反应的化学方程式为
(4)说明反应物CaO与H2O的总能量
您最近一年使用:0次
名校
解题方法
10 . 如下图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质,B与水反应生成C.回答下列问题:
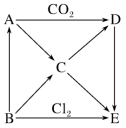
(1)写出物质的化学式:A_______ ,D_______ 。
(2)写出B→C反应的离子方程式:_______ ,该反应热效应△H_______ 0(填“>”、“<”或“=”)。
(3)向C中滴加FeCl2溶液反应一段时间后现象是_______ ,产生这种颜色变化的原因是_______ (用化学方程式解释)。

(1)写出物质的化学式:A
(2)写出B→C反应的离子方程式:
(3)向C中滴加FeCl2溶液反应一段时间后现象是
您最近一年使用:0次



