解题方法
1 . 为消除煤烟气中的 ,研究者提出了多种方法。
,研究者提出了多种方法。
(1)向燃煤中加入适量石灰石( ),高温时将
),高温时将 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(2)以 溶液作为吸收剂,一定条件下将
溶液作为吸收剂,一定条件下将 转化为
转化为 的反应为放热反应。在图中画出该反应过程的能量变化
的反应为放热反应。在图中画出该反应过程的能量变化______ 。

(3)用 溶液吸收烟气中的
溶液吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品,其流程如下。
)粗品,其流程如下。

① 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是_______ 。
②设计实验证明亚硫酸钠粗品中含有
_______ 。
 ,研究者提出了多种方法。
,研究者提出了多种方法。(1)向燃煤中加入适量石灰石(
 ),高温时将
),高温时将 转化为
转化为 的化学方程式是
的化学方程式是(2)以
 溶液作为吸收剂,一定条件下将
溶液作为吸收剂,一定条件下将 转化为
转化为 的反应为放热反应。在图中画出该反应过程的能量变化
的反应为放热反应。在图中画出该反应过程的能量变化
(3)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品,其流程如下。
)粗品,其流程如下。
①
 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是②设计实验证明亚硫酸钠粗品中含有

您最近一年使用:0次
名校
2 . 完成下列问题
(1)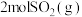 被氧化为
被氧化为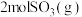 时放出热量198kJ,反应
时放出热量198kJ,反应 的能量变化如图。
的能量变化如图。

①图中A点表示___________ ,E的大小对该反应的热量变化___________ (填“有”或“无”)影响。
②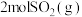 和
和 充分反应放出的热量
充分反应放出的热量___________ 198kJ(填“>”、“<”或“=”)。
(2)一定温度下,在体积为2L的密闭容器中,充入 和
和 发生如下反应:
发生如下反应: 。测定得
。测定得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
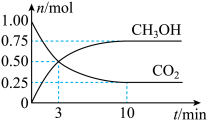
①从反应开始到平衡, 的平均反应速率
的平均反应速率
___________ 。
②达到平衡时, 的转化率为
的转化率为___________ 。(用百分数表示)
③下列措施不能提高化学反应速率的是___________ 。
A.升高温度
B.加入适当催化剂
C.缩小体积,增大压强
D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是___________ 。
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C. 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变
D.反应中 与
与 的物质的量之比为
的物质的量之比为
E.单位时间内每消耗 同时生成
同时生成
(3)如图所示,左侧石墨上通入 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为KOH溶液。完成下列问题:
,电解质溶液为KOH溶液。完成下列问题:
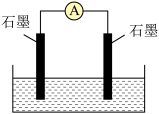
① 属于
属于___________ 化合物(填“离子”或“共价”),KOH中的化学键类型有___________ 。
②放电时 向
向___________ (填“正”或“负”)极移动。负极反应式为___________ 。
③当外电路通过电子的物质的量为7mol时,正极通入的 在标准状况下的体积为
在标准状况下的体积为___________ (假设能量全部转化为电能)。
(1)
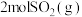 被氧化为
被氧化为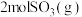 时放出热量198kJ,反应
时放出热量198kJ,反应 的能量变化如图。
的能量变化如图。
①图中A点表示
②
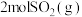 和
和 充分反应放出的热量
充分反应放出的热量(2)一定温度下,在体积为2L的密闭容器中,充入
 和
和 发生如下反应:
发生如下反应: 。测定得
。测定得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
①从反应开始到平衡,
 的平均反应速率
的平均反应速率
②达到平衡时,
 的转化率为
的转化率为③下列措施不能提高化学反应速率的是
A.升高温度
B.加入适当催化剂
C.缩小体积,增大压强
D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C.
 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变D.反应中
 与
与 的物质的量之比为
的物质的量之比为
E.单位时间内每消耗
 同时生成
同时生成
(3)如图所示,左侧石墨上通入
 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为KOH溶液。完成下列问题:
,电解质溶液为KOH溶液。完成下列问题:
①
 属于
属于②放电时
 向
向③当外电路通过电子的物质的量为7mol时,正极通入的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2023-04-29更新
|
478次组卷
|
2卷引用:福建省厦门第一中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 按要求回答下列问题:
(1)下列变化中属于吸热反应的是_______ 。
①铝片与稀盐酸的反应
② 与盐酸的反应
与盐酸的反应
③甲烷在氧气中的燃烧反应
④ 晶体与
晶体与 晶体的反应
晶体的反应
(2)反应 在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是_______ 。
①增加 的量
的量
②将容器的容积缩小一半
③保持容积不变,充入 使体系压强增大
使体系压强增大
④保持压强不变,充入 使容器容积变大
使容器容积变大
(3)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:
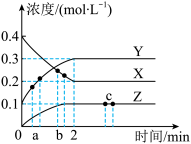
请回答下列问题;
①该反应的化学方程式为_______ ,0~2min内的反应速率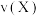
_______ 。
②下列事实能表明300℃时该反应处于平衡状态的是_______ (填序号)。
A.容器内气体压强保持不变 B.生成Y、Z的速率之比为2:1
C. 混合气体的密度保持不变 D.
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应
②
 与盐酸的反应
与盐酸的反应③甲烷在氧气中的燃烧反应
④
 晶体与
晶体与 晶体的反应
晶体的反应(2)反应
 在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加
 的量
的量②将容器的容积缩小一半
③保持容积不变,充入
 使体系压强增大
使体系压强增大④保持压强不变,充入
 使容器容积变大
使容器容积变大(3)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:

请回答下列问题;
①该反应的化学方程式为
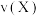
②下列事实能表明300℃时该反应处于平衡状态的是
A.容器内气体压强保持不变 B.生成Y、Z的速率之比为2:1
C. 混合气体的密度保持不变 D.

您最近一年使用:0次
4 . 在人类生产、生活对能量的需求日益增长的今天,研究化学反应及其能量变化和反应速率,合理利用常规能源和开发新能源具有十分重要的意义。能源是人类赖以生存和发展不可缺少的因素。请回答下列问题:
(1)分析如图的能量变化,则 为
为___________ (填“吸热”或“放热”)反应。下列化学反应的能量变化与 的能量变化相同的是
的能量变化相同的是___________ (填标号)。
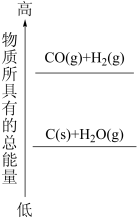
A.稀硫酸与 溶液的反应 B.点燃的镁条在氮气中继续燃烧
溶液的反应 B.点燃的镁条在氮气中继续燃烧
C.灼热的炭与二氧化碳的反应 D. 与
与 的反应
的反应
(2)断裂 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则生成
,则生成 放出的热量为
放出的热量为___________  。
。
(3)如如图是某同学设计的一个简易原电池装置。请回答下列问题。
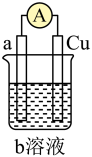
①若a电极材料为碳、b溶液为 溶液,则正极的电极反应式为
溶液,则正极的电极反应式为___________ ,当有1.6g负极材料溶解时,转移的电子个数为___________ 。
②若a电极材料为铁,b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为___________ →___________ (填电极材料,下同),溶液中的 向
向___________ 极移动。
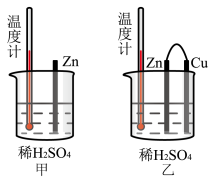
(4)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关实验现象,下列说法正确的是___________(填字母)。
(5)向某体积固定的密闭容器中加入 、
、 和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
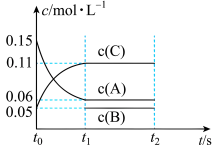
①若 ,则
,则 内反应速率
内反应速率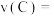
___________ ;
②写出反应的化学方程式:___________ 。
(1)分析如图的能量变化,则
 为
为 的能量变化相同的是
的能量变化相同的是
A.稀硫酸与
 溶液的反应 B.点燃的镁条在氮气中继续燃烧
溶液的反应 B.点燃的镁条在氮气中继续燃烧C.灼热的炭与二氧化碳的反应 D.
 与
与 的反应
的反应(2)断裂
 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则生成
,则生成 放出的热量为
放出的热量为 。
。(3)如如图是某同学设计的一个简易原电池装置。请回答下列问题。

①若a电极材料为碳、b溶液为
 溶液,则正极的电极反应式为
溶液,则正极的电极反应式为②若a电极材料为铁,b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为
 向
向(4)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关实验现象,下列说法正确的是___________(填字母)。

| A.图甲和图乙的气泡均产生于锌棒表面 | B.图乙中产生气体的速率比图甲快 |
| C.图甲中温度计的示数高于图乙的示数 | D.图甲和图乙中温度计的示数相等,且均高于室温 |
 、
、 和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①若
 ,则
,则 内反应速率
内反应速率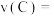
②写出反应的化学方程式:
您最近一年使用:0次
解题方法
5 . 研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
(1)反应的能量变化如图1所示。

①该反应为_______ (填“吸热”或“放热”)反应。
②图2的3个装置中,可以用来证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ (填标号)。

(2)现有纯铁片、纯铜片、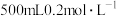 的硫酸溶液,导线和
的硫酸溶液,导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。

①若a,b极不用导线相连,则b极材料为_______ (填“纯铁片”或“纯铜片”)。
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电流从_______ (填“a”或“b”)电极流出;此时b极的电极反应式为_______ 。
③根据上述实验所得结论为_______ 。
(1)反应的能量变化如图1所示。

①该反应为
②图2的3个装置中,可以用来证明“铁与稀硫酸反应是吸热反应还是放热反应”的是

(2)现有纯铁片、纯铜片、
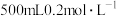 的硫酸溶液,导线和
的硫酸溶液,导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。
①若a,b极不用导线相连,则b极材料为
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电流从
③根据上述实验所得结论为
您最近一年使用:0次
解题方法
6 . Ⅰ.CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+ O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是_____ (填字母)。

a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol•L-1,4min内平均反应速率v(H2)=_____ ,则CH3OH的转化率为______ 。
(3)已知断开1molH-H键吸收的能量为436kJ,形成1molH-N键放出的能量为391kJ,根据化学方程式N2+3H2=2NH3,反应完1molN2放出的能量为92.4kJ,则断开1molN≡N键需吸收的能量是_____ kJ。
Ⅱ.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
(4)x=______ 。
(5)A在5min末的浓度是______ 。
(6)此时容器内的压强与开始时之比为______ 。
(1)已知CH3OH(g)+
 O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol•L-1,4min内平均反应速率v(H2)=
(3)已知断开1molH-H键吸收的能量为436kJ,形成1molH-N键放出的能量为391kJ,根据化学方程式N2+3H2=2NH3,反应完1molN2放出的能量为92.4kJ,则断开1molN≡N键需吸收的能量是
Ⅱ.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。(4)x=
(5)A在5min末的浓度是
(6)此时容器内的压强与开始时之比为
您最近一年使用:0次
名校
7 . 为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置。
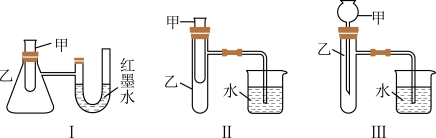
回答下列问题:
(1)上述三套装置中,不能证明“铜与浓硝酸的反应是吸热反应还是放热反应”的是装置______ 。
(2)某同学选用装置I进行实验(实验前U形管里液面相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是________________________ ,说明该反应属于______ (填“吸热”或“放热”)反应。
(3)为探究固体M投入水中的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是_________________ 。
②若观察到烧杯里导管口不产生气泡,但导管内形成一段水柱,则M可能是______ 。
(4)至少有两种实验方法能验证超氧化钾与水的反应( );是放热反应还是吸热反应。
);是放热反应还是吸热反应。
方法①:选择上述装置______ (填“I”“Ⅱ”或“Ⅲ”)进行实验。
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是______ (填“吸热”或“放热”)反应。

回答下列问题:
(1)上述三套装置中,不能证明“铜与浓硝酸的反应是吸热反应还是放热反应”的是装置
(2)某同学选用装置I进行实验(实验前U形管里液面相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是
(3)为探究固体M投入水中的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里导管口不产生气泡,但导管内形成一段水柱,则M可能是
(4)至少有两种实验方法能验证超氧化钾与水的反应(
 );是放热反应还是吸热反应。
);是放热反应还是吸热反应。方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是
您最近一年使用:0次
名校
解题方法
8 . 化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图所示实验,以验证此结论。
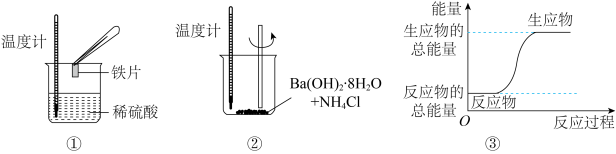
请回答下列问题:
(1)将①中涉及的反应设计成如图所示的原电池,则溶液中的SO 移向
移向_____ (填“正”或“负”)极,电极材料X不能是_____ (填序号)。

A.Cu B.Zn C.Pb D.石墨
(2)进行实验②时,温度计中水银液面变化_____ (填“升高”或“降低”)。
(3)下列化学反应中的能量变化关系与③相符合的是_____ (填序)。
(4)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:

请回答下列问题:
①该反应的化学方程式为_____ 。
②下列事实能表明300℃时该反应处于平衡状态的是_____ (填序号)。
A.v(X):v(Y):v(Z)=2:2:1 B.X(g)的物质的量浓度不变
C.混合气体的质量不变 D.混合气体的密度不变

请回答下列问题:
(1)将①中涉及的反应设计成如图所示的原电池,则溶液中的SO
 移向
移向
A.Cu B.Zn C.Pb D.石墨
(2)进行实验②时,温度计中水银液面变化
(3)下列化学反应中的能量变化关系与③相符合的是
| A.生石灰溶于水 | B.盐酸与碳酸氢钠反应 |
| C.甲烷在空气中燃烧 | D.灼热的木炭与CO2反应 |

请回答下列问题:
①该反应的化学方程式为
②下列事实能表明300℃时该反应处于平衡状态的是
A.v(X):v(Y):v(Z)=2:2:1 B.X(g)的物质的量浓度不变
C.混合气体的质量不变 D.混合气体的密度不变
您最近一年使用:0次
名校
解题方法
9 . 化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)下列变化过程,属于放热反应的是_______ (填写序号)。
①浓H2SO4稀释 ②酸碱中和反应 ③食物因氧化而腐败
④固体NaOH溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原CO2
(2)标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,写出表示甲烷燃烧的热化学方程式_______ 。
(3)已知:C(石墨,s)+ O2(g)=CO2(g) ΔH1=-a kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH2=-b kJ·mol-1
O2(g)=H2O(l) ΔH2=-b kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH3=-c kJ·mol-1
写出C(石墨,s)与H2(g)反应生成CH4(g)的热化学方程式_______ 。
(4)某化学兴趣小组利用如图装置进行中和反应反应热的测定实验。
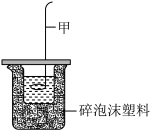
I.实验步骤:
①量取50mL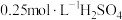 溶液,倒入小烧杯中,测量温度;
溶液,倒入小烧杯中,测量温度;
②量取50mL NaOH溶液,测量温度;
NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,测量混合液的最高温度。
II.实验数据如下:
请回答下列问题:
①仪器甲的名称为_______ ,进行该实验还缺少的仪器为_______ (填仪器名称)。仪器甲不能用铁制材料的原因是_______ 。
②设实验所用的酸、碱溶液的密度均为 ,且酸、碱中和后的溶液的比热容
,且酸、碱中和后的溶液的比热容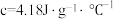 。计算该实验中生成 1mol 水时的反应热
。计算该实验中生成 1mol 水时的反应热
_______  (保留一位小数)
(保留一位小数)
③若改用60mL0.50mol•L-1盐酸与60mL0.55mol•L-1NaOH溶液进行反应,与(1)中实验相比,所放出的热量_______ (填写“相等”或“不相等”);若用50mL0.50mol•L-1CH3COOH溶液代替盐酸进行(1)中实验,测得反应前后温度的变化值_______ (填写“偏大”、“偏小”或“不变”)。
(1)下列变化过程,属于放热反应的是
①浓H2SO4稀释 ②酸碱中和反应 ③食物因氧化而腐败
④固体NaOH溶于水 ⑤液态水变成水蒸气 ⑥碳在高温条件下还原CO2
(2)标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,写出表示甲烷燃烧的热化学方程式
(3)已知:C(石墨,s)+ O2(g)=CO2(g) ΔH1=-a kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH2=-b kJ·mol-1
O2(g)=H2O(l) ΔH2=-b kJ·mol-1CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH3=-c kJ·mol-1
写出C(石墨,s)与H2(g)反应生成CH4(g)的热化学方程式
(4)某化学兴趣小组利用如图装置进行中和反应反应热的测定实验。

I.实验步骤:
①量取50mL
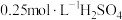 溶液,倒入小烧杯中,测量温度;
溶液,倒入小烧杯中,测量温度;②量取50mL
 NaOH溶液,测量温度;
NaOH溶液,测量温度;③将NaOH溶液倒入小烧杯中,测量混合液的最高温度。
II.实验数据如下:
| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | ||
 溶液 溶液 | NaOH溶液 | 平均值 | ||
| 1 | 25.0 | 25.2 | 28.5 | |
| 2 | 24.9 | 25.1 | 28.4 | |
| 3 | 25.5 | 26.5 | 31.8 | |
①仪器甲的名称为
②设实验所用的酸、碱溶液的密度均为
 ,且酸、碱中和后的溶液的比热容
,且酸、碱中和后的溶液的比热容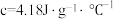 。计算该实验中生成 1mol 水时的反应热
。计算该实验中生成 1mol 水时的反应热
 (保留一位小数)
(保留一位小数)③若改用60mL0.50mol•L-1盐酸与60mL0.55mol•L-1NaOH溶液进行反应,与(1)中实验相比,所放出的热量
您最近一年使用:0次
2023-03-19更新
|
429次组卷
|
2卷引用:湖北省武汉市武钢三中2022-2023学年高一下学期3月月考化学试题
10 . 认识化学反应的本质
化学反应的本质是旧化学键断裂和新化学键形成的过程。在反应中常伴有发光、发热、变色、生成沉淀物等。判断一个反应是否为化学反应的依据是反应是否生成新的物质。认识一个化学反应,不仅要着眼于物质的变化与能量的转化,更要从化学反应的程度与快慢来综合认识一个化学反应。
(1)下列属吸热反应的是___________。
(2)原电池能够实现化学能与电能的转化,下列反应一定不能设计成原电池的是___________。
(3)对于可逆反应 ,决定反应速率的主要因素是___________。
,决定反应速率的主要因素是___________。
(4)下列方法对于可逆反应 的反应速率没有影响的是___________。
的反应速率没有影响的是___________。
(5)一定条件下,在密闭容器中进行合成氨反应: ,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
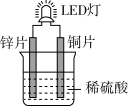
(6)某活动小组设计用如图装置使LED灯发光。下列有关该装置的说法正确的是___________。
(7)恒温恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生下列放热反应:
,一定条件下发生下列放热反应: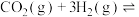
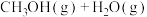 ,测得其中
,测得其中 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
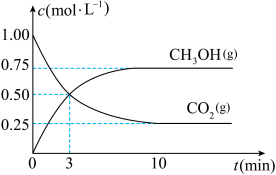
①由图可知,反应从开始至少需要___________ min,反应才达到化学平衡状态。达到化学平衡状态时容器中 的浓度为
的浓度为___________  。
。
②反应达到平衡状态过程中, 的平均反应速率为
的平均反应速率为___________  ,
, 的平均反应速率为
的平均反应速率为___________  。
。
③下列措施能使得该反应化学平衡向逆反应方向移动的是___________ 。
A.升高温度 B.降低温度 C.增大压强 D.分离出产物
化学反应的本质是旧化学键断裂和新化学键形成的过程。在反应中常伴有发光、发热、变色、生成沉淀物等。判断一个反应是否为化学反应的依据是反应是否生成新的物质。认识一个化学反应,不仅要着眼于物质的变化与能量的转化,更要从化学反应的程度与快慢来综合认识一个化学反应。
(1)下列属吸热反应的是___________。
| A.液态水汽化 | B.生石灰与水反应 | C.碳酸钙分解 | D.铝热反应 |
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
 ,决定反应速率的主要因素是___________。
,决定反应速率的主要因素是___________。| A.温度 | B.压强 | C. 和 和 的性质 的性质 | D.催化剂 |
 的反应速率没有影响的是___________。
的反应速率没有影响的是___________。A.加入 | B.压强不变充入He | C.容积不变充入 | D.降低温度 |
 ,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。A. 、 、 、 、 的浓度相等 的浓度相等 |
B. 、 、 、 、 在容器中共存 在容器中共存 |
| C.反应已经达到化学平衡状态 |
D. 、 、 、 、 浓度不再改变 浓度不再改变 |

A.铜片是负极,其附近溶液变蓝,溶液中有 产生 产生 |
| B.如果将锌片换成铁片,电路中的电流方向将改变 |
| C.上述能量转化形式主要是“化学能-电能-光能” |
| D.如果将稀硫酸换成柠檬汁,LED灯将不会发光 |
 和3mol
和3mol ,一定条件下发生下列放热反应:
,一定条件下发生下列放热反应: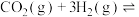
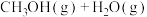 ,测得其中
,测得其中 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
①由图可知,反应从开始至少需要
 的浓度为
的浓度为 。
。②反应达到平衡状态过程中,
 的平均反应速率为
的平均反应速率为 ,
, 的平均反应速率为
的平均反应速率为 。
。③下列措施能使得该反应化学平衡向逆反应方向移动的是
A.升高温度 B.降低温度 C.增大压强 D.分离出产物

您最近一年使用:0次



