1 . 按要求回答下列问题:
(1)下列过程中,既属于氧化还原反应,又属于吸热反应的是_______ 。
①甲烷的燃烧 ②水煤气的制备 ③石灰石受热分解 ④碘升华 ⑤金属的锈蚀
(2)一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应(产物均为气体),反应中各物质物质的量的变化如图所示。______________________ 。
②在0~6 s内,B的化学反应速率为________________ 。
③6s后容器内的压强与开始时压强之比为_____________ 。
(3)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+ 4H2(g)⇌ CH3OCH3(g)+H2O(g),
下列选项不能判断该反应达到平衡状态的依据的________________ 。
①密闭容器中CO的体积分数不变
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤体系内的温度不再变化
⑥单位时间内,断裂4mol H-H键,同时生成2mol H-O键
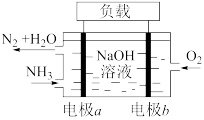
(4)潜艇中使用的液氨液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”),其电极反应为_____________________ 。
(1)下列过程中,既属于氧化还原反应,又属于吸热反应的是
①甲烷的燃烧 ②水煤气的制备 ③石灰石受热分解 ④碘升华 ⑤金属的锈蚀
(2)一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应(产物均为气体),反应中各物质物质的量的变化如图所示。

②在0~6 s内,B的化学反应速率为
③6s后容器内的压强与开始时压强之比为
(3)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+ 4H2(g)⇌ CH3OCH3(g)+H2O(g),
下列选项不能判断该反应达到平衡状态的依据的
①密闭容器中CO的体积分数不变
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤体系内的温度不再变化
⑥单位时间内,断裂4mol H-H键,同时生成2mol H-O键
(4)潜艇中使用的液氨液氧燃料电池工作原理如图所示:
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气
⑤甲烷在氧气中的燃烧反应 ⑥C与H2O(g)高温条件生成水煤气
(2)反应C(s)+H2O(g) CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是 ___________ 。
①增加C的量 ②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
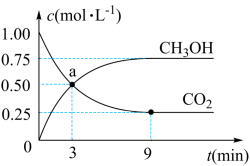
①从3min到9min,v(CO2)=___________ (结果保留两位有效数字);a点时v(正) ___________ v(逆)(填>、<或=,下同);第9分钟时v逆(CH3OH) ___________ 第3分钟时v正(CH3OH)。
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是___________ 。
(4)微生物燃料电池是指在微生物作用下将化学能转化为电能的装置。某微生物燃料电池工作原理如图所示。
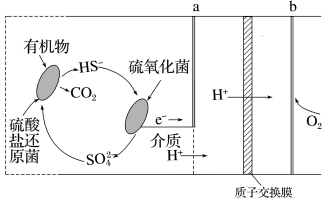
①该微生物燃料电池,负极为___________ (填“a”或“b”)。
②该电池正极电极反应式为___________ 。
③当电路中有0.5mol电子发生转移,则有___________ mol的H+通过质子交换膜。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气
⑤甲烷在氧气中的燃烧反应 ⑥C与H2O(g)高温条件生成水煤气
(2)反应C(s)+H2O(g)
 CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是 ①增加C的量 ②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
①从3min到9min,v(CO2)=
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是
(4)微生物燃料电池是指在微生物作用下将化学能转化为电能的装置。某微生物燃料电池工作原理如图所示。

①该微生物燃料电池,负极为
②该电池正极电极反应式为
③当电路中有0.5mol电子发生转移,则有
您最近一年使用:0次
名校
3 . Ⅰ.CO2催化加氢可以生成低碳有机物,有以下反应:
反应Ⅰ: ;
;
反应Ⅱ:
(1) 分子中化学键类型为
分子中化学键类型为___________ 。  分子的空间填充模型为
分子的空间填充模型为___________ 。
A.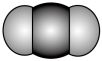 B.
B.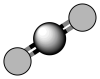
(2)已知反应Ⅰ是放热反应,能正确表示该反应的图示是___________ 。
A.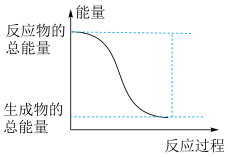 B.
B.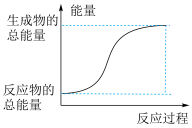
Ⅱ.在 密闭容器中,充入
密闭容器中,充入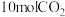 和
和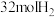 ,在催化剂、200℃条件下,发生反应Ⅰ,部分反应物和产物随时间变化如图所示:
,在催化剂、200℃条件下,发生反应Ⅰ,部分反应物和产物随时间变化如图所示:
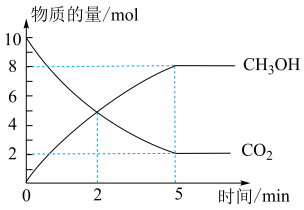
(3) 末,以
末,以  的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________  。
。
(4)下列措施中能增大反应速率且利于平衡正向移动的是___________。
(5)下列情况能说明该反应达到化学平衡状态的是___________ 。
A.单位时间内消耗 ,同时生成
,同时生成
B.密闭容器中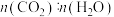 不发生变化
不发生变化
C.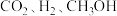 浓度之比为
浓度之比为 的状态
的状态
(6)储氢材料纳米碳管 是空心管状的纳米级晶体,它有力地推动了氢氧燃料电池的开发。关于碳纳米管材料,下列说法错误的是
是空心管状的纳米级晶体,它有力地推动了氢氧燃料电池的开发。关于碳纳米管材料,下列说法错误的是___________ 。
A.与 是同素异形体
是同素异形体
B.表面积大,吸附能力强
C.和氢氧化铁胶体属于同种分散系
(7)某学生用铁棒、铜罐等材料设计了如图简易电池装置。
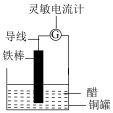
①该装置将___________ 能转化为___________ 能
A.电 B.化学
②___________ 发生氧化反应
A.铁棒 B.铜罐
反应Ⅰ:
 ;
;反应Ⅱ:

(1)
 分子中化学键类型为
分子中化学键类型为 分子的空间填充模型为
分子的空间填充模型为A.
 B.
B.
(2)已知反应Ⅰ是放热反应,能正确表示该反应的图示是
A.
 B.
B.
Ⅱ.在
 密闭容器中,充入
密闭容器中,充入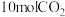 和
和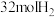 ,在催化剂、200℃条件下,发生反应Ⅰ,部分反应物和产物随时间变化如图所示:
,在催化剂、200℃条件下,发生反应Ⅰ,部分反应物和产物随时间变化如图所示:
(3)
 末,以
末,以  的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 。
。(4)下列措施中能增大反应速率且利于平衡正向移动的是___________。
| A.升高反应温度 | B.将 与反应混合物分离 与反应混合物分离 |
| C.使用高效催化剂 | D.增大 浓度 浓度 |
(5)下列情况能说明该反应达到化学平衡状态的是
A.单位时间内消耗
 ,同时生成
,同时生成
B.密闭容器中
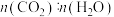 不发生变化
不发生变化C.
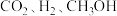 浓度之比为
浓度之比为 的状态
的状态(6)储氢材料纳米碳管
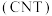 是空心管状的纳米级晶体,它有力地推动了氢氧燃料电池的开发。关于碳纳米管材料,下列说法错误的是
是空心管状的纳米级晶体,它有力地推动了氢氧燃料电池的开发。关于碳纳米管材料,下列说法错误的是A.与
 是同素异形体
是同素异形体B.表面积大,吸附能力强
C.和氢氧化铁胶体属于同种分散系
(7)某学生用铁棒、铜罐等材料设计了如图简易电池装置。

①该装置将
A.电 B.化学
②
A.铁棒 B.铜罐
您最近一年使用:0次
解题方法
4 . 能源是现代社会发展的支柱之一
(1)下列反应中,属于吸热反应的是___________ (填序号)
a.灼热的炭与二氧化碳反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与碳酸氢钠反应
(2)已知稀溶液中, 与
与 溶液恰好完全反应时,放出
溶液恰好完全反应时,放出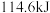 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式___________ 。
(3)实验测得, 甲醇(
甲醇( ,常温下为液态)在氧气中完全燃烧释放出
,常温下为液态)在氧气中完全燃烧释放出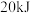 的热量,则表示甲醇燃烧热的热化学方程式为:
的热量,则表示甲醇燃烧热的热化学方程式为:___________ 。
(4)恒温恒容时,能表明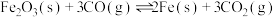 达平衡状态的是
达平衡状态的是___________ (填字母)
A.单位时间内生成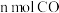 同时消耗
同时消耗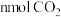
B.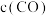 不随时间改变
不随时间改变
C. 的体积分数不变
的体积分数不变
D.Fe的浓度不变,容器内压强不再变化
E.容器内压强不再变化
F.正反应的平衡常数不再变化
G.气体的总质量不再变化
(5)取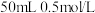 盐酸、
盐酸、 溶液和如图所示装置进行中和热的测定实验。
溶液和如图所示装置进行中和热的测定实验。
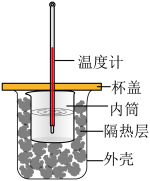
从实验装置上看,图中缺少的一种玻璃仪器是___________ 。
(1)下列反应中,属于吸热反应的是
a.灼热的炭与二氧化碳反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与碳酸氢钠反应
(2)已知稀溶液中,
 与
与 溶液恰好完全反应时,放出
溶液恰好完全反应时,放出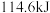 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式(3)实验测得,
 甲醇(
甲醇( ,常温下为液态)在氧气中完全燃烧释放出
,常温下为液态)在氧气中完全燃烧释放出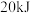 的热量,则表示甲醇燃烧热的热化学方程式为:
的热量,则表示甲醇燃烧热的热化学方程式为:(4)恒温恒容时,能表明
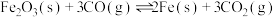 达平衡状态的是
达平衡状态的是A.单位时间内生成
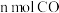 同时消耗
同时消耗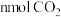
B.
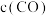 不随时间改变
不随时间改变C.
 的体积分数不变
的体积分数不变D.Fe的浓度不变,容器内压强不再变化
E.容器内压强不再变化
F.正反应的平衡常数不再变化
G.气体的总质量不再变化
(5)取
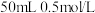 盐酸、
盐酸、 溶液和如图所示装置进行中和热的测定实验。
溶液和如图所示装置进行中和热的测定实验。
从实验装置上看,图中缺少的一种玻璃仪器是
您最近一年使用:0次
名校
5 . Ⅰ.肼(N2H4)是一种重要的化工产品,有广泛用途,常用于火箭推进剂和燃料电池。回答下列问题:
(1)N2H4的电子式为________ 。
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:
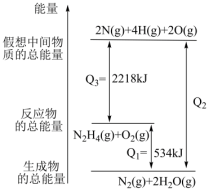
①则该反应为______ (填“吸热反应”或“放热反应”)。
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出_____ kJ能量。
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:
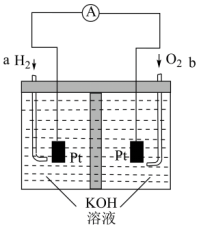
(3)氢燃料电池工作时H2从______ (填“正极”或“负极”)通入。
(4)负极发生的反应方程式为_______ 。
(5)溶液中OH-向_____ 电极(填“a”或“b”)移动。
(6)当有16g气体被还原时,回路中转移的电子数为_____ 。
(1)N2H4的电子式为
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:

①则该反应为
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:

(3)氢燃料电池工作时H2从
(4)负极发生的反应方程式为
(5)溶液中OH-向
(6)当有16g气体被还原时,回路中转移的电子数为
您最近一年使用:0次
2024-01-06更新
|
54次组卷
|
2卷引用:四川省安岳中学2023-2024学年高三10月月考理科综合试题
名校
解题方法
6 . 研究化学反应及其能量变化,对于社会发展、科技进步具有重要的意义。
(1)下列反应属于吸热反应的是___________。
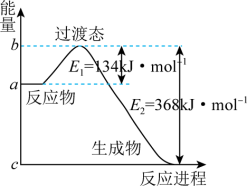
(2)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化的示意图,请写出NO2和CO反应的热化学方程式:_________ 。
(3)一定条件下CO2能与N2发生反应: 。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
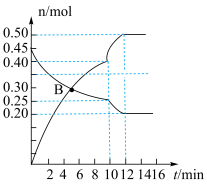
①图中B点v正_______ v逆(填“>”“<”或“=”);B点中CO2的转化率为_________ 。
②反应到10min时向容器中加入催化剂N2的消耗速率迅速增大,请用相关理论解释N2消耗速率增大的原因:_________ 。
③下列情况能说明该反应达到平衡状态的是_________ 。
A.2v(N2)=v(NO) B.混合气体的密度保持不变
C.t时刻,C(s)质量不再增加 D.混合气体的总物质的量不再改变
E.CO2、N2、NO的物质的量之比达到1:1:2
(1)下列反应属于吸热反应的是___________。
| A.碳酸氢钠溶液和盐酸的反应 | B.Ba(OH)2•8H2O与NH4Cl反应 |
| C.铝片与盐酸反应 | D.酒精在氧气中燃烧的反应 |
(2)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化的示意图,请写出NO2和CO反应的热化学方程式:

(3)一定条件下CO2能与N2发生反应:
 。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
。某温度下,若向2L体积恒定的密闭容器中充入等物质的量的N2和CO2,其中N2、NO物质的量随时间变化的曲线如图所示:
①图中B点v正
②反应到10min时向容器中加入催化剂N2的消耗速率迅速增大,请用相关理论解释N2消耗速率增大的原因:
③下列情况能说明该反应达到平衡状态的是
A.2v(N2)=v(NO) B.混合气体的密度保持不变
C.t时刻,C(s)质量不再增加 D.混合气体的总物质的量不再改变
E.CO2、N2、NO的物质的量之比达到1:1:2
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应: 。已知该反应为放热反应,如图能正确表示该反应中能量变化的是
。已知该反应为放热反应,如图能正确表示该反应中能量变化的是______ 。
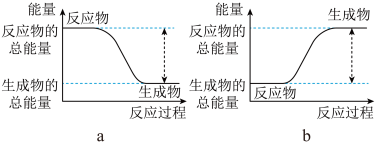
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
反应 的
的
______ kJ/mol。则该反应生成1 mol  可以放出热量是
可以放出热量是______ kJ。
(2) 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生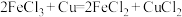 ,若将此反应设计成原电池,则负极所用电极材料为:
,若将此反应设计成原电池,则负极所用电极材料为:______ 。当线路中转移0.2 mol电子时,则被腐蚀铜的质量为:______ g。
(3)铅蓄电池在放电时发生的电池反应式为: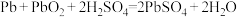 ,负极电极反应式为:
,负极电极反应式为:__________________ 。
(1)从能量的变化和反应的快慢等角度研究反应:
 。已知该反应为放热反应,如图能正确表示该反应中能量变化的是
。已知该反应为放热反应,如图能正确表示该反应中能量变化的是
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 的
的
 可以放出热量是
可以放出热量是(2)
 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生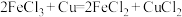 ,若将此反应设计成原电池,则负极所用电极材料为:
,若将此反应设计成原电池,则负极所用电极材料为:(3)铅蓄电池在放电时发生的电池反应式为:
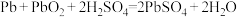 ,负极电极反应式为:
,负极电极反应式为:
您最近一年使用:0次
名校
解题方法
8 . 在日常生活和工农业生产中经常涉及到吸热反应和放热反应,回答下面问题:
(1)下列反应一定属于吸热反应的是_____。
(2)在101kPa时,H2在1.0molO2中完全燃烧,生成2.0mol液态水,放出571.6kJ的热量,表示氢气燃烧的热化学方程式为_____ ,氢气的燃烧热为_____ kJ•mol-1.
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:

①反应I的△H_____ 0(填“<”“>”或“=”),反应Ⅱ的活化能是_____ kJ•mol-1。
②在相同条件下反应I的反应速率_____ (填“<”“>”或“=”)反应Ⅱ的反应速率。
③写出反应Ⅱ的热化学方程式_____ 。
(1)下列反应一定属于吸热反应的是_____。
| A.酸碱中和反应 | B.燃烧反应 | C.铝热反应 | D.C(s)+CO2(g)  2CO(g) 2CO(g) |
(2)在101kPa时,H2在1.0molO2中完全燃烧,生成2.0mol液态水,放出571.6kJ的热量,表示氢气燃烧的热化学方程式为
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:

①反应I的△H
②在相同条件下反应I的反应速率
③写出反应Ⅱ的热化学方程式
您最近一年使用:0次
名校
解题方法
9 . 按要求完成下列问题。
(1)反应 过程中的能量变化如图,回答下列问题。
过程中的能量变化如图,回答下列问题。

①该反应 =
=___________ (用含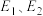 式子表示);
式子表示);
②在反应体系中加入催化剂,
___________ (填“增大”、“减小”、“不变”),
___________ (填“增大”、“减小”、“不变”)。
(2)在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应: ,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白
,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白
①x值等于___________ 。
②A的转化率为___________ 。
③生成D的反应速率为___________ 。
(3)在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图。
为原料生产尿素的反应历程与能量变化示意图如图。
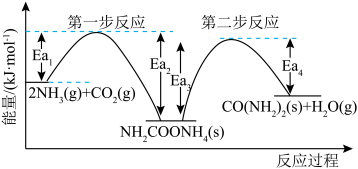
第二步反应的
___________ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第___________ 步反应。
(1)反应
 过程中的能量变化如图,回答下列问题。
过程中的能量变化如图,回答下列问题。
①该反应
 =
=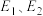 式子表示);
式子表示);②在反应体系中加入催化剂,


(2)在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:
 ,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白
,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白①x值等于
②A的转化率为
③生成D的反应速率为
(3)在碳循环中,以
 为原料生产尿素的反应历程与能量变化示意图如图。
为原料生产尿素的反应历程与能量变化示意图如图。
第二步反应的

您最近一年使用:0次
名校
解题方法
10 . 化学反应伴随能量变化,获取反应能量变化有多条途径
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。
已知:
计算可得:

___________ 
②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.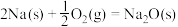
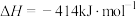
Ⅱ.
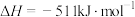
写出 与
与 反应生成
反应生成 的热化学方程式:
的热化学方程式:___________ 。
(3)以 、
、 为原料生产尿素[
为原料生产尿素[ ]的反应历程与能量变化示意图如图。
]的反应历程与能量变化示意图如图。

①第二步反应的
___________ 0(填“>”、“<”或“=”)
②从图像分析决定生产尿素的总反应的反应速率的步骤是第___________ 步反应。
(4)火箭和导弹表面的薄层是耐高温物质,将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,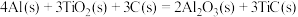
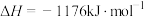 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为___________ kJ。
(1)下列反应中,属于吸热反应的是___________(填字母)。
A. 与水反应 与水反应 | B.甲烷的燃烧反应 |
C. 与氯化铵反应 与氯化铵反应 | D.锌与盐酸反应 |
①通过化学键的键能计算。
已知:
| 化学键种类 |  |  |  |
键能( ) ) | 436 | 247 | 434 |



②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.
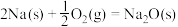
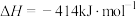
Ⅱ.

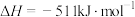
写出
 与
与 反应生成
反应生成 的热化学方程式:
的热化学方程式:(3)以
 、
、 为原料生产尿素[
为原料生产尿素[ ]的反应历程与能量变化示意图如图。
]的反应历程与能量变化示意图如图。
①第二步反应的

②从图像分析决定生产尿素的总反应的反应速率的步骤是第
(4)火箭和导弹表面的薄层是耐高温物质,将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
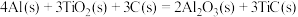
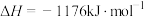 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为
您最近一年使用:0次
2023-10-17更新
|
171次组卷
|
2卷引用:四川省南充高级中学2023-2024学年高二上学期10月月考化学试题



