名校
解题方法
1 . 化学反应在发生物质变化的同时伴随着能量的变化,它是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。回答下列问题:
(1) 的反应过程如图所示:
的反应过程如图所示:
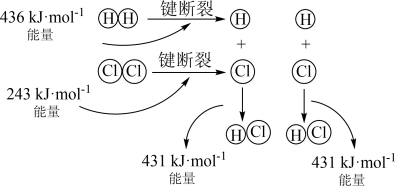
该反应为___________ (填“放热”或“吸热”)反应,生成2 mol 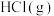 吸收或放出的热量为
吸收或放出的热量为___________ 。
(2)下列变化中属于吸热反应的是___________ (填标号)。
①液态水汽化②生石灰与水反应生成熟石灰③ ④
④ 与固体
与固体 混合
混合
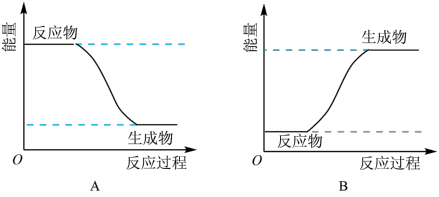
(3)某化学反应中,设反应物的总能量为 ,生成物的总能量为
,生成物的总能量为 。若
。若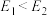 ,则该反应可用图
,则该反应可用图___________ (填“A”或“B”)表示。
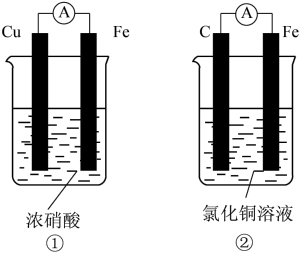
(4)为了验证 与
与 的氧化性强弱,图中能达到实验目的的装置是
的氧化性强弱,图中能达到实验目的的装置是___________ (填标号),其正极的电极反应式为___________ ;若构建该原电池时两个电极的质量相等,当导线中通过0.4 mol电子时,两个电极的质量差为___________ g。
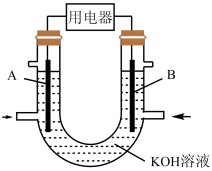
(5) 用于燃料电池后,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得
用于燃料电池后,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则
定向移向A电极,则___________ (填“A”或“B”)电极入口处通 ,
, 参与的电极反应为
参与的电极反应为___________ 。
(1)
 的反应过程如图所示:
的反应过程如图所示:
该反应为
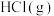 吸收或放出的热量为
吸收或放出的热量为(2)下列变化中属于吸热反应的是
①液态水汽化②生石灰与水反应生成熟石灰③
 ④
④ 与固体
与固体 混合
混合(3)某化学反应中,设反应物的总能量为
 ,生成物的总能量为
,生成物的总能量为 。若
。若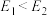 ,则该反应可用图
,则该反应可用图
(4)为了验证
 与
与 的氧化性强弱,图中能达到实验目的的装置是
的氧化性强弱,图中能达到实验目的的装置是
(5)
 用于燃料电池后,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得
用于燃料电池后,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则
定向移向A电极,则 ,
, 参与的电极反应为
参与的电极反应为
您最近一年使用:0次
2023-07-06更新
|
249次组卷
|
3卷引用:陕西省商洛市2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
2 . 工业制硫酸中的一步重要反应是 在400~500℃下的催化氧化。
在400~500℃下的催化氧化。
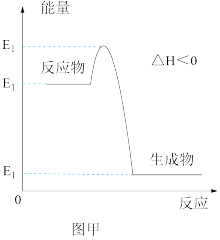
(1)根据图甲,该反应是___________ (填“放热”或者“吸热”)反应。 和5mol
和5mol ,反应过程中部分物质的物质的量随反应时间变化的曲线如图所示。恒温恒容时,下列措施能使该反应速率增大的是_____。
,反应过程中部分物质的物质的量随反应时间变化的曲线如图所示。恒温恒容时,下列措施能使该反应速率增大的是_____。
(3)2min时,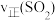
___________ 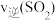 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)在图中画出 的物质的量随反应时间变化的曲线
的物质的量随反应时间变化的曲线_____ 。
 在400~500℃下的催化氧化。
在400~500℃下的催化氧化。(1)根据图甲,该反应是
 和5mol
和5mol ,反应过程中部分物质的物质的量随反应时间变化的曲线如图所示。恒温恒容时,下列措施能使该反应速率增大的是_____。
,反应过程中部分物质的物质的量随反应时间变化的曲线如图所示。恒温恒容时,下列措施能使该反应速率增大的是_____。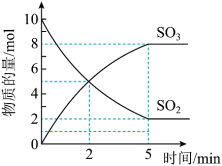
A.增加 的浓度 的浓度 | B.选择高效催化剂 | C.充入氦气 | D.适当降低温度 |
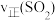
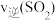 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)在图中画出
 的物质的量随反应时间变化的曲线
的物质的量随反应时间变化的曲线
您最近一年使用:0次
名校
解题方法
3 . 利用太阳能分解H2O获得H2,再通过CO2加氢制甲醇(CH3OH)等燃料,从而实现可再生能源和CO2的资源化利用。
(1)已知2H2O(g)=2H2(g)+O2(g)△H>0,下列说法正确的是 ;
(2)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH+H2O(g)该反应的反应历程如图一所示:
①二氧化碳加氢制甲醇的总反应为________ (填“放热”或“吸热“)反应。
②上述反应历程中有________ (填“1“”、“2”或“3“)步基元反应,通常将其中的慢反应称为决速步,此步骤活化能较高,根据如图写出决速步的反应为________ ;
(3)CO2催化加氢制取甲醇,反应如下:
主反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49kJ•mol-1
副反应:CO2(g)+H2(g)=CO(g)+H2O(g)△H2=+41.2kJ•mol-1
写出CO、H2生成CH3OH(g)的热化学方程式________ ;
(4)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步是先将二氧化碳还原为甲醛(HCHO),过程如图二所示:
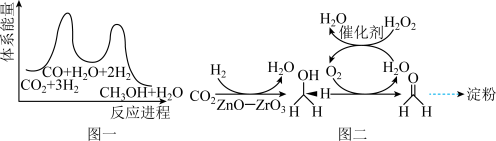
请写出前两步总反应的化学方程式________ ;
(1)已知2H2O(g)=2H2(g)+O2(g)△H>0,下列说法正确的是 ;
| A.从宏观来看,2molH2O(g)的总能量高于2molH2(g)+1molO2(g)的总能量 |
| B.从微观来看,2molH2O(g)中总键能高于2molH2(g)+1molO2(g)的总键能 |
| C.此反应正反应的活化能高于逆反应的活化能 |
| D.加入催化剂后改变反应途径,活化能降低,反应的△H减小 |
①二氧化碳加氢制甲醇的总反应为
②上述反应历程中有
(3)CO2催化加氢制取甲醇,反应如下:
主反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49kJ•mol-1
副反应:CO2(g)+H2(g)=CO(g)+H2O(g)△H2=+41.2kJ•mol-1
写出CO、H2生成CH3OH(g)的热化学方程式
(4)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接经过11步路径人工合成淀粉。前两步是先将二氧化碳还原为甲醛(HCHO),过程如图二所示:

请写出前两步总反应的化学方程式
您最近一年使用:0次
解题方法
4 . Ⅰ.某实验小组同学进行如图1实验,以检验化学反应中的能量变化。请回答下列问题:
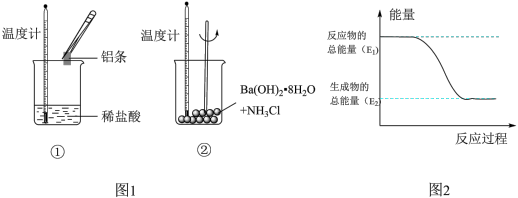
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是________ 热反应。反应过程________ (填“①”或“②”)的能量变化可用图2表示。
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
(2)根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是________ 。
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是________ 。
A. B.
B.
C. D.
D.

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 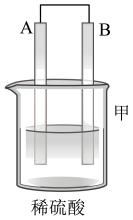 | 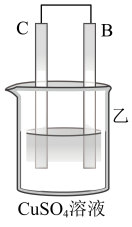 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
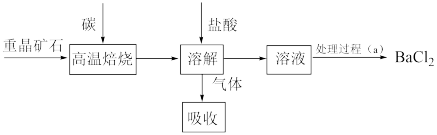
5 . 硫酸盐在生产、生活中有广泛的应用。工业上以重晶石(主要成分 )为原料制备
)为原料制备 ,其工艺流程示意图如下:
,其工艺流程示意图如下:
某研究小组查阅资料得:

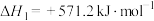 ①
①

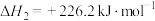 ②
②
(1)用过量NaOH溶液吸收气体,得到硫化钠。该反应的离子方程式是_____ 。
(2)实际生产中必须加入过量的碳,同时还要通入空气,其目的有两个:
a.从原料角度看_____ ;
b.从能量角度看_____ ;
(3)处理过程(a)包括操作名称是_____ 。
 )为原料制备
)为原料制备 ,其工艺流程示意图如下:
,其工艺流程示意图如下:
某研究小组查阅资料得:

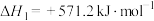 ①
①
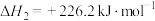 ②
②(1)用过量NaOH溶液吸收气体,得到硫化钠。该反应的离子方程式是
(2)实际生产中必须加入过量的碳,同时还要通入空气,其目的有两个:
a.从原料角度看
b.从能量角度看
(3)处理过程(a)包括操作名称是
您最近一年使用:0次
名校
解题方法
6 . 已知断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B的键能。如表列出了一些化学键的键能(E):
(1)反应H2(g)+ O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=______ 。
(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
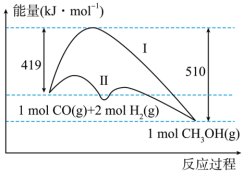
①计算当反应生成1.5molCH3OH(g)时,能量变化值是______ kJ。
②推测反应CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是______ (填“吸热”或“放热”)反应。
(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
①表中,a为______ mol。
②由表可知,3~6min内,v(CO2)=______ mol•L-1•min-1。
③对于上述反应,下列叙述正确的是______ 。
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
| 化学键 | H-H | O=O | O-H |
| E/(kJ•mol-1) | 436 | x | 463 |
 O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
①计算当反应生成1.5molCH3OH(g)时,能量变化值是
②推测反应CH3OH(g)
 CO(g)+2H2(g)是
CO(g)+2H2(g)是(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH) | 0mol | 0.50mol | 0.65mol | 0.75mol | 0.75mol |
| n(CO2) | 1mol | 0.50mol | 0.35mol | a | 0.25mol |
②由表可知,3~6min内,v(CO2)=
③对于上述反应,下列叙述正确的是
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
您最近一年使用:0次
解题方法
7 . 从物质分类的角度看, 和
和 都属于氧化物,但二者的性质存在很大差异。查阅资料得知,
都属于氧化物,但二者的性质存在很大差异。查阅资料得知, 可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究
可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究 的性质与用途。
的性质与用途。
【实验I】探究 与水的反应
与水的反应
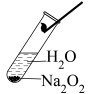
(1)如图,将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,立即把带火星的小木条伸入试管中,观察到带火星的小木条复燃,说明生成了______ ,用手触摸试管外壁,感觉发烫,说明该反应是______ (填“吸热”或“放热”)反应。用pH计测得溶液呈碱性,说明该反应还生成了______ 。
【实验II】探究 与
与 的反应
的反应
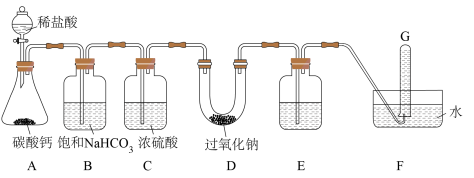
(2)装置A用于制备______ 气体,盛装稀盐酸的仪器名称是______ 。
(3)装置B的作用是______ 。
(4)写出D中发生反应的化学方程式:______ 。
(5)装置E的作用是除去过量的 ,则装置E中盛装的试剂是
,则装置E中盛装的试剂是______ 。
(6)G中得到的物质是______ ,证明 可用作呼吸面具和潜水艇的供氧剂。
可用作呼吸面具和潜水艇的供氧剂。
 和
和 都属于氧化物,但二者的性质存在很大差异。查阅资料得知,
都属于氧化物,但二者的性质存在很大差异。查阅资料得知, 可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究
可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究 的性质与用途。
的性质与用途。【实验I】探究
 与水的反应
与水的反应
(1)如图,将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,立即把带火星的小木条伸入试管中,观察到带火星的小木条复燃,说明生成了
【实验II】探究
 与
与 的反应
的反应
(2)装置A用于制备
(3)装置B的作用是
(4)写出D中发生反应的化学方程式:
(5)装置E的作用是除去过量的
 ,则装置E中盛装的试剂是
,则装置E中盛装的试剂是(6)G中得到的物质是
 可用作呼吸面具和潜水艇的供氧剂。
可用作呼吸面具和潜水艇的供氧剂。
您最近一年使用:0次
解题方法
8 . 硫酰氯( )是工业合成的氯化剂,在生产中有广泛应用。制备原理是
)是工业合成的氯化剂,在生产中有广泛应用。制备原理是 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和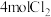 只发生上述反应。测得
只发生上述反应。测得 的物质的量变化如图所示。回答下列问题:
的物质的量变化如图所示。回答下列问题:

(1)经测定,生成物的总能量低于反应物的总能量。该反应的正反应是________ (填“吸热”或“放热”)反应。
(2)a点正反应速率________ (填“大于”“小于”或“等于”)逆反应速率。此时 的转化率为
的转化率为________ %。
(3)在上述条件下,a、b、c点中,反应达到最大限度的点是________ 。b点逆反应速率________ c点正反应速率(填“>”“=”或“<”)。
(4)从反应开始到c点时间内平均速率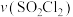 为
为________  。
。
(5)温度不变,加入催化剂, 最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
(6)c点时各组成浓度比值
________ 。
 )是工业合成的氯化剂,在生产中有广泛应用。制备原理是
)是工业合成的氯化剂,在生产中有广泛应用。制备原理是 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和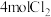 只发生上述反应。测得
只发生上述反应。测得 的物质的量变化如图所示。回答下列问题:
的物质的量变化如图所示。回答下列问题:
(1)经测定,生成物的总能量低于反应物的总能量。该反应的正反应是
(2)a点正反应速率
 的转化率为
的转化率为(3)在上述条件下,a、b、c点中,反应达到最大限度的点是
(4)从反应开始到c点时间内平均速率
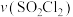 为
为 。
。(5)温度不变,加入催化剂,
 最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。| A.水平右移 | B.水平左移 | C.向左下方移动 | D.向右上方移动 |

您最近一年使用:0次
解题方法
9 . 能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。制作冷敷袋可以利用___________ 。(填标号)
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
(2)氢能是一种极具发展潜力的清洁能源。
①已知:断裂 、
、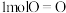 和
和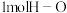 需要的能量依次为436kJ、498kJ和463kJ,则理论上每
需要的能量依次为436kJ、498kJ和463kJ,则理论上每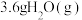 完全分解,需
完全分解,需___________ (填“放出”或“吸收”)___________ kJ能量。下列能正确表示该过程的能量变化的是___________ (填标号)。
A. B.
B. C.
C.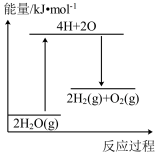 D.
D.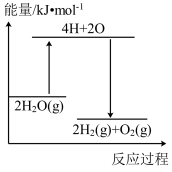
②长征五号被称为“冰箭”,这缘于长征五号“肚子”里装着满满的深低温液氢、液氧燃料。中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如图所示。下列说法错误的是___________ (填标号)。

A.整个过程实现了光能向化学能的转化
B.过程Ⅱ吸收能量
C.过程Ⅲ发生的反应: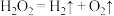
D.上述过程的总反应:2H2O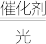 2H2↑+O2↑
2H2↑+O2↑
③氢燃料电池具有清洁高效等优点,其简易装置如图所示。该电池正极上的反应式为_______ ;反应过程中将_______ 能转化为_______ 能。
④氢能是发展中的新能源,与汽油相比, 作为燃料的优点是
作为燃料的优点是___________ 。 直接燃烧的能量转化率
直接燃烧的能量转化率___________ (填“高于”、“等于”或“低于”)燃料电池。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。制作冷敷袋可以利用
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
(2)氢能是一种极具发展潜力的清洁能源。
①已知:断裂
 、
、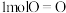 和
和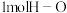 需要的能量依次为436kJ、498kJ和463kJ,则理论上每
需要的能量依次为436kJ、498kJ和463kJ,则理论上每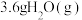 完全分解,需
完全分解,需A.
 B.
B. C.
C. D.
D.
②长征五号被称为“冰箭”,这缘于长征五号“肚子”里装着满满的深低温液氢、液氧燃料。中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如图所示。下列说法错误的是

A.整个过程实现了光能向化学能的转化
B.过程Ⅱ吸收能量
C.过程Ⅲ发生的反应:
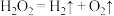
D.上述过程的总反应:2H2O
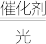 2H2↑+O2↑
2H2↑+O2↑③氢燃料电池具有清洁高效等优点,其简易装置如图所示。该电池正极上的反应式为

④氢能是发展中的新能源,与汽油相比,
 作为燃料的优点是
作为燃料的优点是 直接燃烧的能量转化率
直接燃烧的能量转化率
您最近一年使用:0次
名校
10 . 甲烷在自然界的分布很广,是天然气、沼气、煤矿坑道气的主要成分,它可用来作为燃料以及制造合成气、炭黑等物质的原料。甲烷用于生产合成气的反应为 。请回答下列问题:
。请回答下列问题:
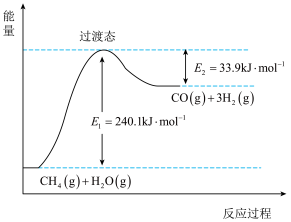
(1)反应过程中的能量变化如下图所示,1mol 参加反应时
参加反应时___________ (填“吸收”或“放出”)的能量为___________ kJ。
(2)T℃时,向2L恒容密闭容器中投入1mol 和1mol
和1mol ,发生反应:
,发生反应:
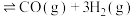 ,经过5min,反应达到平衡,已知平衡时
,经过5min,反应达到平衡,已知平衡时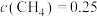 mol∙L
mol∙L 。
。
①0~5min内,该反应的平均反应速率
___________ ,平衡时CO的物质的量为___________ 。
②下列表述能说明该反应达到化学平衡状态的是___________ 。
a.反应速率
b. 的物质的量浓度不再改变
的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内断裂1molH—O键同时断裂3molH—H键
(3)科学家利用甲烷生产的合成气,发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。
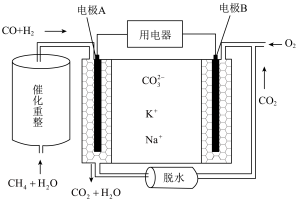
内电路中阴离子向电极___________ (填A或B)移动,试写出B电极的电极反应式___________ 。
 。请回答下列问题:
。请回答下列问题:(1)反应过程中的能量变化如下图所示,1mol
 参加反应时
参加反应时
(2)T℃时,向2L恒容密闭容器中投入1mol
 和1mol
和1mol ,发生反应:
,发生反应:
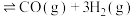 ,经过5min,反应达到平衡,已知平衡时
,经过5min,反应达到平衡,已知平衡时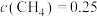 mol∙L
mol∙L 。
。①0~5min内,该反应的平均反应速率

②下列表述能说明该反应达到化学平衡状态的是
a.反应速率

b.
 的物质的量浓度不再改变
的物质的量浓度不再改变c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内断裂1molH—O键同时断裂3molH—H键
(3)科学家利用甲烷生产的合成气,发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。

内电路中阴离子向电极
您最近一年使用:0次



