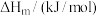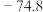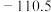名校
解题方法
1 . 2024年上海国际碳中和技术博览会以“中和科技、碳素未来”为主题,重点聚焦二氧化碳的捕捉、利用与封存(CCUS)等问题。回答下列问题:
Ⅰ. 是典型的温室气体,Sabatier反应可实现
是典型的温室气体,Sabatier反应可实现 转化为甲烷,实现
转化为甲烷,实现 的资源化利用。合成
的资源化利用。合成 过程中涉及如下反应:
过程中涉及如下反应:
甲烷化反应(主反应):①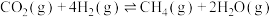

逆变换反应(副反应):②

(1)反应③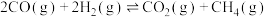

___________ ,该反应在___________ (填“高温”“低温”或“任何温度”)下能自发进行。
(2)下列叙述中能说明反应①达到平衡状态的是___________ (填字母)。
A.断裂4mol 的同时断裂1mol
的同时断裂1mol 
B.恒温恒容条件下,体系压强不再变化
C.恒温恒容条件下,气体的密度不再变化
D.
E.绝热恒容条件下, 不再变化
不再变化
(3)科研小组按 进行投料,下面探究影响
进行投料,下面探究影响 选择性的一些因素。
选择性的一些因素。
①若在恒容容器中进行反应(初始压强为0.1MPa),平衡时各气体的物质的量分数随温度变化的曲线如图所示。图中表示 的物质的量分数随温度变化的曲线是
的物质的量分数随温度变化的曲线是___________ (填“曲线1”“曲线2”或“曲线3”)。曲线1和曲线3交叉点处 的平衡分压为
的平衡分压为___________ MPa(该空忽略副反应逆变换反应)。
反应a:

反应b: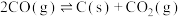

反应c: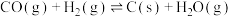

由表中数据可知,积碳反应主要由反应___________ 引起(填“a”“b”或“c”)。
Ⅱ.完成下列问题
(4)一定条件下,向4L恒容密闭容器中充入2mol 和6mol
和6mol  ,发生反应
,发生反应 。已知容器内起始压强为240kPa,反应达平衡时容器内压强为150kPa,该温度下反应的标准平衡常数
。已知容器内起始压强为240kPa,反应达平衡时容器内压强为150kPa,该温度下反应的标准平衡常数
___________ 。(该反应标准平衡常数的表达式为 ,其中p为分压,分压=总压×物质的量分数,
,其中p为分压,分压=总压×物质的量分数,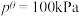 )
)
Ⅰ.
 是典型的温室气体,Sabatier反应可实现
是典型的温室气体,Sabatier反应可实现 转化为甲烷,实现
转化为甲烷,实现 的资源化利用。合成
的资源化利用。合成 过程中涉及如下反应:
过程中涉及如下反应:甲烷化反应(主反应):①
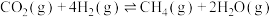

逆变换反应(副反应):②


(1)反应③
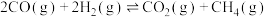

(2)下列叙述中能说明反应①达到平衡状态的是
A.断裂4mol
 的同时断裂1mol
的同时断裂1mol 
B.恒温恒容条件下,体系压强不再变化
C.恒温恒容条件下,气体的密度不再变化
D.

E.绝热恒容条件下,
 不再变化
不再变化(3)科研小组按
 进行投料,下面探究影响
进行投料,下面探究影响 选择性的一些因素。
选择性的一些因素。①若在恒容容器中进行反应(初始压强为0.1MPa),平衡时各气体的物质的量分数随温度变化的曲线如图所示。图中表示
 的物质的量分数随温度变化的曲线是
的物质的量分数随温度变化的曲线是 的平衡分压为
的平衡分压为
| 温度℃ |  |  |  |
| 800 | 21.60 | 0.136 | 0.133 |
| 850 | 33.94 | 0.058 | 0.067 |
| 900 | 51.38 | 0.027 | 0.036 |


反应b:
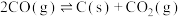

反应c:
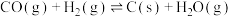

由表中数据可知,积碳反应主要由反应
Ⅱ.完成下列问题
(4)一定条件下,向4L恒容密闭容器中充入2mol
 和6mol
和6mol  ,发生反应
,发生反应 。已知容器内起始压强为240kPa,反应达平衡时容器内压强为150kPa,该温度下反应的标准平衡常数
。已知容器内起始压强为240kPa,反应达平衡时容器内压强为150kPa,该温度下反应的标准平衡常数
 ,其中p为分压,分压=总压×物质的量分数,
,其中p为分压,分压=总压×物质的量分数,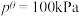 )
)
您最近一年使用:0次
昨日更新
|
116次组卷
|
3卷引用:2024届湖南省岳阳市高三下学期三模化学试题
名校
解题方法
2 . 在298K、 下,将
下,将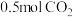 通入
通入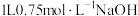 溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下,
溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下, 通入
通入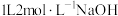 溶液中充分反应放出y kJ的热量,则
溶液中充分反应放出y kJ的热量,则 与NaOH溶液反应生成
与NaOH溶液反应生成 的热化学方程式正确的是
的热化学方程式正确的是
 下,将
下,将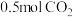 通入
通入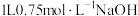 溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下,
溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下, 通入
通入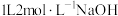 溶液中充分反应放出y kJ的热量,则
溶液中充分反应放出y kJ的热量,则 与NaOH溶液反应生成
与NaOH溶液反应生成 的热化学方程式正确的是
的热化学方程式正确的是A.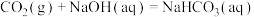 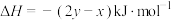 |
B.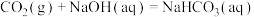 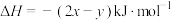 |
C.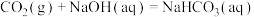  |
D.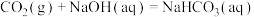 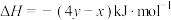 |
您最近一年使用:0次
3 . 在一定的温度和压强下,将按一定比例混合的CO2和H2通过装有催化剂的反应器可得到甲烷.
已知: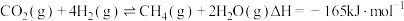
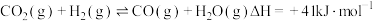
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.
下列有关说法错误的是
已知:
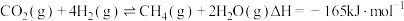
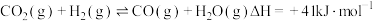
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.
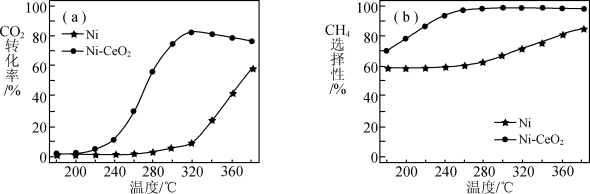
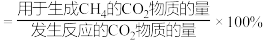
下列有关说法错误的是
A.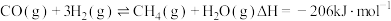 |
| B.延长W点的反应时间,能提高CO2的转化率 |
| C.在260~320℃间,以Ni-CeO2为催化剂,升高温度CH4的产率不变 |
| D.选择合适的催化剂、合适的温度有利于提高CH4的选择性 |
您最近一年使用:0次
名校
4 . 某温度下,利用CO2生产甲醇主要涉及以下两个反应。
反应I._______
反应Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
回答下列问题:
(1)已知CO(g)+2H2(g) CH3OH(g) ΔH3=–90.6kJ·mol-1。反应I的转化原理如图所示。该反应的热化学方程式为
CH3OH(g) ΔH3=–90.6kJ·mol-1。反应I的转化原理如图所示。该反应的热化学方程式为_______ ,在_______ 条件下反应I可自发发生。_______ 移动(填“正向”、“逆向”或“不”)。
(3)将1molCO2(g)和3molH2(g)充入密闭容器发生反应I和Ⅱ,并达到平衡状态。相同温度下,在不同压强下测得CO2的平衡转化率、CH3OH(g)的选择性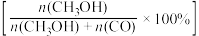 和CO的选择性
和CO的选择性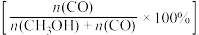 随压强变化曲线如图所示。图中表示CO2的平衡转化率的曲线是
随压强变化曲线如图所示。图中表示CO2的平衡转化率的曲线是_______ (填“m”、“n”或“p”),A点时H2的转化率为_______ ,CH3OH的平衡分压为_______ MPa(保留两位有效数字)。 ,式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示各组分的物质的量分数。Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp
,式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示各组分的物质的量分数。Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp_______ (填“增大”、“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是_______ 。
反应I._______
反应Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
回答下列问题:
(1)已知CO(g)+2H2(g)
 CH3OH(g) ΔH3=–90.6kJ·mol-1。反应I的转化原理如图所示。该反应的热化学方程式为
CH3OH(g) ΔH3=–90.6kJ·mol-1。反应I的转化原理如图所示。该反应的热化学方程式为
(3)将1molCO2(g)和3molH2(g)充入密闭容器发生反应I和Ⅱ,并达到平衡状态。相同温度下,在不同压强下测得CO2的平衡转化率、CH3OH(g)的选择性
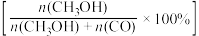 和CO的选择性
和CO的选择性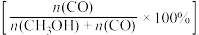 随压强变化曲线如图所示。图中表示CO2的平衡转化率的曲线是
随压强变化曲线如图所示。图中表示CO2的平衡转化率的曲线是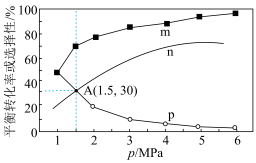
 ,式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示各组分的物质的量分数。Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp
,式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示各组分的物质的量分数。Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的Kp
您最近一年使用:0次
5 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(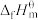 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
则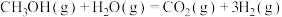 △H=
△H=___________ kJ∙mol-1,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:
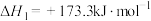
反应②:

(2)向恒容密闭容器中充入1mol 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时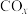 的分布分数
的分布分数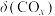 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。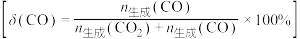
___________ (写出2条)。
②200℃以后,解释曲线a随温度变化趋势的原因:___________ 。
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内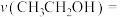
___________ kPa∙min-1,该温度下,反应②的Kp=___________ (保留小数点后两位)。
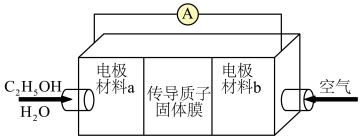
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:___________ ,当转移1.2mol电子时,正极消耗的氧气的体积为___________ L(标准状况下)。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(
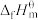 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。| 物质 |  |  |  |  |
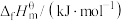 | 0 | ―393.5 | ―241.8 | ―200.7 |
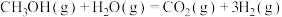 △H=
△H=Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:

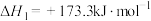
反应②:


(2)向恒容密闭容器中充入1mol
 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时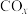 的分布分数
的分布分数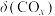 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。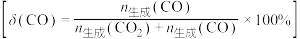
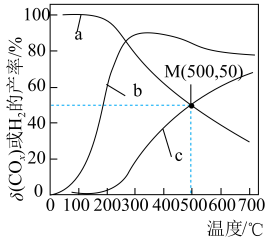
②200℃以后,解释曲线a随温度变化趋势的原因:
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内
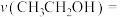
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:
您最近一年使用:0次
2024-05-19更新
|
94次组卷
|
3卷引用:河南省新乡市2024届高三第三次模拟考试理综-化学试题
名校
6 . 链状葡萄糖分子中的醛基可与分子内羟基发生加成反应形成两种六元环状结构。常温下,各种葡萄糖结构及其所占百分含量如下图所示。已知各种葡萄糖结构中链状结构的熵最大,两种环状结构的熵相近。下列说法正确的是

A. |
B.三种结构中,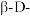 吡喃葡萄糖的焓最小 吡喃葡萄糖的焓最小 |
| C.葡萄糖由链状转化为环状结构是醛基和6号碳原子上羟基作用的结果 |
D.18g葡萄糖完全燃烧生成 和 和 放热akJ,故葡萄糖的燃烧热为10akJ/mol 放热akJ,故葡萄糖的燃烧热为10akJ/mol |
您最近一年使用:0次
名校
7 . 铜及其化合物是高中化学的重要组成部分,在工农业生产中具有重要的应用。
(1)在农业上可用含铜的波尔多液作为农药,配制波尔多液需要___________ (填化学式)。
(2)已知CuCl在氨水中络合后极易被空气中的 氧化。
氧化。
①补齐下列离子方程式:__________ 。
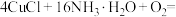 ___________
___________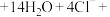 ___________
___________
②现将Cu置于 溶液中,通入
溶液中,通入 ,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为
,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为___________ 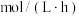 。
。
(3)查阅文献:在无氧条件下CuCl在氨水溶液中存下如下平衡(含足量CuCl固体)
ⅰ:

ⅱ: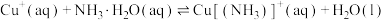

ⅲ: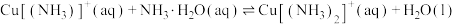

①反应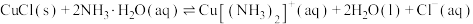

___________ (用 、
、 、
、 来表示);在上述反应中,配原子是
来表示);在上述反应中,配原子是___________ (填元素符号)。
②对于上述相关平衡体系,下列说法不正确的是:___________ (填编号)
A.加水稀释,平衡后溶液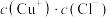 不变
不变
B.向体系中通入 ,有利于提高
,有利于提高 平衡转化率
平衡转化率
C.升高温度,有利于生成
D.溶液中存在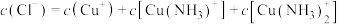
③向一定浓度的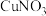 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数
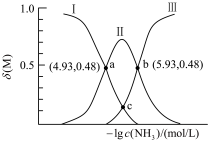
得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数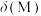 与
与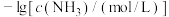 关系如下图所示(其中M代表体系中含铜微粒)。如
关系如下图所示(其中M代表体系中含铜微粒)。如 的分布系数
的分布系数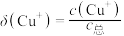 ,
, 。
。___________ 分布系数(填离子符号)。
(b)反应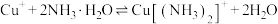 的
的
___________ 。(已知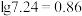 )
)
(c)c点的坐标为___________ 。(已知 )
)
(1)在农业上可用含铜的波尔多液作为农药,配制波尔多液需要
(2)已知CuCl在氨水中络合后极易被空气中的
 氧化。
氧化。①补齐下列离子方程式:
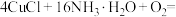 ___________
___________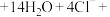 ___________
___________②现将Cu置于
 溶液中,通入
溶液中,通入 ,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为
,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为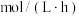 。
。(3)查阅文献:在无氧条件下CuCl在氨水溶液中存下如下平衡(含足量CuCl固体)
ⅰ:


ⅱ:
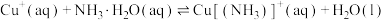

ⅲ:
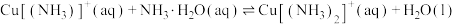

①反应
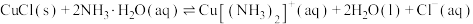

 、
、 、
、 来表示);在上述反应中,配原子是
来表示);在上述反应中,配原子是②对于上述相关平衡体系,下列说法不正确的是:
A.加水稀释,平衡后溶液
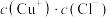 不变
不变B.向体系中通入
 ,有利于提高
,有利于提高 平衡转化率
平衡转化率C.升高温度,有利于生成

D.溶液中存在
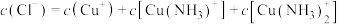
③向一定浓度的
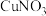 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数
得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数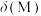 与
与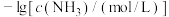 关系如下图所示(其中M代表体系中含铜微粒)。如
关系如下图所示(其中M代表体系中含铜微粒)。如 的分布系数
的分布系数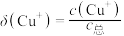 ,
, 。
。
(b)反应
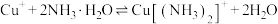 的
的
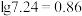 )
)(c)c点的坐标为
 )
)
您最近一年使用:0次
解题方法
8 . 甲烷干重整反应可以强化碳酸钙分解.
I.碳酸钙分解: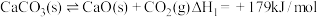
Ⅱ.甲烷干重整: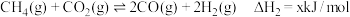
(1)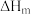 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
___________ .
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.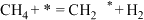 Ⅱ.
Ⅱ.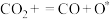
Ⅲ.___________ IV. V.
V.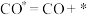
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量 和
和 ;
;
①下列能说明反应达到平衡状态的是___________ (填字母);
a. b.
b. 和
和 的体积比保持不变
的体积比保持不变
c.每生成 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变
②反应达到平衡时, 的转化率为
的转化率为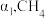 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
___________ ;(用含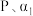 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下: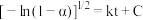 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在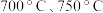 得到的
得到的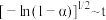 的曲线如图所示:
的曲线如图所示: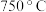 的曲线是曲线
的曲线是曲线___________ ,用碰撞理论解释原因___________ ;
(5)在某温度下,催化剂活性良好,加入一定量的 ,通入
,通入 ,和
,和 的流速为
的流速为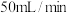 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是___________ 。
I.碳酸钙分解:
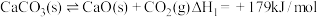
Ⅱ.甲烷干重整:
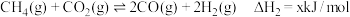
(1)
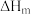 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
|
|
|
| |
|
|
|
| 0 |
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.
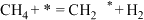 Ⅱ.
Ⅱ.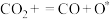
Ⅲ.
 V.
V.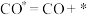
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量
 和
和 ;
;①下列能说明反应达到平衡状态的是
a.
 b.
b. 和
和 的体积比保持不变
的体积比保持不变c.每生成
 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变②反应达到平衡时,
 的转化率为
的转化率为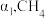 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
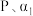 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下:
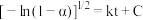 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在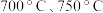 得到的
得到的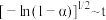 的曲线如图所示:
的曲线如图所示: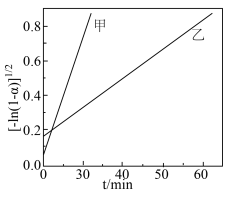
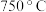 的曲线是曲线
的曲线是曲线(5)在某温度下,催化剂活性良好,加入一定量的
 ,通入
,通入 ,和
,和 的流速为
的流速为 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是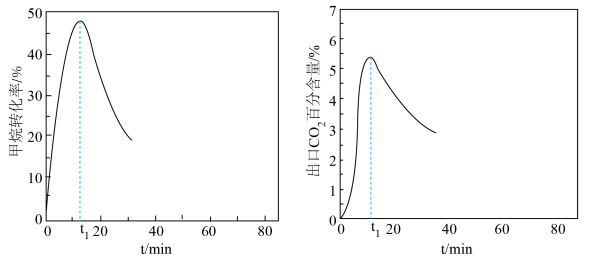
您最近一年使用:0次
解题方法
9 . 甲烷干重整(DRM)以温室气体CH4和CO2为原料在催化条件下生成合成气CO和H2.体系中发生的反应有
ⅰ.CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1=+247kJ/mol
2CO(g)+2H2(g) △H1=+247kJ/mol
ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41kJ。mol1
CO(g)+H2O(g) △H2=+41kJ。mol1
ⅲ.CH4(g) C(s)+2H2(g) △H3=+74.9kJ/mol
C(s)+2H2(g) △H3=+74.9kJ/mol
ⅳ.2CO(g) C(s)+CO2(g) △H4
C(s)+CO2(g) △H4
(1)△H4=___________ kJ/mol。
(2)___________ (填“高温”或“低温”)有利于反应ⅰ自发进行。
(3)起始投入CH4和CO2各1kmol,DRM反应过程中所有物质在100kPa下的热力学平衡数据如图1所示。___________ (填“升高”、“不变”或“降低”),理由是___________ 。
②625℃时,起始投入CH4、CO2、H2、CO、H2O各0.5kmol,此时反应ⅱ的v正___________ v逆(填“>”“=”或“<”)。
(4)CO2在Ni基催化剂表面氢助解离有两种可能路径,图2为不同解离路径的能量变化,其中吸附在催化剂表面上的物种用*标注。___________ 。
②写出最有可能发生的“氢助解离”路径的决速步反应方程式___________ 。
ⅰ.CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1=+247kJ/mol
2CO(g)+2H2(g) △H1=+247kJ/molⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41kJ。mol1
CO(g)+H2O(g) △H2=+41kJ。mol1ⅲ.CH4(g)
 C(s)+2H2(g) △H3=+74.9kJ/mol
C(s)+2H2(g) △H3=+74.9kJ/molⅳ.2CO(g)
 C(s)+CO2(g) △H4
C(s)+CO2(g) △H4(1)△H4=
(2)
(3)起始投入CH4和CO2各1kmol,DRM反应过程中所有物质在100kPa下的热力学平衡数据如图1所示。
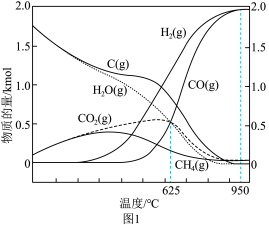
②625℃时,起始投入CH4、CO2、H2、CO、H2O各0.5kmol,此时反应ⅱ的v正
(4)CO2在Ni基催化剂表面氢助解离有两种可能路径,图2为不同解离路径的能量变化,其中吸附在催化剂表面上的物种用*标注。
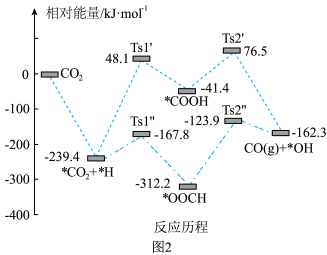
②写出最有可能发生的“氢助解离”路径的决速步反应方程式
您最近一年使用:0次
名校
解题方法
10 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为 、
、 、
、 )在催化剂作用下合成甲醇,主要发生的反应有:
)在催化剂作用下合成甲醇,主要发生的反应有:
反应Ⅰ.


反应Ⅱ.


反应Ⅲ.
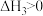

回答下列问题:
(1)_______ (填“低温”“高温”或“任意温度”)有利于反应Ⅰ自发进行,反应Ⅰ的
_______ (用含 和
和 的代数式表示),
的代数式表示),
_______ (用含 和
和 的代数式表示)。
的代数式表示)。
(2)在某一密闭容器中充入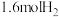 、
、 和
和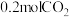 ,同时发生上述三个反应,且
,同时发生上述三个反应,且 平衡转化率与温度和压强的关系如图所示。
平衡转化率与温度和压强的关系如图所示。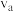
_______ (填“ ”“
”“ ”或“
”或“ ”)
”)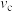 。
。
②氧元素的物质的量分数: 点
点_______ (填“ ”“
”“ ”或“
”或“ ”)
”) 点。
点。
③ 平衡转化率随温度升高而降低,其原因
平衡转化率随温度升高而降低,其原因_______ 。
④ ,
, 点时,测得体系中
点时,测得体系中 ,则此时
,则此时 的物质的量为
的物质的量为_____  ,该温度下
,该温度下 点反应Ⅲ的平衡常数
点反应Ⅲ的平衡常数
____ (分压 物质的量分数
物质的量分数 总压)。
总压)。
 、
、 、
、 )在催化剂作用下合成甲醇,主要发生的反应有:
)在催化剂作用下合成甲醇,主要发生的反应有:反应Ⅰ.



反应Ⅱ.



反应Ⅲ.

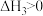

回答下列问题:
(1)

 和
和 的代数式表示),
的代数式表示),
 和
和 的代数式表示)。
的代数式表示)。(2)在某一密闭容器中充入
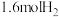 、
、 和
和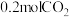 ,同时发生上述三个反应,且
,同时发生上述三个反应,且 平衡转化率与温度和压强的关系如图所示。
平衡转化率与温度和压强的关系如图所示。
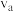
 ”“
”“ ”或“
”或“ ”)
”)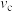 。
。②氧元素的物质的量分数:
 点
点 ”“
”“ ”或“
”或“ ”)
”) 点。
点。③
 平衡转化率随温度升高而降低,其原因
平衡转化率随温度升高而降低,其原因④
 ,
, 点时,测得体系中
点时,测得体系中 ,则此时
,则此时 的物质的量为
的物质的量为 ,该温度下
,该温度下 点反应Ⅲ的平衡常数
点反应Ⅲ的平衡常数
 物质的量分数
物质的量分数 总压)。
总压)。
您最近一年使用:0次