1 . 拟用如图装置设计实验来探究纯净、干燥的氯气与氨气的反应。___________ 。
(2)如图中的装置连接顺序为A→___________ (用大写字母表示)。若按照正确顺序连接实验装置后,整套实验装置存在的主要缺点___________ 。
(3)写出F装置中的反应的一种工业用途:___________ 。
(4)在工业上利用反应N2+3H2 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是___________ (填字母)。
A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)

(2)如图中的装置连接顺序为A→
(3)写出F装置中的反应的一种工业用途:
(4)在工业上利用反应N2+3H2
 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)
您最近一年使用:0次
名校
解题方法
2 . 将0.5 mol PCl5充入体积为1 L的密闭容器中发生反应:PCl5⇌PCl3+Cl2,达到平衡后测得PCl5的浓度为0.3 mol·L-1,而且这段时间内的平均反应速率v(PCl5)=0.4 mol·L-1·min-1,则这段时间为
| A.1.5 min | B.2.5 min | C.30 s | D.15 s |
您最近一年使用:0次
2023-02-02更新
|
482次组卷
|
2卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(三)
名校
3 . 将CH4和CO2重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:
主反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)
积碳反应:CH4(g)⇌C(s)+2H2(g) =+75 kJ/mol
=+75 kJ/mol
回答问题(1)~(3):
(1)已知:2CO(g)⇌CO2(g)+C(s) =-172 kJ/mol, 则
=-172 kJ/mol, 则 =
=_______ kJ/mol
(2)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是________.(填标号)
(3)在体积为5L恒容密闭容器中充入2.0mol CH4和4.0molCO2,500℃下仅发生主反应,CH4、CO2的物质的量随时间变化如下表所示:
①CO2在 0~30 min 内的平均反应速率v(CO2)= ___________ 。
②主反应的平衡常数表达式为_____________ 。
③若在60min 时再充入2.0 mol CH4,达到新平衡后CH4的转化率减小,此时平衡常数K_______ (填“增大”、“减小”或“不变”)
④ 若相同条件下改为充入4.0 mol CH4和 8.0 mol CO2反应,平衡后CH4的转化率______ 90%(填“<”、“=”或“>”)。
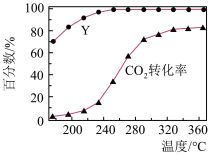
(4)CO2催化加H2可以制备CH4,保持反应气中CO2与 H2的体积比为 1∶4,以40 mL·min-1的流速通过催化剂,甲烷化过程中,含碳产物CH4的物质的量百分数(Y)及CO2的转化率随温度的变化如图所示。320℃时CO2反应速率为__________ mL·min-1。
主反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)

积碳反应:CH4(g)⇌C(s)+2H2(g)
 =+75 kJ/mol
=+75 kJ/mol回答问题(1)~(3):
(1)已知:2CO(g)⇌CO2(g)+C(s)
 =-172 kJ/mol, 则
=-172 kJ/mol, 则 =
=(2)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是________.(填标号)
| A.容器内的压强不再变化 | B.c (CH4):c(CO2): c (CO): c (H2)=1:1:2:2 |
| C.混合气体的密度不再变化 | D.断开4molC-H键同时断开2molH-H键 |
| 时间/min 反应物 | 0 | 15 | 30 | 45 | 60 | 75 |
| n(CH4)/mol | 2.0 | 1.3 | 0.8 | 0.4 | 0.2 | 0.2 |
| n(CO2)/mol | 4.0 | 3.3 | 2.8 | 2.4 | 2.2 | 2.2 |
②主反应的平衡常数表达式为
③若在60min 时再充入2.0 mol CH4,达到新平衡后CH4的转化率减小,此时平衡常数K
④ 若相同条件下改为充入4.0 mol CH4和 8.0 mol CO2反应,平衡后CH4的转化率
(4)CO2催化加H2可以制备CH4,保持反应气中CO2与 H2的体积比为 1∶4,以40 mL·min-1的流速通过催化剂,甲烷化过程中,含碳产物CH4的物质的量百分数(Y)及CO2的转化率随温度的变化如图所示。320℃时CO2反应速率为

您最近一年使用:0次
2022-11-27更新
|
174次组卷
|
2卷引用:广东省佛山市南海区2022-2023学年高二上学期学业水平测试化学试题
名校
解题方法
4 . 金属Zn与酸反应产生H2的反应速率最大的是
| 选项 | 温度 | 金属 | 酸 |
| A | 25℃ | Zn粒 | 0.1mol·L-1盐酸 |
| B | 50℃ | Zn粉 | 0.1mol·L-1硫酸 |
| C | 50℃ | Zn粒 | 0.1mol·L-1盐酸 |
| D | 25℃ | Zn粉 | 0.1mol·L-1硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-15更新
|
659次组卷
|
10卷引用:广东省普通高中2016-2017学年高二6月学业水平考试化学试题
广东省普通高中2016-2017学年高二6月学业水平考试化学试题【校级联考】广东省汕头市达濠华侨中学、东厦中学2018-2019学年高二(文)上学期阶段测试(二)化学试题广东省惠州市2020-2021学年高二上学期期末质量监测化学试题广东省江门市第二中学2020-2021学年高一下学期第二次月考化学试题广东省阳江市高新区2022-2023学年高二上学期1月期末考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 课时2 影响化学反应速率的因素高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时2 影响化学反应速率的因素选择性必修1 专题2 第一单元 课时2 影响化学反应速率的因素(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)江苏省无锡市运河实验中学2021-2022学年高二上学期期初考试化学试题
解题方法
5 . 在一体积不变的密闭容器中发生反应A(g)+3B(g)  2C(g)。开始反应时,A的浓度为2 mol/L。反应进行2min时,测得容器中A的浓度为1.8 mol/L,则该2min内B的平均反应速率是
2C(g)。开始反应时,A的浓度为2 mol/L。反应进行2min时,测得容器中A的浓度为1.8 mol/L,则该2min内B的平均反应速率是
 2C(g)。开始反应时,A的浓度为2 mol/L。反应进行2min时,测得容器中A的浓度为1.8 mol/L,则该2min内B的平均反应速率是
2C(g)。开始反应时,A的浓度为2 mol/L。反应进行2min时,测得容器中A的浓度为1.8 mol/L,则该2min内B的平均反应速率是| A.0.4 mol/(L•min) | B.0.3 mol/(L•min) |
| C.0.2 mol/(L•min) | D.0.1 mol/(L•min) |
您最近一年使用:0次
2021-04-21更新
|
614次组卷
|
3卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(三)
解题方法
6 . Ⅰ.影响化学反应速率的因素有多种,请在横线上填入与下列各项关系最为密切的影响化学反应速率的因素(填“温度”、“浓度”、“催化剂”、“压强”、“物质本身的性质”或“固体表面积”):
(1)夏天的食品易变霉,在冬天不易发生该现象:_______ 。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:_______ 。
(3)MnO2加入双氧水中放出气泡加快:__________ 。
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。
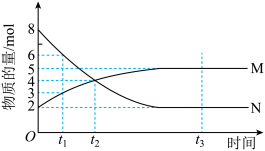
(1)比较t2时刻,正、逆反应速率大小:v(正)________ (填“>”“=”或“<”)v(逆)。
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=______ mol·L-1·min-1。
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为_________ (填“t1”“t2”或“t3”)。
(4)如果升高温度,则v(逆)________ (填“增大”“减小”或“不变”)。
(1)夏天的食品易变霉,在冬天不易发生该现象:
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:
(3)MnO2加入双氧水中放出气泡加快:
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。

(1)比较t2时刻,正、逆反应速率大小:v(正)
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为
(4)如果升高温度,则v(逆)
您最近一年使用:0次
名校
解题方法
7 . 反应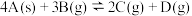 ,经过
,经过 后,B的浓度减少
后,B的浓度减少 。对此反应速率的表示正确的是( )
。对此反应速率的表示正确的是( )
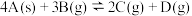 ,经过
,经过 后,B的浓度减少
后,B的浓度减少 。对此反应速率的表示正确的是( )
。对此反应速率的表示正确的是( )A.用A表示的反应速率是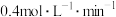 |
| B.用B、C、D表示的反应速率之比是3∶2∶1 |
C.在 末, 末, |
D.在 内,用B和C表示的反应速率的值相同 内,用B和C表示的反应速率的值相同 |
您最近一年使用:0次
2020-09-17更新
|
154次组卷
|
8卷引用:广东省潮州市潮安区龙溪中学2019-2020学年上学期普通高中学业水平测试合格考化学试题
广东省潮州市潮安区龙溪中学2019-2020学年上学期普通高中学业水平测试合格考化学试题2015-2016学年湖北省孝感高中高一下期末化学试卷甘肃省武威市第十八中学2019-2020学年高二上学期期末考试化学试题湖北省黄冈市黄梅国际育才高级中学2018-2019学年高一下学期5月月考化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率(已下线)2.1 化学反应速率(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)2.1+化学反应速率-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)北京市第五十中学2022-2023学年高二上学期期中考试化学试题
8 . 氯气是一种重要的化工原料,从氯气的发现到氯元素的确认,经历了数位科学家30多年的不懈探索,根据相关信息,回答下列问题:
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的黄绿色气体,完成该反应的化学方程式:MnO2+4HCl(浓) MnCl2+Cl2↑+
MnCl2+Cl2↑+___ 。最合理的氯气发生装置是_______ (填字母)。

(2)化学家贝托莱将Cl2的水溶液露置在阳光下,反应生成一种无色无味气体,该气体为_____ 。
(3)化学家泰耐特将Cl2通入石灰乳中,得到一种具有漂白作用的混合液。为证明该混合液的漂白作用,进行如下实验(试剂、材料等任选),完成下表中的空白。
(4)我国学者近年研究了铜基催化剂作用下的反应:4HCl+O2 2H2O+2Cl2,保持其他条件不变,温度为T1和T2时,HCl的反应速率v(HCl)随HCl的转化率
2H2O+2Cl2,保持其他条件不变,温度为T1和T2时,HCl的反应速率v(HCl)随HCl的转化率 (HCl)的变化示意图如下图所示,据图回答:
(HCl)的变化示意图如下图所示,据图回答:

①T1____ T2(填“>”、“<”、“=”);
②在同一温度下, (HCl)越大,v(HCl)越
(HCl)越大,v(HCl)越_____ (填“大”或“小”)。
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的黄绿色气体,完成该反应的化学方程式:MnO2+4HCl(浓)
 MnCl2+Cl2↑+
MnCl2+Cl2↑+
(2)化学家贝托莱将Cl2的水溶液露置在阳光下,反应生成一种无色无味气体,该气体为
(3)化学家泰耐特将Cl2通入石灰乳中,得到一种具有漂白作用的混合液。为证明该混合液的漂白作用,进行如下实验(试剂、材料等任选),完成下表中的空白。
| 实验步骤 | 实验现象 | 实验结论 |
| 取 | | 该混合液具有漂白作用 |
(4)我国学者近年研究了铜基催化剂作用下的反应:4HCl+O2
 2H2O+2Cl2,保持其他条件不变,温度为T1和T2时,HCl的反应速率v(HCl)随HCl的转化率
2H2O+2Cl2,保持其他条件不变,温度为T1和T2时,HCl的反应速率v(HCl)随HCl的转化率 (HCl)的变化示意图如下图所示,据图回答:
(HCl)的变化示意图如下图所示,据图回答:
①T1
②在同一温度下,
 (HCl)越大,v(HCl)越
(HCl)越大,v(HCl)越
您最近一年使用:0次
名校
解题方法
9 . 一定条件下反应2SO2(g)+O2(g) 2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol·L-1。则0~10s内平均反应速率为
2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol·L-1。则0~10s内平均反应速率为
 2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol·L-1。则0~10s内平均反应速率为
2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol·L-1。则0~10s内平均反应速率为| A.v(O2)=0.03mol·L-1·s-1 | B.v(O2)=0.3mol·L-1·s-1 |
| C.v(SO2)=0.03mol·L-1·s-1 | D.v(SO3)=0.03mol·L-1·s-1 |
您最近一年使用:0次
2020-06-13更新
|
418次组卷
|
9卷引用:2019年6月广东省普通高中学业水平考试化学试题
名校
解题方法
10 . 下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 | B.工业炼钢用纯氧代替空气 | C.合成氨工业中使用催化剂 | D.在加热条件下,用氢气还原氧化铜 |
您最近一年使用:0次
2019-01-30更新
|
1681次组卷
|
11卷引用:广东省2020年普通高中学业水平考试化学合格性考试模拟试题(三)
广东省2020年普通高中学业水平考试化学合格性考试模拟试题(三)广东省普通高中2020-2021学年高一学业水平合格性考试(会考)化学模拟测试卷(三)广东省乐昌市第二中学2020-2021学年高二上学期期中考试化学试题广东省梅州中学2020-2021学年高一下学期中段考试化学试题(已下线)2010-2011学年江苏省淮安五校高二上学期期末考试化学试卷山东省泰安市新泰市第一中学北校2019-2020学年高一下学期第二次阶段性考试化学试题内蒙古杭锦后旗奋斗中学2020-2021学年高二上学期期中考试化学试题福建省厦门双十中学2021-2022学年高一下学期期中考试化学试题福建省厦门双十中学2021-2022学年高一下学期期中考试化学试题福建省福州第四中学2021-2022学年高一下学期期末考试化学试题(已下线)合格考汇编13化学反应速率和限度



