解题方法
1 . 固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。某科学实验小组将6 mol CO2和8 mol H2充入2 L的恒温密闭容器中,测得H2的物质的量随时间变化如图曲线所示。a、b、c、d、e括号内数据表示坐标。________ ,该时间段内H2的平均反应速率是_______________ 。
(2)8 min时,CO2的转化率是________ ,反应前后容器内的压强比是________ 。
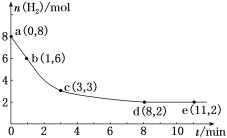
(2)8 min时,CO2的转化率是
您最近一年使用:0次
名校
解题方法
2 . 根据化学反应速率和化学反应限度的知识回答下列问题:
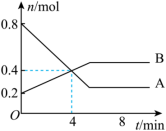
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,AB物质的量随时间变化的曲线如图所示:___________ 。
(2)反应开始至4 min时,A的平均反应速率为___________ 。
(3)4 min时,反应是否达平衡状态?___________ (填“是”或“否”),8 min时,v正___________ v逆。(填“>”“<”或“=”)
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g) ⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。___________ 。
(5)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和
8 mol氢气及固体催化剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。
①N2的转化率为___________ 。
②反应达到平衡时,放出的热量___________ (填字母,下同)。
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
(6)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为___________ 。
A.混合气体的平均相对分子质量
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的密度不变
E.断开3 mol H-H键的同时断开2 mol N-H键
(7)反应达到平衡后,保持其他条件不变,t0时刻升高温度,请在图中画出 改变条件后至达到新平衡时v正、v逆的变化曲线并注明v正、v逆(在答题卡做答)__________
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,AB物质的量随时间变化的曲线如图所示:
(2)反应开始至4 min时,A的平均反应速率为
(3)4 min时,反应是否达平衡状态?
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g) ⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。

(5)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和
8 mol氢气及固体催化剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。
①N2的转化率为
②反应达到平衡时,放出的热量
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
(6)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为
A.混合气体的平均相对分子质量
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的密度不变
E.断开3 mol H-H键的同时断开2 mol N-H键
(7)反应达到平衡后,保持其他条件不变,t0时刻升高温度,请在图中画出 改变条件后至达到新平衡时v正、v逆的变化曲线并注明v正、v逆(在答题卡做答)

您最近一年使用:0次
2024-04-30更新
|
296次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
3 . I.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(5)①本实验待测数据可以是___________ ,实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响﹔实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验发现 比实验
比实验 反应速率快,原因是
反应速率快,原因是___________ 。

 时刻,正逆反应速率大小
时刻,正逆反应速率大小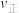
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g |  硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
 | 2.0 | 50.0 | 25 | 0 | 0 |
 | 2.0 | 40.0 | 25 | 0 | 10.0 |
 | 2.0 | 50.0 | 25 | 0.2 | 0 |
 | 2.0 | 50.0 | 35 | 0 | 0 |
(5)①本实验待测数据可以是
 和实验
和实验 可以探究
可以探究 和实验
和实验 可以探究
可以探究②实验发现
 比实验
比实验 反应速率快,原因是
反应速率快,原因是
您最近一年使用:0次
2024-04-28更新
|
319次组卷
|
2卷引用:安徽省合肥市六校联盟2023-2024学年高一下学期4月期中考试化学试题
名校
4 . 某化学研究性学习小组模拟工业合成氨的反应。在容积固定为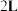 的密闭容器内充入
的密闭容器内充入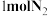 和
和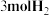 ,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
1.请写出合成氨逆反应的平衡常数表达式:___________ 。
2.反应后的气体总物质的量是___________ 。
3.则从反应开始到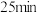 时,以
时,以 表示的平均反应速率
表示的平均反应速率
___________ 。
4.实验中, 时向容器中充入一定量
时向容器中充入一定量 ,则正反应速率
,则正反应速率___________ 。
A.增大 B.减小 C.不变
5.实验中, 时若容器体积减少一半,则平衡
时若容器体积减少一半,则平衡___________ 。
A.正向移动 B.逆向移动 C.不移动
6.改变条件能改变合成氨的反应速率,下列改变的条件中能降低反应物所需能量的是 。
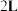 的密闭容器内充入
的密闭容器内充入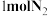 和
和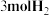 ,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:反应时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强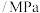 | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
2.反应后的气体总物质的量是
3.则从反应开始到
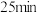 时,以
时,以 表示的平均反应速率
表示的平均反应速率
4.实验中,
 时向容器中充入一定量
时向容器中充入一定量 ,则正反应速率
,则正反应速率A.增大 B.减小 C.不变
5.实验中,
 时若容器体积减少一半,则平衡
时若容器体积减少一半,则平衡A.正向移动 B.逆向移动 C.不移动
6.改变条件能改变合成氨的反应速率,下列改变的条件中能降低反应物所需能量的是 。
| A.温度 | B.压强 | C.浓度 | D.催化剂 |
您最近一年使用:0次
5 . 试分析有关化学反应速率问题。
(1)某反应在体积为 的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知
的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知 均为气体)。
均为气体)。___________ 。
②反应开始至 时,B的平均反应速率为
时,B的平均反应速率为___________ 。
③平衡时A的转化率为___________ 。
(2)下表是某学习兴趣小组,一定条件下测定 在水溶液中分解浓度减少一半所需时间。已知:
在水溶液中分解浓度减少一半所需时间。已知: 的起始浓度为
的起始浓度为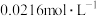 。
。
①在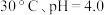 条件下,
条件下, 的分解速率为
的分解速率为___________ 。
② 增大能加速
增大能加速 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是___________ 。
③根据表中数据,推测 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为___________ (填序号)。
a.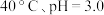 b.
b.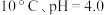 c.
c.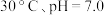
(1)某反应在体积为
 的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知
的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知 均为气体)。
均为气体)。
②反应开始至
 时,B的平均反应速率为
时,B的平均反应速率为③平衡时A的转化率为
(2)下表是某学习兴趣小组,一定条件下测定
 在水溶液中分解浓度减少一半所需时间。已知:
在水溶液中分解浓度减少一半所需时间。已知: 的起始浓度为
的起始浓度为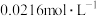 。
。
| 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
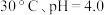 条件下,
条件下, 的分解速率为
的分解速率为②
 增大能加速
增大能加速 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是③根据表中数据,推测
 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为a.
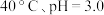 b.
b.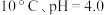 c.
c.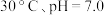
您最近一年使用:0次
名校
解题方法
6 . 在2L密闭容器中,800℃时,反应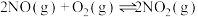 体系中,
体系中, 随时间的变化如下表所示。
随时间的变化如下表所示。
(1)图中,A点处
______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。 变化的曲线是
变化的曲线是______ ,用 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
______ 。
(3)下列能使该反应的反应速率增大的是______ 。
a.及时分离出 气体 b.适当升高温度
气体 b.适当升高温度
c.增大 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂
(4)下列能说明该反应已经达到平衡状态的是______ (填字母,下同)。
a. b.容器内压强保持不变
b.容器内压强保持不变
c. d.容器内的密度保持不变
d.容器内的密度保持不变
e.气体的总质量保持不变 f. 和
和 的物质的量之比为
的物质的量之比为
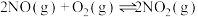 体系中,
体系中, 随时间的变化如下表所示。
随时间的变化如下表所示。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)图中,A点处

 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
 变化的曲线是
变化的曲线是 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
(3)下列能使该反应的反应速率增大的是
a.及时分离出
 气体 b.适当升高温度
气体 b.适当升高温度c.增大
 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂(4)下列能说明该反应已经达到平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.
 d.容器内的密度保持不变
d.容器内的密度保持不变e.气体的总质量保持不变 f.
 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
7 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

您最近一年使用:0次
8 . 请回答下列问题:
(1) 可发生二聚反应生成
可发生二聚反应生成 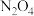 ,化学方程式为
,化学方程式为 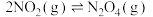 ,上述反应达到平衡后,升高温度可使体系颜色加深,则该反应的
,上述反应达到平衡后,升高温度可使体系颜色加深,则该反应的
___________ 0(填“>”或“<”)。已知该反应的正反应速率方程为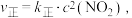 逆反应速率方程为
逆反应速率方程为 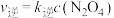 ,其中
,其中 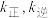 分别为正、逆反应的速率常数。则如图(
分别为正、逆反应的速率常数。则如图( 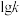 表示速率常数的对数;
表示速率常数的对数; 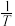 示温度的倒数)所示①、②、③、④四条斜线中,能表示
示温度的倒数)所示①、②、③、④四条斜线中,能表示 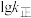 随
随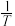 变化关系的是斜线
变化关系的是斜线___________ ,能表示 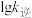 随
随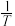 变化关系的是斜线
变化关系的是斜线___________ 。
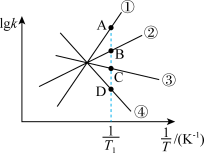
(2)图中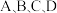 点的纵坐标分别为
点的纵坐标分别为 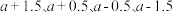 ,则温度
,则温度  时化学平衡常数K=
时化学平衡常数K=___________ mol/L。已知温度  时,某时刻恒容密闭容器中
时,某时刻恒容密闭容器中 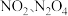 浓度均为
浓度均为 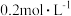 ,此时v正
,此时v正___________ v逆(填“>”“<”或“=”)。
(1)
 可发生二聚反应生成
可发生二聚反应生成 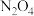 ,化学方程式为
,化学方程式为 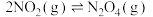 ,上述反应达到平衡后,升高温度可使体系颜色加深,则该反应的
,上述反应达到平衡后,升高温度可使体系颜色加深,则该反应的
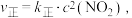 逆反应速率方程为
逆反应速率方程为 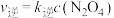 ,其中
,其中 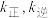 分别为正、逆反应的速率常数。则如图(
分别为正、逆反应的速率常数。则如图( 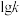 表示速率常数的对数;
表示速率常数的对数; 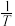 示温度的倒数)所示①、②、③、④四条斜线中,能表示
示温度的倒数)所示①、②、③、④四条斜线中,能表示 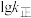 随
随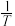 变化关系的是斜线
变化关系的是斜线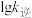 随
随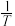 变化关系的是斜线
变化关系的是斜线
(2)图中
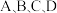 点的纵坐标分别为
点的纵坐标分别为 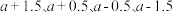 ,则温度
,则温度  时化学平衡常数K=
时化学平衡常数K= 时,某时刻恒容密闭容器中
时,某时刻恒容密闭容器中 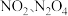 浓度均为
浓度均为 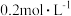 ,此时v正
,此时v正
您最近一年使用:0次
名校
解题方法
9 . 氨和铵盐用途广泛。
(1)工业合成氨的反应是 N2+3H2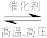 2NH3 。
2NH3 。
① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,___________
b.平衡时NH3的体积分数___________ 。(写出计算过程)
② 对上述反应,下列说法不正确的是___________
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是___________ ,负极是___________ 。当生成25.5克NH3时,转移___________ mol电子。
(1)工业合成氨的反应是 N2+3H2
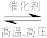 2NH3 。
2NH3 。① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,
b.平衡时NH3的体积分数
② 对上述反应,下列说法不正确的是
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH
 + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
您最近一年使用:0次
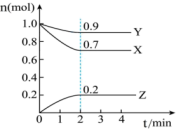
10 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。___________ ;
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为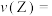
___________ ;
(3)2min反应达到平衡时体系内的压强比起始时的压强___________ (填增大、减小或无变化);平衡时混合气体密度和起始时相比___________ 。(填增大、减小或无变化)
(4)下列措施能加快反应速率的是___________。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为
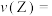
(3)2min反应达到平衡时体系内的压强比起始时的压强
(4)下列措施能加快反应速率的是___________。
| A.升高温度 | B.选择高效的催化剂 | C.恒容时充入X | D.恒容时充入氩气 |
您最近一年使用:0次