名校
1 . 硫酸是重要的化工原料,工业制硫酸的其中一步重要反应是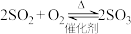 ,正反应放热。一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。
,正反应放热。一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。 的平均反应速率为
的平均反应速率为___________ 。
(2)图中a点,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(3)反应进行到第___________ 分钟时恰好达到平衡,此时 的转化率为
的转化率为___________ 。
(4)下列说法正确的是___________。
(5)硫酸厂产生的尾气中含有少量 。双碱法脱硫的原理示意图如下:
。双碱法脱硫的原理示意图如下:___________ ,过程I的离子方程式为___________ 。
②理论上,过程 中消耗1mol氧气时,过程I中吸收
中消耗1mol氧气时,过程I中吸收 的体积(标准状况)是
的体积(标准状况)是___________ L。
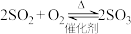 ,正反应放热。一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。
,正反应放热。一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。
 的平均反应速率为
的平均反应速率为(2)图中a点,正反应速率
(3)反应进行到第
 的转化率为
的转化率为(4)下列说法正确的是___________。
A.反应过程中, 和 和 的转化率始终相等 的转化率始终相等 |
B.通过调控反应条件,可以实现 的完全转化 的完全转化 |
| C.其他条件不变,升高温度,正反应速率和逆反应速率均增大 |
| D.使用催化剂可以提高反应速率,提高生产效率 |
(5)硫酸厂产生的尾气中含有少量
 。双碱法脱硫的原理示意图如下:
。双碱法脱硫的原理示意图如下:
②理论上,过程
 中消耗1mol氧气时,过程I中吸收
中消耗1mol氧气时,过程I中吸收 的体积(标准状况)是
的体积(标准状况)是
您最近一年使用:0次
解题方法
2 . 按要求回答下列问题:
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
(2)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应(反应物、产物均为气体),反应中各物质物质的量的变化如图所示。___________ 。
②在0~6s内,B的平均反应速率为___________ 。
③6s后容器内的压强与开始时压强之比为___________ 。
(3)已知CH3OCH3的结构式为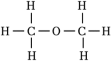 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 ___________ (填字母)。
a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
| A.甲烷的燃烧 |
| B.CO2通入灼热的炭层 |
| C.石灰石受热分解 |
| D.碘升华 |

②在0~6s内,B的平均反应速率为
③6s后容器内的压强与开始时压强之比为
(3)已知CH3OCH3的结构式为
 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
您最近一年使用:0次
解题方法
3 . 一定温度下,在 的密闭容器中,
的密闭容器中, 两种气体的物质的量随时间变化的曲线如图所示:
两种气体的物质的量随时间变化的曲线如图所示:_______ 。
(2)反应达到最大限度的时间是______  ,该时间内的平均反应速率
,该时间内的平均反应速率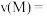
______ 。
(3)判断该反应达到平衡状态的依据是_______。
(4)能加快反应速率的措施是_______。
(5)反应进行到4min时,N的转化率为_______ 。
 的密闭容器中,
的密闭容器中, 两种气体的物质的量随时间变化的曲线如图所示:
两种气体的物质的量随时间变化的曲线如图所示: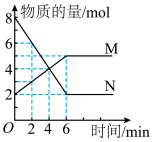
(2)反应达到最大限度的时间是
 ,该时间内的平均反应速率
,该时间内的平均反应速率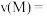
(3)判断该反应达到平衡状态的依据是_______。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
D.该条件下,单位时间内消耗 的同时,消耗 的同时,消耗 |
(4)能加快反应速率的措施是_______。
| A.升高温度 |
B.容器容积不变,充入惰性气体 |
C.容器压强不变,充入惰性气体 |
| D.使用催化剂 |
(5)反应进行到4min时,N的转化率为
您最近一年使用:0次
名校
解题方法
4 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为CO和 ),其反应的化学方程式为
),其反应的化学方程式为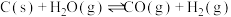 ,请回答下列问题:
,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是_______。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是_______。
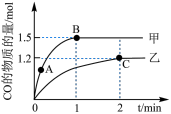
(3)在体积均为2L的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和2.8mol水蒸气,在不同温度下反应的过程如图所示:
_______ 。
②甲容器中,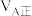
_______ 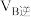 (填“<”“>”或“=”下同)。
(填“<”“>”或“=”下同)。
③反应过程中,两个容器温度:甲_______ 乙。
(4)乙容器中C点时,CO的物质的量百分数为_______ 。
 ),其反应的化学方程式为
),其反应的化学方程式为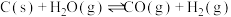 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是_______。

| A.铝粉与氧化铁的反应 | B.氯化铵与 的反应 的反应 |
| C.锌片与稀硫酸的反应 | D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是_______。
| A.充入He使容器压强增大,提高反应速率 |
B.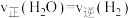 ,说明反应达到平衡状态 ,说明反应达到平衡状态 |
| C.容器中焦炭的质量不再变化,说明反应达到平衡状态 |
D.容器中水蒸气与氢气的体积比为 时,说明反应达到平衡状态 时,说明反应达到平衡状态 |
(3)在体积均为2L的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和2.8mol水蒸气,在不同温度下反应的过程如图所示:

②甲容器中,
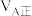
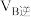 (填“<”“>”或“=”下同)。
(填“<”“>”或“=”下同)。③反应过程中,两个容器温度:甲
(4)乙容器中C点时,CO的物质的量百分数为
您最近一年使用:0次
2024-05-03更新
|
278次组卷
|
2卷引用:广东省东莞市东华高级中学2023-2024学年高一下学期前段考试化学试题
名校
解题方法
5 . 峨眉金顶摄身崖又称舍身崖,因常现佛光而得名。“佛光”因摄入身之影像于其中,遂称“摄身光”,为峨眉胜景之一、摄身崖下土壤中富含磷矿,所以在无月的黑夜可见到崖下荧光无数。
(1)“荧光”主要成分是PH3,其中心原子的价层电子对数为____ ,下列有关PH3的说法错误 的是____ 。
A.PH3分子是极性分子
B.PH3分子稳定性低于 NH3分子,因为N−H键键能高
C.一个 PH3分子中,P原子核外有一对孤电子对
D.PH3沸点低于NH3沸点,因P−H键键能低
(2)“荧光”产生的原理是Ca3P2在潮湿的空气中剧烈反应,写出该反应的化学方程式_______ 。
(3)已知下列键能数据及P4(白磷)分子结构:
则反应4PH3(g) P4(g)+6H2(g) ΔH=
P4(g)+6H2(g) ΔH=______ kJ/mol。
(4)某温度下,向容积为2L的密闭容器中通入2molPH3发生(3)中反应,5min后反应达平衡,测得此时H2的物质的量为1.5 mol,则用PH3表示的这段时间内的化学反应速率v(PH3)=____ ;下列说法能表明该反应达到平衡状态的是____ 。
A.混合气体的密度不变 B.6v(PH3) = 4v(H2)
C.c(PH3):c(P4):c(H2) = 4:1:6 D.混合气体的压强不变
(1)“荧光”主要成分是PH3,其中心原子的价层电子对数为
A.PH3分子是极性分子
B.PH3分子稳定性低于 NH3分子,因为N−H键键能高
C.一个 PH3分子中,P原子核外有一对孤电子对
D.PH3沸点低于NH3沸点,因P−H键键能低
(2)“荧光”产生的原理是Ca3P2在潮湿的空气中剧烈反应,写出该反应的化学方程式
(3)已知下列键能数据及P4(白磷)分子结构:
| 化学键 | P−P | H−H | P−H | 分子结构 |
| 键能(kJ∙mol−1) | 213 | 436 | 322 |
|
 P4(g)+6H2(g) ΔH=
P4(g)+6H2(g) ΔH=(4)某温度下,向容积为2L的密闭容器中通入2molPH3发生(3)中反应,5min后反应达平衡,测得此时H2的物质的量为1.5 mol,则用PH3表示的这段时间内的化学反应速率v(PH3)=
A.混合气体的密度不变 B.6v(PH3) = 4v(H2)
C.c(PH3):c(P4):c(H2) = 4:1:6 D.混合气体的压强不变
您最近一年使用:0次
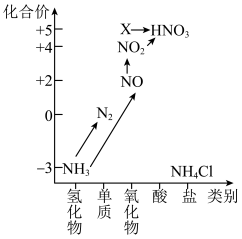
6 . 依据图中氮元素及其化合物的转化关系,回答下列问题:______ 。
(2)回答下列关于 的问题:
的问题:
①利用下列方法制氨气,其中合理的是______ (填字母)。
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:______ 。
③ 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是______ 。
A. B.
B.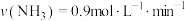
C.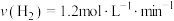 D.
D.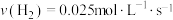
(3)下列关于NO、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:______ 。
②NO和 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:______ 。
(2)回答下列关于
 的问题:
的问题:①利用下列方法制氨气,其中合理的是
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
③
 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是A.
 B.
B.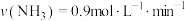
C.
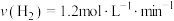 D.
D.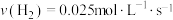
(3)下列关于NO、
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和
 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
您最近一年使用:0次
解题方法
7 . 回答下列问题:
(1)一定温度下,反应 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
①缩小体积使压强增大:________ ;②恒容充入 :
:________ ;③恒压充入He:________ 。
(2)在恒温恒容条件下,可逆反应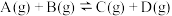 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为________ (填正确选项前的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.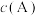 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
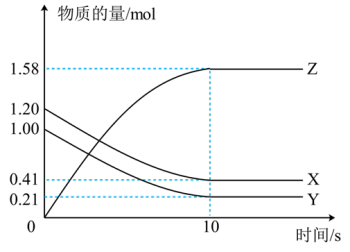
①从反应开始到10s时,用Z表示的反应速率为________ ,X的物质的量浓度减少了________ ,Y的转化率为________ 。
②该反应的化学方程式为________ 。
(1)一定温度下,反应
 在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)
在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”“减小”或“不变”)①缩小体积使压强增大:
 :
:(2)在恒温恒容条件下,可逆反应
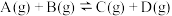 。判断该反应是否达到平衡的依据为
。判断该反应是否达到平衡的依据为a.压强不随时间改变 b.气体的密度不随时间改变
c.
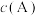 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等(3)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

①从反应开始到10s时,用Z表示的反应速率为
②该反应的化学方程式为
您最近一年使用:0次
名校
8 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
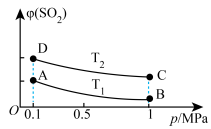
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
(4)已知反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
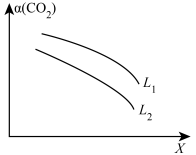
①X表示的物理量是___________ 。
②L1___________ L2(填“<”或“>”),判断理由是___________ 。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

(4)已知反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
①X表示的物理量是
②L1
您最近一年使用:0次
名校
解题方法
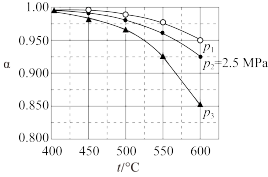
9 . 硫酸是一种重要的基础化工产品,接触法制硫酸生产中的关键工序是 的催化氧化:
的催化氧化: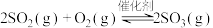
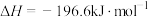 。回答下列问题。
。回答下列问题。
(1)某温度下,在体积为 的刚性密闭容器中投入
的刚性密闭容器中投入 和
和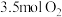 ,下图是
,下图是 和
和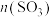 随时间的变化曲线。
随时间的变化曲线。

① ,
,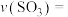
___________ 。
②反应达到平衡时,平衡常数
___________  。(保留3位有效数字)
。(保留3位有效数字)
③下列情况不能说明反应达到化学平衡状态的是___________ 。
A. B.混合气体的相对分子质量不再变化
B.混合气体的相对分子质量不再变化
C.体系的压强不再发生改变 D.混合气体的密度保持不变
(2)下表列出了在不同温度和压强下,反应达到平衡时 的转化率。
的转化率。
①仅从表中数据可得出最优的条件是___________ 。
②在实际生产中,选定的温度为400~500℃和常压(0.1MPa),原因是___________ 。
(3)当 、
、 和
和 起始的物质的量分数分别为7.5%、10.5%和82%时,在
起始的物质的量分数分别为7.5%、10.5%和82%时,在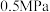 、
、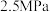 和
和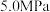 压强下,
压强下, 平衡转化率
平衡转化率 随温度的变化如下图所示。反应在
随温度的变化如下图所示。反应在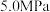 、550℃时的
、550℃时的
___________ ,影响 的因素有温度、压强和
的因素有温度、压强和___________ 。
 的催化氧化:
的催化氧化: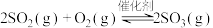
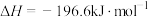 。回答下列问题。
。回答下列问题。(1)某温度下,在体积为
 的刚性密闭容器中投入
的刚性密闭容器中投入 和
和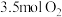 ,下图是
,下图是 和
和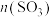 随时间的变化曲线。
随时间的变化曲线。
①
 ,
,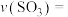
②反应达到平衡时,平衡常数

 。(保留3位有效数字)
。(保留3位有效数字)③下列情况不能说明反应达到化学平衡状态的是
A.
 B.混合气体的相对分子质量不再变化
B.混合气体的相对分子质量不再变化C.体系的压强不再发生改变 D.混合气体的密度保持不变
(2)下表列出了在不同温度和压强下,反应达到平衡时
 的转化率。
的转化率。| 温度/℃ | 平衡时 的转化率/% 的转化率/% | ||||
 | 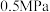 |  |  | 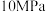 | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
②在实际生产中,选定的温度为400~500℃和常压(0.1MPa),原因是
(3)当
 、
、 和
和 起始的物质的量分数分别为7.5%、10.5%和82%时,在
起始的物质的量分数分别为7.5%、10.5%和82%时,在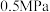 、
、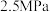 和
和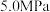 压强下,
压强下, 平衡转化率
平衡转化率 随温度的变化如下图所示。反应在
随温度的变化如下图所示。反应在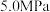 、550℃时的
、550℃时的
 的因素有温度、压强和
的因素有温度、压强和
您最近一年使用:0次
名校
10 .  年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
(1)已知:I. ;
;
II.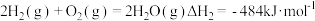 。
。
在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式 ∆H=
∆H= ___________ kJ∙mol-1。
(2) 时,将
时,将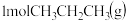 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: 。用压强传感器测出容器内体系压强随时间的变化关系如图
。用压强传感器测出容器内体系压强随时间的变化关系如图 所示:
所示:
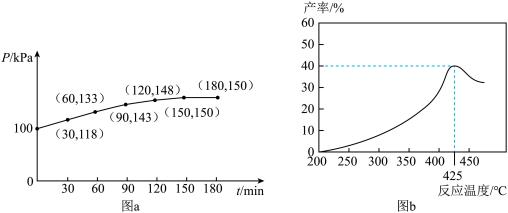
①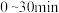 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为___________ 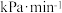 。
。
②保持相同反应时间,在不同温度下,丙烯产率如图 所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
所示,丙烯产率在425℃之前随温度升高而增大的原因可能是___________ 或___________ 。425℃之后,丙烯产率快速降低的主要原因可能是___________ (任写一点)。
 年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:(1)已知:I.
 ;
;II.
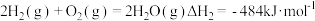 。
。在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式
 ∆H=
∆H= (2)
 时,将
时,将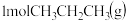 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: 。用压强传感器测出容器内体系压强随时间的变化关系如图
。用压强传感器测出容器内体系压强随时间的变化关系如图 所示:
所示:
①
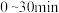 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为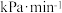 。
。②保持相同反应时间,在不同温度下,丙烯产率如图
 所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
您最近一年使用:0次




