名校
解题方法
1 . 汞及其化合物在催化、科学研究等方面具有重要应用。
(1)HgO可作为光催化剂降解有机染料污染物(如罗丹明B,以下简称B)。
①在三组100mL12mg•L-1的B溶液中分别加入0.075gHgO,在不同波长的可见光照射下做光催化活性测试,溶液中某时刻B的浓度c与初始浓度c0的比值随光照时间t的变化如下图所示,三条曲线产生差异的原因可能是___________ 。___________ mg•L-1•min-1。
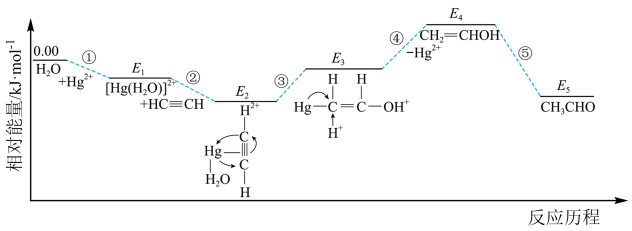
(2)乙炔(HC≡CH)能在汞盐溶液催化下与水反应生成CH3CHO,反应历程及相对能垒如下图所示。___________ (用相对能量E表示)。
②下列说法正确的是___________ 。
A.本反应历程涉及的物质中,CH2=CHOH最不稳定
B.过程①中,Hg2+的空轨道接受水分子中氧原子的孤对电子
C.该反应历程中,存在非极性键的断裂和形成
D.增大压强和乙炔的浓度均能加快反应速率,并且增大乙炔的平衡转化率
(3)常温下,Hg2+与Cl-的配合物存在如下平衡:HgCl
 HgCl
HgCl
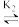 HgCl2
HgCl2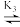 HgCl+
HgCl+ Hg2+,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
Hg2+,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示: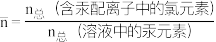
①图中能代表HgCl2曲线是___________ (填字母),平衡常数K4=___________ 。
②在P点,溶液中c(HgCl2):c(Hg2+)=___________ (写出计算过程)。
(1)HgO可作为光催化剂降解有机染料污染物(如罗丹明B,以下简称B)。
①在三组100mL12mg•L-1的B溶液中分别加入0.075gHgO,在不同波长的可见光照射下做光催化活性测试,溶液中某时刻B的浓度c与初始浓度c0的比值随光照时间t的变化如下图所示,三条曲线产生差异的原因可能是

(2)乙炔(HC≡CH)能在汞盐溶液催化下与水反应生成CH3CHO,反应历程及相对能垒如下图所示。
②下列说法正确的是
A.本反应历程涉及的物质中,CH2=CHOH最不稳定
B.过程①中,Hg2+的空轨道接受水分子中氧原子的孤对电子
C.该反应历程中,存在非极性键的断裂和形成
D.增大压强和乙炔的浓度均能加快反应速率,并且增大乙炔的平衡转化率
(3)常温下,Hg2+与Cl-的配合物存在如下平衡:HgCl

 HgCl
HgCl
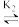 HgCl2
HgCl2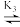 HgCl+
HgCl+ Hg2+,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
Hg2+,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
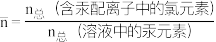
①图中能代表HgCl2曲线是
②在P点,溶液中c(HgCl2):c(Hg2+)=
您最近一年使用:0次
2 . 化学在生产生活中无处不在。
 .某汽车安全气囊的气体发生剂主要含有叠氮化钠(
.某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、三氧化二铁(
)、三氧化二铁( )、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是___________ (填字母),生成氮气的电子式为___________ 。 .
. 、
、 (甲醇)既是重要的化工原料,又是重要的能源物质。
(甲醇)既是重要的化工原料,又是重要的能源物质。
(2)将2.0 mol 和4.0 mol
和4.0 mol  通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应
通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应 ,测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用
,测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为___________ 。
(3)一定条件下,将1.0 mol 与2.0 mol
与2.0 mol  充入密闭容器中发生反应
充入密闭容器中发生反应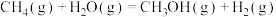 ,下列措施可以提高化学反应速率的是
,下列措施可以提高化学反应速率的是___________ (填字母)。
a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的 e.加入合适的催化剂
e.加入合适的催化剂
(4)用 设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为
设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为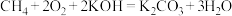 。
。 向B电极定向移动,则
向B电极定向移动,则___________ (填“A”或“B”)电极入口通甲烷,该电极反应的离子方程式为___________ 。
②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为___________ 。
 .某汽车安全气囊的气体发生剂主要含有叠氮化钠(
.某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、三氧化二铁(
)、三氧化二铁( )、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。(1)汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是A.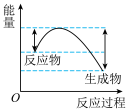 B.
B.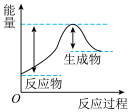 C.
C.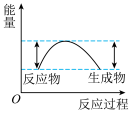
 .
. 、
、 (甲醇)既是重要的化工原料,又是重要的能源物质。
(甲醇)既是重要的化工原料,又是重要的能源物质。(2)将2.0 mol
 和4.0 mol
和4.0 mol  通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应
通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应 ,测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用
,测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为(3)一定条件下,将1.0 mol
 与2.0 mol
与2.0 mol  充入密闭容器中发生反应
充入密闭容器中发生反应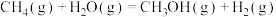 ,下列措施可以提高化学反应速率的是
,下列措施可以提高化学反应速率的是a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的
 e.加入合适的催化剂
e.加入合适的催化剂(4)用
 设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为
设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为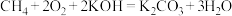 。
。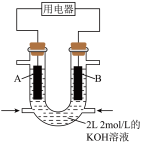
 向B电极定向移动,则
向B电极定向移动,则②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为
您最近一年使用:0次
名校
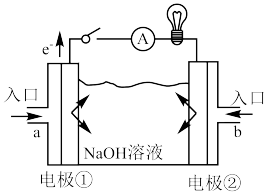
3 . 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:___________ ,Y的转化率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:___________ (填“增大”、“减小”或“不变”,下同)。
B.继续通入一定量的He:___________ 。
(5)下列图像或实验属于放热反应的是___________ (填序号)。___________ (填物质名称),负极的电极反应式为___________ 。

(2)该反应的化学方程式为
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
| A.容器内气体质量不再发生变化 |
| B.容器内气体压强不再发生变化 |
| C.X的体积分数不再改变 |
| D.容器内混合气体的密度不再发生变化 |
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:
B.继续通入一定量的He:
(5)下列图像或实验属于放热反应的是

您最近一年使用:0次
名校
解题方法
4 . 回答下列问题。
(1)治理大气中的 以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①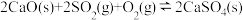
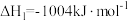
②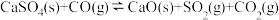
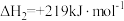
则 的燃烧热为
的燃烧热为___________  。
。
(2)一定条件下铁可以和 发生反应:
发生反应: 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如图所示。
气体的浓度与时间的关系如图所示。 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。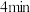 内,
内, 的平均反应速率
的平均反应速率
___________ 。
②下列描述能说明上述反应已达到平衡状态的是___________ (填序号)。
A.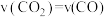
B.单位时间内生成 ,的同时生成
,的同时生成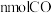
C.容器中气体压强不随时间变化而变化
D.容器中气体的平均相对分子质量不随时间变化而变化
E. 和
和 浓度相等
浓度相等
(3)某温度下在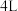 密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:___________ 。
②平衡时,混合气体中X、Y、Z的体积比为___________ 。
(1)治理大气中的
 以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
以及废水中的硫化物是环境保护的重要课题。加入固硫剂,是一种有效的治理措施。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:①
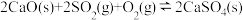
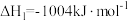
②
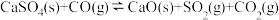
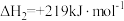
则
 的燃烧热为
的燃烧热为 。
。(2)一定条件下铁可以和
 发生反应:
发生反应: 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如图所示。
气体的浓度与时间的关系如图所示。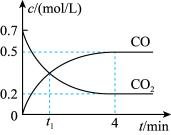
 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。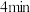 内,
内, 的平均反应速率
的平均反应速率
②下列描述能说明上述反应已达到平衡状态的是
A.
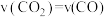
B.单位时间内生成
 ,的同时生成
,的同时生成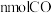
C.容器中气体压强不随时间变化而变化
D.容器中气体的平均相对分子质量不随时间变化而变化
E.
 和
和 浓度相等
浓度相等(3)某温度下在
 密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
②平衡时,混合气体中X、Y、Z的体积比为
您最近一年使用:0次
名校
解题方法
5 . Ⅰ.铁是生产生活、科学研究中的重要物质,研究与Fe相关的反应时要关注反应的快慢和程度,某些有铁参与的反应可设计成原电池。
(1)以下是相同条件下,等体积等浓度的H2O2溶液分解的对比实验时,放出 O2的体积随时间的变化关系示意图(线a为使用FeCl3作催化剂,线b为不使用催化剂),其中正确的图像是______(填字母)。
Ⅱ.已知下列热化学为程式:
①Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H1=﹣25 kJ·mol-1
②Fe2O3(s)+CO(g) = 2FeO(s)+CO2(g) △H2=﹣3 kJ·mol-1
(2)写出Fe被CO2氧化成FeO(s) 和 CO的热化学方程式_______ 。
一定温度下,向某密闭容器中加入足量铁并充入一定量的CO2气体,发生第(2)题的反应。反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。_____ v逆(CO2)(填“>”“<”或“=”)。
(4)0~4min内, CO的平均反应速率v(CO)=____ 。
(5)仅改变下列条件,化学反应速率减小的是___ (填字母)。
A.减少铁的质量 B.降低温度 C.保持压强不变,充入He使容器的体积增大
Ⅲ.某化学兴趣小组利用反应Cu + 2FeCl3 = CuCl2 + 2FeCl2,设计了如图所示的原电池装置。___ 极(填“正”或“负”),。
(7)写出b电极上的电极反应式______ 。
(1)以下是相同条件下,等体积等浓度的H2O2溶液分解的对比实验时,放出 O2的体积随时间的变化关系示意图(线a为使用FeCl3作催化剂,线b为不使用催化剂),其中正确的图像是______(填字母)。
A. | B.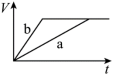 |
C.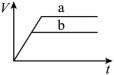 | D.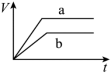 |
Ⅱ.已知下列热化学为程式:
①Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H1=﹣25 kJ·mol-1
②Fe2O3(s)+CO(g) = 2FeO(s)+CO2(g) △H2=﹣3 kJ·mol-1
(2)写出Fe被CO2氧化成FeO(s) 和 CO的热化学方程式
一定温度下,向某密闭容器中加入足量铁并充入一定量的CO2气体,发生第(2)题的反应。反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。
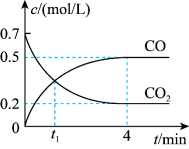
(4)0~4min内, CO的平均反应速率v(CO)=
(5)仅改变下列条件,化学反应速率减小的是
A.减少铁的质量 B.降低温度 C.保持压强不变,充入He使容器的体积增大
Ⅲ.某化学兴趣小组利用反应Cu + 2FeCl3 = CuCl2 + 2FeCl2,设计了如图所示的原电池装置。
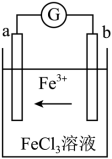
(7)写出b电极上的电极反应式
您最近一年使用:0次
6 . 碳单质及其化合物广泛存在于人们的生产和生活中。研究碳单质及其化合物的结构、性质、转化是科技工作者的研究热点。
(1)实验室常用邻二氮菲检验亚铁离子,生成橙红色的邻二氮菲亚铁络离子X: 的最外层电子排布式是
的最外层电子排布式是________________ 。
②X中除含共价键外,还含配位键, X含
X含________ mol配位键。
(2)温度为T时,在恒容密闭容器中充入一定量的 和
和 混合气体,发生反应:
混合气体,发生反应:

 。
。
已知该反应存在: ,
,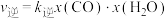 ,其中
,其中 、
、 为速率常数,x为相关物质的物质的量分数。反应达到平衡时,若
为速率常数,x为相关物质的物质的量分数。反应达到平衡时,若 、
、 转化率均为60%,且该反应的
转化率均为60%,且该反应的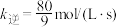 ,则
,则
________ 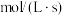 ,压强平衡常数
,压强平衡常数
________ 。
(3)氧化锰八面体分子筛(简称OMS-2)是一种纳米级别的新型环保催化剂,对挥发性有机物(VOCs)的氧化去除有着很好的催化作用。如用OMS-2为催化剂( 为对比催化实验)氧化处理甲醛的反应生成
为对比催化实验)氧化处理甲醛的反应生成 、
、 ,在等时间内HCHO转化率随温度的变化关系如图所示。
,在等时间内HCHO转化率随温度的变化关系如图所示。 、
、 反应的化学方程式是
反应的化学方程式是________________________ 。
②下列有关说法中,正确的有________ 。
A.相比 ,OMS-2能提高甲醛氧化的平衡转化率
,OMS-2能提高甲醛氧化的平衡转化率
B.OMS-2能降低甲醛氧化反应的活化能
C.OMS-2作为纳米材料,表面积大,催化效果好
D.两种催化剂的平衡转化率均随温度的升高而增大
(4)以合成气( 、
、 )为原料合成乙二醇的反应:
)为原料合成乙二醇的反应:
反应ⅰ.
反应ⅱ.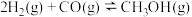
温度为473K,在恒容(2.0L)密闭容器中充入一定量的合成气(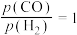 ,测得体系总压为40MPa),在
,测得体系总压为40MPa),在 (其中含
(其中含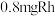 )催化剂作用下,进行上述反应。测得
)催化剂作用下,进行上述反应。测得 的时空收率为
的时空收率为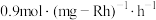 ,反应速率
,反应速率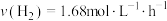 。
。
【注】(催化剂)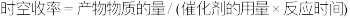 。
。
①反应速率
________  。
。
②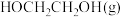 的时空收率为
的时空收率为________ 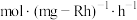 。
。
(1)实验室常用邻二氮菲检验亚铁离子,生成橙红色的邻二氮菲亚铁络离子X:

 的最外层电子排布式是
的最外层电子排布式是②X中除含共价键外,还含配位键,
 X含
X含(2)温度为T时,在恒容密闭容器中充入一定量的
 和
和 混合气体,发生反应:
混合气体,发生反应:
 。
。已知该反应存在:
 ,
,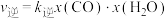 ,其中
,其中 、
、 为速率常数,x为相关物质的物质的量分数。反应达到平衡时,若
为速率常数,x为相关物质的物质的量分数。反应达到平衡时,若 、
、 转化率均为60%,且该反应的
转化率均为60%,且该反应的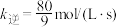 ,则
,则
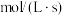 ,压强平衡常数
,压强平衡常数
(3)氧化锰八面体分子筛(简称OMS-2)是一种纳米级别的新型环保催化剂,对挥发性有机物(VOCs)的氧化去除有着很好的催化作用。如用OMS-2为催化剂(
 为对比催化实验)氧化处理甲醛的反应生成
为对比催化实验)氧化处理甲醛的反应生成 、
、 ,在等时间内HCHO转化率随温度的变化关系如图所示。
,在等时间内HCHO转化率随温度的变化关系如图所示。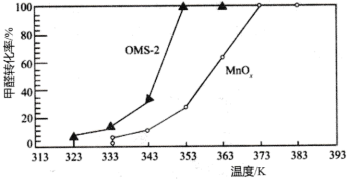
 、
、 反应的化学方程式是
反应的化学方程式是②下列有关说法中,正确的有
A.相比
 ,OMS-2能提高甲醛氧化的平衡转化率
,OMS-2能提高甲醛氧化的平衡转化率B.OMS-2能降低甲醛氧化反应的活化能
C.OMS-2作为纳米材料,表面积大,催化效果好
D.两种催化剂的平衡转化率均随温度的升高而增大
(4)以合成气(
 、
、 )为原料合成乙二醇的反应:
)为原料合成乙二醇的反应:反应ⅰ.

反应ⅱ.
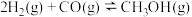
温度为473K,在恒容(2.0L)密闭容器中充入一定量的合成气(
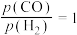 ,测得体系总压为40MPa),在
,测得体系总压为40MPa),在 (其中含
(其中含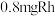 )催化剂作用下,进行上述反应。测得
)催化剂作用下,进行上述反应。测得 的时空收率为
的时空收率为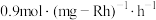 ,反应速率
,反应速率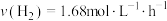 。
。【注】(催化剂)
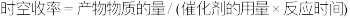 。
。①反应速率

 。
。②
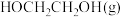 的时空收率为
的时空收率为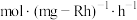 。
。
您最近一年使用:0次
7 . 工业合成氨是人类科学技术的一项重大突破,选择高效催化剂实现降能提效是目前研究的重点。回答下列问题:
(1)合成氨反应为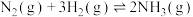
 ,理论上
,理论上___________ (填“高”或“低”,下同)温有利于提高反应速率,___________ 温有利于提高平衡转化率。
(2)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
①写出 参与化学吸附的反应方程式:
参与化学吸附的反应方程式:___________ 。
②以上历程须克服的最大能垒为___________ eV。
(3)在t℃、压强为0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示: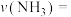
___________  ,该反应的
,该反应的
___________ (用数字表达式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是___________ (填标号)。
a.氨气的体积分数保持不变 b.容器中氢氮比保持不变
c. 和
和 的平均反应速率之比为1∶2 d.气体密度保持不变
的平均反应速率之比为1∶2 d.气体密度保持不变
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中___________ (填“d”“e”“f”或“g”)点。
(1)合成氨反应为
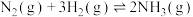
 ,理论上
,理论上(2)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
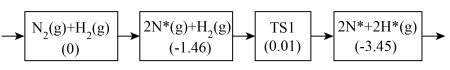
①写出
 参与化学吸附的反应方程式:
参与化学吸附的反应方程式:②以上历程须克服的最大能垒为
(3)在t℃、压强为0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
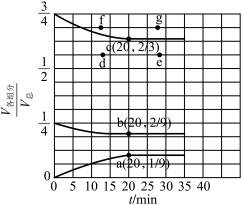
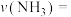
 ,该反应的
,该反应的
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。②下列叙述能说明该条件下反应达到平衡状态的是
a.氨气的体积分数保持不变 b.容器中氢氮比保持不变
c.
 和
和 的平均反应速率之比为1∶2 d.气体密度保持不变
的平均反应速率之比为1∶2 d.气体密度保持不变③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
您最近一年使用:0次
解题方法
8 . 船舶柴油机发动机工作时,反应产生的 尾气是空气主要污染物之一,研究
尾气是空气主要污染物之一,研究 的转化方法和机理具有重要意义。
的转化方法和机理具有重要意义。
已知: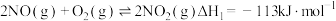 ;
; ;
;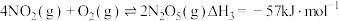
(1) 氧化脱除
氧化脱除 的总反应是
的总反应是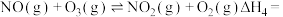
_______ 。
(2)该反应过程有两步: ,反应中各物质浓度变化如图所示。则速率常数
,反应中各物质浓度变化如图所示。则速率常数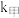
_______  (填“
(填“ ”、“
”、“ ”或“
”或“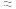 ”),原因是
”),原因是 _______ 。  的反应历程分两步:
的反应历程分两步:
①则反应Ⅰ与反应Ⅱ的活化能:
_______ 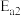 (填“
(填“ ”“
”“ ”或“
”或“ ”)。反应
”)。反应 的平衡常数
的平衡常数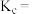
_______ (用 、
、 、
、 、
、 表示)。
表示)。
②在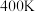 、初始压强为
、初始压强为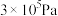 的恒温刚性容器(体积为VL)中,按
的恒温刚性容器(体积为VL)中,按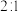 通入
通入 和
和 一定条件下发生反应。达平衡时
一定条件下发生反应。达平衡时 转化率为
转化率为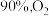 转化率为
转化率为
____________ 。
(4)某研究小组将 、
、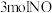 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生反应
催化剂表面发生反应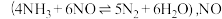 的转化率随温度的变化情况如图所示:
的转化率随温度的变化情况如图所示: 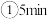 内温度从
内温度从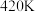 升高到
升高到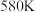 ,此时段内
,此时段内 的平均反应速率
的平均反应速率
_______ (保留 位有效数字)。
位有效数字)。
②无氧条件下, 生成
生成 的转化率较低,原因可能是
的转化率较低,原因可能是 _______ 。
 尾气是空气主要污染物之一,研究
尾气是空气主要污染物之一,研究 的转化方法和机理具有重要意义。
的转化方法和机理具有重要意义。 已知:
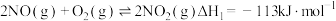 ;
; ;
;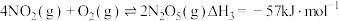
(1)
 氧化脱除
氧化脱除 的总反应是
的总反应是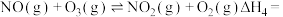
(2)该反应过程有两步:
 ,反应中各物质浓度变化如图所示。则速率常数
,反应中各物质浓度变化如图所示。则速率常数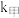
 (填“
(填“ ”、“
”、“ ”或“
”或“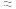 ”),原因是
”),原因是 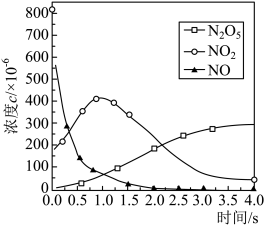
 的反应历程分两步:
的反应历程分两步: | 步骤 | 反应 | 活化能 | 正反应速率方程 | 逆反应速率方程 |
| Ⅰ |  (快) (快) |  | 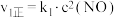 | 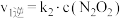 |
| Ⅱ | 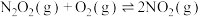 (慢) | 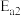 | 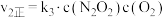 |  |

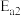 (填“
(填“ ”“
”“ ”或“
”或“ ”)。反应
”)。反应 的平衡常数
的平衡常数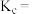
 、
、 、
、 、
、 表示)。
表示)。 ②在
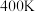 、初始压强为
、初始压强为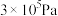 的恒温刚性容器(体积为VL)中,按
的恒温刚性容器(体积为VL)中,按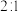 通入
通入 和
和 一定条件下发生反应。达平衡时
一定条件下发生反应。达平衡时 转化率为
转化率为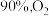 转化率为
转化率为
(4)某研究小组将
 、
、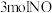 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生反应
催化剂表面发生反应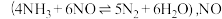 的转化率随温度的变化情况如图所示:
的转化率随温度的变化情况如图所示: 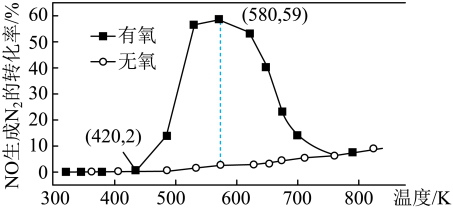
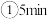 内温度从
内温度从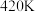 升高到
升高到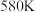 ,此时段内
,此时段内 的平均反应速率
的平均反应速率
 位有效数字)。
位有效数字)。 ②无氧条件下,
 生成
生成 的转化率较低,原因可能是
的转化率较低,原因可能是
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应_______ (填“吸收”或“放出”)_______ kJ能量(用含有a、b的关系式表示)。 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=_______ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为_______ 。
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(4)该实验探究的是_______ 因素对化学反应速率的影响。如下图一,相同时间内针筒中所得的CO2体积大小关系是_______ (填实验序号)。 =
=_______ (假设混合液体积为50mL)。
(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______ 。
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应
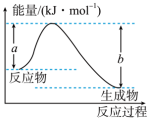
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
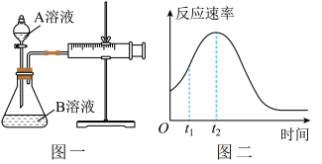
 =
=(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
您最近一年使用:0次
2024-04-25更新
|
192次组卷
|
2卷引用:广东省汕头市潮阳第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
10 . 在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为 。
。
(1)德国化学家F·Haber利用 和
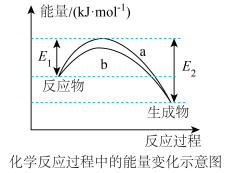
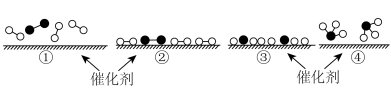
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、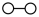 、
、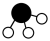 分别
分别 、
、 、
、 。
。_______ 。
A.氢气燃烧 B.氯化铵与 的反应
的反应
C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是_______ 。
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的
D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。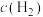 变化的曲线是
变化的曲线是_______ (填“A”“B”或“C”)。
②下列能说明该反应达到平衡状态的是_______ (填序号)。
a.容器中的压强不随时间变化
b.
c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol 的同时生成2mol
的同时生成2mol
e.容器内 的质量分数不变
的质量分数不变
(3)一定条件下,将2mol 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为_______ , 的转化率是
的转化率是_______ ,混合气中 的物质的量分数是
的物质的量分数是_______ 。
Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠( )与硫酸反应速率的影响。
)与硫酸反应速率的影响。
【查阅资料】
a. 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: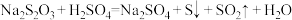
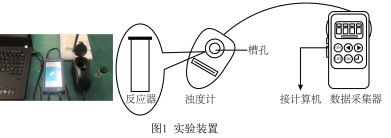
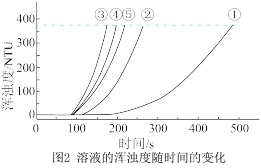
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
实验数据:
(4)选用浊度计进行测量,原因是 溶液与
溶液与 溶液反应生成了
溶液反应生成了_______ 。
(5)实验③中,x=_______ 。
(6)实验①、②、③的目的是_______ 。
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是_______ 。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为
 。
。(1)德国化学家F·Haber利用
 和
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、 、
、 分别
分别 、
、 、
、 。
。
A.氢气燃烧 B.氯化铵与
 的反应
的反应C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的

D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的
 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。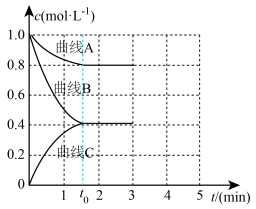
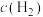 变化的曲线是
变化的曲线是②下列能说明该反应达到平衡状态的是
a.容器中的压强不随时间变化
b.

c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol
 的同时生成2mol
的同时生成2mol
e.容器内
 的质量分数不变
的质量分数不变(3)一定条件下,将2mol
 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为 的转化率是
的转化率是 的物质的量分数是
的物质的量分数是Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠(
 )与硫酸反应速率的影响。
)与硫酸反应速率的影响。【查阅资料】
a.
 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: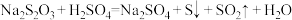
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
| 实验编号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | ||
 | V/mL |  | V/mL | V/mL | |
| ① | 0.1 | 1.5 | 0.1 | 3.5 | 10 |
| ② | 0.1 | 2.5 | 0.1 | 3.5 | 9 |
| ③ | 0.1 | 3.5 | 0.1 | 3.5 | x |
| ④ | 0.1 | 3.5 | 0.1 | 2.5 | 9 |
| ⑤ | 0.1 | 3.5 | 0.1 | 1.5 | 10 |
(4)选用浊度计进行测量,原因是
 溶液与
溶液与 溶液反应生成了
溶液反应生成了(5)实验③中,x=
(6)实验①、②、③的目的是
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对
 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是
您最近一年使用:0次
2024-04-25更新
|
294次组卷
|
2卷引用:广东省广州市育才中学2023-2024学年高一下学期 期中考试化学试题



