解题方法
1 . I.含碳化合物甲烷、 等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
(1)一种甲烷催化氧化的反应历程如图所示,“*”表示微粒吸附在催化剂表面。下列叙述错误的是___________(填标号)。
Ⅱ.以氧化铟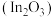 作催化剂,可实现
作催化剂,可实现 催化加氢制甲醇。
催化加氢制甲醇。
已知:ⅰ.催化剂活化: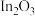 (无活性)
(无活性)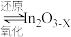 (有活性);
(有活性);
ⅱ. 与
与 在活化的催化剂表面同时发生如下反应:
在活化的催化剂表面同时发生如下反应:
反应①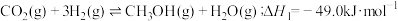
反应②
反应③: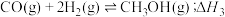
(2)反应③中
___________ 。
(3)工业上以原料气通过催化剂表面的方法生产甲醇, 是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:
是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:___________ 。为了减少催化剂的失活,可以采用的方法是___________ 。
(4)按 时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为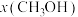 ,在t=250℃条件下的
,在t=250℃条件下的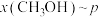 、在
、在 条件下的
条件下的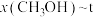 (温度)如图所示。
(温度)如图所示。___________ (填“a”或“b”),判断理由是___________ 。
ii.A、B、C、D、E、F中可能表示220℃ 时的平衡状态的点是
时的平衡状态的点是___________ 。
(5)将 和
和 按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
反应①的速率可表示为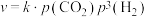 (
( 为常数),平衡时
为常数),平衡时 ,已知在
,已知在 时
时 的转化率为
的转化率为 ,则反应①的正向反应在
,则反应①的正向反应在 时的
时的
___________ (用含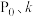 的式子表示)。
的式子表示)。
 等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:
等是重要的化工原料,可生产氢气、甲醇、烯烃等物质。回答下列问题:(1)一种甲烷催化氧化的反应历程如图所示,“*”表示微粒吸附在催化剂表面。下列叙述错误的是___________(填标号)。
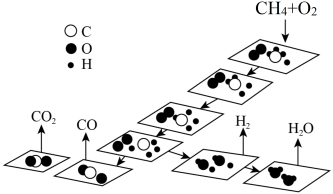
A.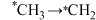 的过程中,放出能量 的过程中,放出能量 |
| B.产物从催化剂表面脱附的速率慢会降低总反应速率 |
C.适当提高 分压会降低 分压会降低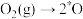 的反应速率 的反应速率 |
D. 与 与 反应生成 反应生成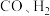 均涉及极性键、非极性键的断裂和生成 均涉及极性键、非极性键的断裂和生成 |
Ⅱ.以氧化铟
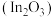 作催化剂,可实现
作催化剂,可实现 催化加氢制甲醇。
催化加氢制甲醇。已知:ⅰ.催化剂活化:
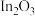 (无活性)
(无活性)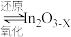 (有活性);
(有活性);ⅱ.
 与
与 在活化的催化剂表面同时发生如下反应:
在活化的催化剂表面同时发生如下反应:反应①
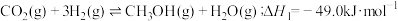
反应②

反应③:
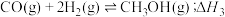
(2)反应③中

(3)工业上以原料气通过催化剂表面的方法生产甲醇,
 是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:
是造成催化剂失活的重要原因,请用化学方程式表示催化剂失活的原因:(4)按
 时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时只发生反应①,在不同条件下达到平衡,设体系中甲醇的物质的量分数为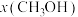 ,在t=250℃条件下的
,在t=250℃条件下的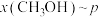 、在
、在 条件下的
条件下的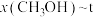 (温度)如图所示。
(温度)如图所示。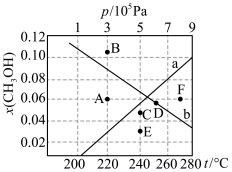
ii.A、B、C、D、E、F中可能表示220℃
 时的平衡状态的点是
时的平衡状态的点是(5)将
 和
和 按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:
按物质的量之比1:3混合通入刚性密闭容器中,在催化剂作用下只发生反应①和反应②。230℃时,容器内压强随时间的变化如下表所示:| 时间/min | 0 | 20 | 40 | 60 | 80 |
| 压强/MPa |  | 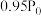 | 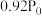 |  |  |
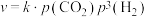 (
( 为常数),平衡时
为常数),平衡时 ,已知在
,已知在 时
时 的转化率为
的转化率为 ,则反应①的正向反应在
,则反应①的正向反应在 时的
时的
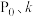 的式子表示)。
的式子表示)。
您最近一年使用:0次
2 . 甲醇是重要的化工原料。利用合成气(主要成分为CO、 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:
Ⅰ.

Ⅱ.

(1)在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
①
__________ 0,其理由是__________ 。
②能判断该反应达到化学平衡状态的依据是__________ 。
A. B.容器内
B.容器内 的体积分数保持不变
的体积分数保持不变
C.容器内气体密度保持不变 D.容器中压强保持不变
③若1200℃时,在某时刻平衡体系中 、
、 、CO(g)、
、CO(g)、 的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,此时
的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,此时
__________  (填大于、小于或等于),其理由是
(填大于、小于或等于),其理由是__________ 。
(2)某温度时在另一2L的恒容密闭容器中进行反应Ⅱ,若开始时通入CO1mol, 2mol,5min时反应达到平衡,测得平衡时CO的转化率为60%,平衡时总压强为PkPa.
2mol,5min时反应达到平衡,测得平衡时CO的转化率为60%,平衡时总压强为PkPa.
①0-5min,用CO表示的化学反应速率为__________ 。
②平衡时, 所占的物质的量分数为
所占的物质的量分数为__________ 。
 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:Ⅰ.


Ⅱ.


(1)在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

②能判断该反应达到化学平衡状态的依据是
A.
 B.容器内
B.容器内 的体积分数保持不变
的体积分数保持不变C.容器内气体密度保持不变 D.容器中压强保持不变
③若1200℃时,在某时刻平衡体系中
 、
、 、CO(g)、
、CO(g)、 的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,此时
的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,此时
 (填大于、小于或等于),其理由是
(填大于、小于或等于),其理由是(2)某温度时在另一2L的恒容密闭容器中进行反应Ⅱ,若开始时通入CO1mol,
 2mol,5min时反应达到平衡,测得平衡时CO的转化率为60%,平衡时总压强为PkPa.
2mol,5min时反应达到平衡,测得平衡时CO的转化率为60%,平衡时总压强为PkPa.①0-5min,用CO表示的化学反应速率为
②平衡时,
 所占的物质的量分数为
所占的物质的量分数为
您最近一年使用:0次
3 .  储存还原技术法(NSR)利用催化剂消除汽车尾气中的
储存还原技术法(NSR)利用催化剂消除汽车尾气中的 ,其原理:
,其原理: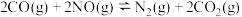
 。
。
(1)已知:① ;②
;②
 用含
用含 和
和 的代数式表示
的代数式表示
________ 。
(2)NSR反应机理及相对能量如图(TS表示过渡态):

反应过程中,速率最慢步骤的热化学方程式为________ 。
(3)在一定温度下,向2L恒容密闭容器中充入等物质的量的NO和CO模拟NSR反应,反应过程中c(NO)随时间变化的曲线如图1所示。

①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线________ (填“a”或“b”)。
②曲线b中前10min内CO的平均反应进率v(CO)=________ ,此温度下该反应的平衡常数K=________ 。
③在一恒温恒容的密闭容器中发生反应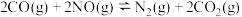 ,下列说法不能说明该反应达到化学平衡状态的是
,下列说法不能说明该反应达到化学平衡状态的是________ (填字母)。
aA.体系的压强保持不变 B.混合气体的密度保持不变
C. D.
D. 的浓度保持不变
的浓度保持不变
④若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是点________ (填“A、B、C、D或E”)。
(4) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图2可知工业使用的最佳催化剂和相应的温度分别为
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图2可知工业使用的最佳催化剂和相应的温度分别为________ 、________ 。
 储存还原技术法(NSR)利用催化剂消除汽车尾气中的
储存还原技术法(NSR)利用催化剂消除汽车尾气中的 ,其原理:
,其原理: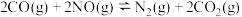
 。
。(1)已知:①
 ;②
;②
 用含
用含 和
和 的代数式表示
的代数式表示
(2)NSR反应机理及相对能量如图(TS表示过渡态):

反应过程中,速率最慢步骤的热化学方程式为
(3)在一定温度下,向2L恒容密闭容器中充入等物质的量的NO和CO模拟NSR反应,反应过程中c(NO)随时间变化的曲线如图1所示。

①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线
②曲线b中前10min内CO的平均反应进率v(CO)=
③在一恒温恒容的密闭容器中发生反应
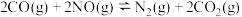 ,下列说法不能说明该反应达到化学平衡状态的是
,下列说法不能说明该反应达到化学平衡状态的是aA.体系的压强保持不变 B.混合气体的密度保持不变
C.
 D.
D. 的浓度保持不变
的浓度保持不变④若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是点
(4)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图2可知工业使用的最佳催化剂和相应的温度分别为
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图2可知工业使用的最佳催化剂和相应的温度分别为
您最近一年使用:0次
4 .  甲烷化是绿色低碳前沿技术研发的热点方向之一,在环境保护方面显示出较大潜力。涉及反应如下:
甲烷化是绿色低碳前沿技术研发的热点方向之一,在环境保护方面显示出较大潜力。涉及反应如下:
主反应:

副反应:
 ,
,
回答下列问题:
(1)向 密闭容器中充入
密闭容器中充入 反应合成
反应合成 ,平衡时混合气体中含碳物质的物质的量随温度的变化如图所示。
,平衡时混合气体中含碳物质的物质的量随温度的变化如图所示。
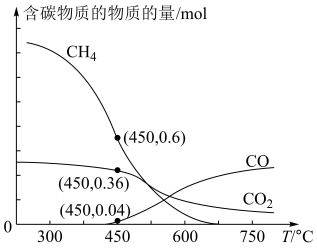
①工业上,常选用 作为合成温度,原因是
作为合成温度,原因是__________ 。
② 时,经过t分钟反应达平衡,t分钟内用
时,经过t分钟反应达平衡,t分钟内用 表示的反应速率为
表示的反应速率为______  ;该温度下
;该温度下 对甲烷的选择性=
对甲烷的选择性=________ 。(已知:选择性 )
)
(2)在体积相等的多个恒容密闭容器中,分别充入 和
和 发生上述主反应(忽略副反应),已知该反应的速率方程为
发生上述主反应(忽略副反应),已知该反应的速率方程为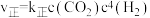 ,
, ,其中
,其中 为速率常数,只受温度影响。在不同温度下反应相同时间,测得
为速率常数,只受温度影响。在不同温度下反应相同时间,测得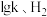 转化率与温度关系如图所示。
转化率与温度关系如图所示。
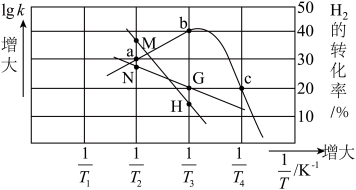
①c点______ (填“达平衡”或“未平衡”)。
②主反应活化能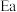 (正)
(正)___ 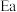 (逆)(填“>”或“<”),代表
(逆)(填“>”或“<”),代表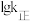 的曲线是
的曲线是______ (填“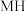 ”或“
”或“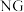 ”)。
”)。
③ 温度下达平衡时总压为p,该反应的
温度下达平衡时总压为p,该反应的
________ (列出计算式)。
(3)生物电化学系统可实现 合成甲烷。阴极功能微生物
合成甲烷。阴极功能微生物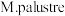 可以直接从阴极表面获得电子还原二氧化碳生产甲烷。酸性环境下该过程的电极反应式
可以直接从阴极表面获得电子还原二氧化碳生产甲烷。酸性环境下该过程的电极反应式________ 。
 甲烷化是绿色低碳前沿技术研发的热点方向之一,在环境保护方面显示出较大潜力。涉及反应如下:
甲烷化是绿色低碳前沿技术研发的热点方向之一,在环境保护方面显示出较大潜力。涉及反应如下:主反应:


副反应:

 ,
,回答下列问题:
(1)向
 密闭容器中充入
密闭容器中充入 反应合成
反应合成 ,平衡时混合气体中含碳物质的物质的量随温度的变化如图所示。
,平衡时混合气体中含碳物质的物质的量随温度的变化如图所示。
①工业上,常选用
 作为合成温度,原因是
作为合成温度,原因是②
 时,经过t分钟反应达平衡,t分钟内用
时,经过t分钟反应达平衡,t分钟内用 表示的反应速率为
表示的反应速率为 ;该温度下
;该温度下 对甲烷的选择性=
对甲烷的选择性= )
)(2)在体积相等的多个恒容密闭容器中,分别充入
 和
和 发生上述主反应(忽略副反应),已知该反应的速率方程为
发生上述主反应(忽略副反应),已知该反应的速率方程为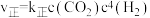 ,
, ,其中
,其中 为速率常数,只受温度影响。在不同温度下反应相同时间,测得
为速率常数,只受温度影响。在不同温度下反应相同时间,测得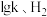 转化率与温度关系如图所示。
转化率与温度关系如图所示。
①c点
②主反应活化能
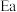 (正)
(正)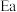 (逆)(填“>”或“<”),代表
(逆)(填“>”或“<”),代表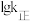 的曲线是
的曲线是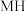 ”或“
”或“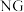 ”)。
”)。③
 温度下达平衡时总压为p,该反应的
温度下达平衡时总压为p,该反应的
(3)生物电化学系统可实现
 合成甲烷。阴极功能微生物
合成甲烷。阴极功能微生物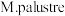 可以直接从阴极表面获得电子还原二氧化碳生产甲烷。酸性环境下该过程的电极反应式
可以直接从阴极表面获得电子还原二氧化碳生产甲烷。酸性环境下该过程的电极反应式
您最近一年使用:0次
名校
5 . 运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机有重要意义。
Ⅰ.已知: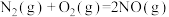 ∆H=akJ·mol
∆H=akJ·mol K1
K1
 ∆H=bkJ·mol
∆H=bkJ·mol K2
K2
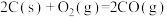 ∆H=ckJ·mol
∆H=ckJ·mol K3
K3
(1)写出CO还原NO反应的热化学方程式______ (∆H用含a、b、c表达式表示),并写出该反应的平衡常数表达式______ (用)K1、K2、K3表示)。
Ⅱ.用H2还原CO2在一定条件下合成CH3OH; ∆H<0
∆H<0
(2)某温度下,在恒容密闭容器中发生可逆反应 ,下列说法中能说明该反应达到化学平衡状态的是______(填字母序号)。
,下列说法中能说明该反应达到化学平衡状态的是______(填字母序号)。
(3)T1℃下,在2 L恒容密闭容器中充入2 mol CO2和6 mol H2合成CH3OH(g),测得5分钟后反应达平衡,平衡后压强是初始压强的 ,求v(H2)=
,求v(H2)= ______ 。
(4)用 还原CO2合成CH3OH反应中在起始物
还原CO2合成CH3OH反应中在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃时,x(CH3OH)随压强(p)的变化及在
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃时,x(CH3OH)随压强(p)的变化及在 Pa时x(CH3OH)随温度(T)的变化,如图所示。
Pa时x(CH3OH)随温度(T)的变化,如图所示。
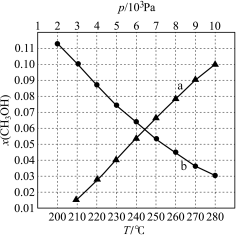
①图中对应等压过程的曲线是______ (填“a”或“b”),判断的理由是____________ 。
②恒温时(T=250℃),x(CH3OH)=0.1时,CO2的平衡转化率
______ (保留小数点后一位),此条件下该反应的Kp=______ Pa-2(保留小数点后一位)(分压=总压×物质的量分数)。
Ⅰ.已知:
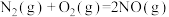 ∆H=akJ·mol
∆H=akJ·mol K1
K1 ∆H=bkJ·mol
∆H=bkJ·mol K2
K2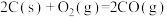 ∆H=ckJ·mol
∆H=ckJ·mol K3
K3(1)写出CO还原NO反应的热化学方程式
Ⅱ.用H2还原CO2在一定条件下合成CH3OH;
 ∆H<0
∆H<0(2)某温度下,在恒容密闭容器中发生可逆反应
 ,下列说法中能说明该反应达到化学平衡状态的是______(填字母序号)。
,下列说法中能说明该反应达到化学平衡状态的是______(填字母序号)。| A.混合气体的平均相对分子质量不再变化 |
| B.混合气体的密度不再变化 |
| C.体系的压强不再发生变化 |
| D. CO2、H2、CH3OH的物质的量之比为1∶2∶1 |
(3)T1℃下,在2 L恒容密闭容器中充入2 mol CO2和6 mol H2合成CH3OH(g),测得5分钟后反应达平衡,平衡后压强是初始压强的
 ,求v(H2)=
,求v(H2)= (4)用
 还原CO2合成CH3OH反应中在起始物
还原CO2合成CH3OH反应中在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃时,x(CH3OH)随压强(p)的变化及在
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃时,x(CH3OH)随压强(p)的变化及在 Pa时x(CH3OH)随温度(T)的变化,如图所示。
Pa时x(CH3OH)随温度(T)的变化,如图所示。
①图中对应等压过程的曲线是
②恒温时(T=250℃),x(CH3OH)=0.1时,CO2的平衡转化率

您最近一年使用:0次
6 . 2023年9月23日晚,随着亚运会主火炬的点燃,第19届亚运会在杭州正式开幕。开幕式主火炬燃料创新使用零碳甲醇燃料,彰显了中国打造碳中和亚运会的成果。
I.甲醇作为火炬燃料亮相世界,为甲醇产业迎来了高光时刻,甲醇技术路线有望成为中国绿色能源重要组成部分。
目前,工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:
反应Ⅱ: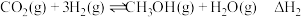
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)
(1)在一定条件下将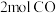 和
和 充入
充入 的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得
的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得 ,此段时间的反应速率(用
,此段时间的反应速率(用 表示)为
表示)为___________  。若此时再向容器中加入
。若此时再向容器中加入 、
、 、
、 各
各 ,则化学平衡
,则化学平衡___________ (填“正向”、“逆向”或“不”)移动。
(2)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是___________ 。
a.充入CO b.将 从体系中分离 c.升高温度 d.选用新型高效催化剂
从体系中分离 c.升高温度 d.选用新型高效催化剂
(3)一定温度下,在固定容积的密闭容器中发生反应Ⅱ,下列能判断反应达到平衡状态的是___________ 。
a.容器中的压强不再改变 b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变 d.消耗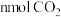 的同时生成
的同时生成
Ⅱ.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨,二氧化碳加氢制甲醇为零碳甲醇的重要来源,在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
Ⅰ.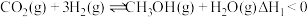
Ⅱ.
回答下列问题:
(4) 在催化剂作用下,将平均相对分子质量为16的
在催化剂作用下,将平均相对分子质量为16的 和
和 的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正)
的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正) (正)
(正)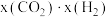 ,v(逆)
,v(逆) (逆)
(逆)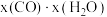 ,k(正)、k(逆)为速率常数,x为物质的量分数。
,k(正)、k(逆)为速率常数,x为物质的量分数。
①当 转化率达到
转化率达到 时,反应达到平衡状态,这时
时,反应达到平衡状态,这时 和
和 的平均相对分子质量为23,若反应Ⅱ的k(正)
的平均相对分子质量为23,若反应Ⅱ的k(正)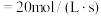 ,平衡时反应速率v(逆)
,平衡时反应速率v(逆)
___________ 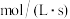 ;
;
②由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回16,原因是___________ 。
(5)其他条件相同时,反应温度对 选择性(转化为
选择性(转化为 的
的 在总转化量中的占比)的影响如图所示:
在总转化量中的占比)的影响如图所示:
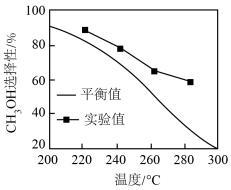
由图可知,温度相同时 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是___________ 。
I.甲醇作为火炬燃料亮相世界,为甲醇产业迎来了高光时刻,甲醇技术路线有望成为中国绿色能源重要组成部分。
目前,工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:

反应Ⅱ:
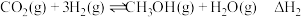
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(1)在一定条件下将
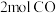 和
和 充入
充入 的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得
的密闭容器中发生反应Ⅰ,5分钟后达到平衡,测得 ,此段时间的反应速率(用
,此段时间的反应速率(用 表示)为
表示)为 。若此时再向容器中加入
。若此时再向容器中加入 、
、 、
、 各
各 ,则化学平衡
,则化学平衡(2)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是
a.充入CO b.将
 从体系中分离 c.升高温度 d.选用新型高效催化剂
从体系中分离 c.升高温度 d.选用新型高效催化剂(3)一定温度下,在固定容积的密闭容器中发生反应Ⅱ,下列能判断反应达到平衡状态的是
a.容器中的压强不再改变 b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变 d.消耗
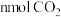 的同时生成
的同时生成
Ⅱ.近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨,二氧化碳加氢制甲醇为零碳甲醇的重要来源,在某
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:Ⅰ.
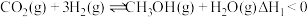
Ⅱ.

回答下列问题:
(4)
 在催化剂作用下,将平均相对分子质量为16的
在催化剂作用下,将平均相对分子质量为16的 和
和 的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正)
的混合气体充入一恒容密闭容器中发生反应Ⅰ、Ⅱ,已知反应Ⅱ的反应速率v(正) (正)
(正)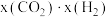 ,v(逆)
,v(逆) (逆)
(逆)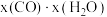 ,k(正)、k(逆)为速率常数,x为物质的量分数。
,k(正)、k(逆)为速率常数,x为物质的量分数。①当
 转化率达到
转化率达到 时,反应达到平衡状态,这时
时,反应达到平衡状态,这时 和
和 的平均相对分子质量为23,若反应Ⅱ的k(正)
的平均相对分子质量为23,若反应Ⅱ的k(正)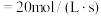 ,平衡时反应速率v(逆)
,平衡时反应速率v(逆)
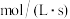 ;
;②由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回16,原因是
(5)其他条件相同时,反应温度对
 选择性(转化为
选择性(转化为 的
的 在总转化量中的占比)的影响如图所示:
在总转化量中的占比)的影响如图所示:
由图可知,温度相同时
 选择性的实验值略高于其平衡值,可能的原因是
选择性的实验值略高于其平衡值,可能的原因是
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.分别取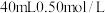 盐酸与
盐酸与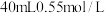 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:
(1)本实验除烧杯、量筒、温度计外还缺少的玻璃仪器名称为___________ 。
(2)若某同学通过该实验测定出中和热 偏大,请分析可能的原因是
偏大,请分析可能的原因是___________ (填序号)。
A.用量筒量取盐酸时仰视读数
B.分多次将 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
C.将盐酸错取为等浓度的醋酸
Ⅱ.某化学小组为了探究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】
【实验内容及记录】
回答下列问题:
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)利用实验3中数据计算,此条件下的反应速率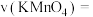
___________  。
。
(5)该小组同学根据经验绘制了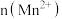 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中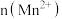 随时间变化的趋势应如图2所示。
随时间变化的趋势应如图2所示。
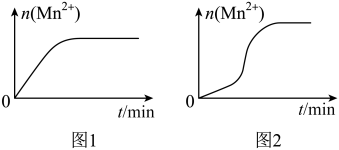
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设:生成的 对该反应有催化作用。
对该反应有催化作用。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③现象及结论:依据现象___________ ,得出该小组同学提出的假设成立。
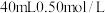 盐酸与
盐酸与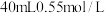 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:(1)本实验除烧杯、量筒、温度计外还缺少的玻璃仪器名称为
(2)若某同学通过该实验测定出中和热
 偏大,请分析可能的原因是
偏大,请分析可能的原因是A.用量筒量取盐酸时仰视读数
B.分多次将
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中C.将盐酸错取为等浓度的醋酸
Ⅱ.某化学小组为了探究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】

【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量 | 室温下溶液褪色所需时间 | |||
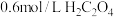 |  | 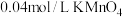 | 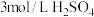 | ||
| 1 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
| 2 | 2.0 | 3.0 | 3.0 | 2.0 | 5.2 |
| 3 | 3.0 | 2.0 | 3.0 | 2.0 | 2.0 |
(3)根据上表中的实验数据,可以得到的结论是
(4)利用实验3中数据计算,此条件下的反应速率
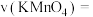
 。
。(5)该小组同学根据经验绘制了
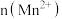 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中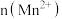 随时间变化的趋势应如图2所示。
随时间变化的趋势应如图2所示。
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设:生成的
 对该反应有催化作用。
对该反应有催化作用。②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入少量固体 | 室温下溶液褪色所需时间 | |||
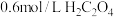 |  | 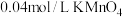 | 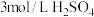 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | (填化学式) | t |
您最近一年使用:0次
名校
8 . 苯乙稀是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。
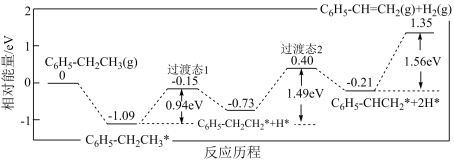
(1)科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图所示(吸附在催化剂表面的物质用*标注):
___________ (填“>”“<”或“=”)0,为提高乙苯的平衡转化率,应选择的反应条件为___________ (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
(2)有研究者发现,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:___________ 。
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是___________ (写一点即可)。
③从资源综合利用角度分析, 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是___________ 。
(3) 恒压下,将
恒压下,将 乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
① 时,反应经过
时,反应经过 达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为
达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为________ ,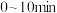 内的平均反应速率
内的平均反应速率
________  ,该温度下的
,该温度下的
________  。
。
②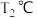 时,若再向体系中通入氮气,此时
时,若再向体系中通入氮气,此时
___________ (填“增大”“减小”或“不变”)。
(1)科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图所示(吸附在催化剂表面的物质用*标注):

A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
(2)有研究者发现,在
 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图: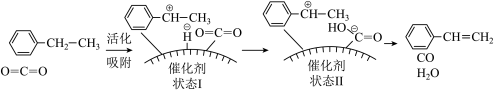
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是
③从资源综合利用角度分析,
 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是(3)
 恒压下,将
恒压下,将 乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。①
 时,反应经过
时,反应经过 达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为
达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为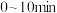 内的平均反应速率
内的平均反应速率
 ,该温度下的
,该温度下的
 。
。②
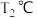 时,若再向体系中通入氮气,此时
时,若再向体系中通入氮气,此时
您最近一年使用:0次
2023-12-01更新
|
820次组卷
|
6卷引用:2024届内蒙古自治区包头市高三下学期适应性考试(一)理综试题-高中化学
2024届内蒙古自治区包头市高三下学期适应性考试(一)理综试题-高中化学2024届河南省新乡市高三第一次模拟考试理科综合试题河北省邯郸市六校联考2023-2024学年高二上学期11月月考化学试题2024届陕西省西安市第一中学高三上学期12月月考理综试卷河南省濮阳市油田第一中学2024届高三第四次考试理科综合化学试题(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
9 . 研究化学反应中的能量和速率变化对生产、生活有着重要意义。
I.某些常见化学键的键能(将 气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
(1) 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为___________ kJ。该反应中反应物的总能量___________ (填“>”、“<”或“=”)生成物的总能量。
II.实验室模拟热气循环法合成尿素, 与
与 在一定条件下发生反应:
在一定条件下发生反应: 。
。
为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
(2)控制变量是科学研究的重要方法,因此表中数据:
________ ,
________ 。
(3)对比实验①③,目的是验证___________ (填“反应温度”或“催化剂的比表面积”)对化学反应速率的影响规律。
(4)一定温度下,向1L密闭容器中充入 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
___________  ,
, 的平衡转化率为
的平衡转化率为___________ %。
(5)下列情况中,一定能说明上述反应达到平衡的是___________(填标号)。
(6)“碳呼吸电池”是一种新型化学电源,其工作原理如图。当得到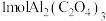 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为___________ mol。

I.某些常见化学键的键能(将
 气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:
气体分子AB断裂为中性气态原子A和B所需的能量或A和B合成1molAB气体所放出的能量)数据如下表:| 化学键 |  |  |  |  |
键能/( ) ) | 414 | 803 | 463 | 498 |
(1)
 完全燃烧生成
完全燃烧生成 和气态水放出的能量为
和气态水放出的能量为II.实验室模拟热气循环法合成尿素,
 与
与 在一定条件下发生反应:
在一定条件下发生反应: 。
。为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
| 实验编号 | 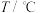 |  初始浓度/( 初始浓度/( ) ) |  初始浓度/( 初始浓度/( ) ) | 催化剂的比表面积/(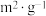 ) ) |
| ① | 280 |  | 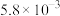 | 82 |
| ② |  |  | 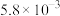 | 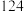 |
| ③ | 350 | a | 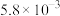 | 82 |
(2)控制变量是科学研究的重要方法,因此表中数据:


(3)对比实验①③,目的是验证
(4)一定温度下,向1L密闭容器中充入
 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
,反应2min后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则0~2min内,
 ,
, 的平衡转化率为
的平衡转化率为(5)下列情况中,一定能说明上述反应达到平衡的是___________(填标号)。
A. 的体积分数保持不变 的体积分数保持不变 |
| B.反应体系中气体的密度保持不变 |
C.反应消耗 ,同时生成 ,同时生成 |
D. 的质量保持不变 的质量保持不变 |
(6)“碳呼吸电池”是一种新型化学电源,其工作原理如图。当得到
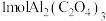 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为
您最近一年使用:0次
10 . 甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列反应合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在体积为2L的密闭中,充入2molCO2和9molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g)。在体积为2L的密闭中,充入2molCO2和9molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。

(1)该反应的平衡常数K表达式为_____ 。
(2)0~10min时间内,该反应的平均反应速率v(H2O)=_____ ,H2的转化率为_____ 。
(3)下列叙述中,能说明反应已达到化学平衡状态的是_____ 。(填字母)
A.容器内CO2、H2、CH3OH、H2O(g)的浓度之比为1:3:1:1
B.v(CO2)正:v(H2)逆=1:3
C.混合气体的平均相对分子质量保持不变
(4)已知在常温常压下:
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) △H1=-1452.8kJ•mol-1
②2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ•mol-1
③CH3OH(1)+O2(g)=2H2O(1)+CO(g) △H
则△H=_____ kJ/mol
 CH3OH(g)+H2O(g)。在体积为2L的密闭中,充入2molCO2和9molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g)。在体积为2L的密闭中,充入2molCO2和9molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
(1)该反应的平衡常数K表达式为
(2)0~10min时间内,该反应的平均反应速率v(H2O)=
(3)下列叙述中,能说明反应已达到化学平衡状态的是
A.容器内CO2、H2、CH3OH、H2O(g)的浓度之比为1:3:1:1
B.v(CO2)正:v(H2)逆=1:3
C.混合气体的平均相对分子质量保持不变
(4)已知在常温常压下:
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) △H1=-1452.8kJ•mol-1
②2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ•mol-1
③CH3OH(1)+O2(g)=2H2O(1)+CO(g) △H
则△H=
您最近一年使用:0次



