名校
解题方法
1 . Ⅰ.已知在氨水中存在下平衡:NH3+H2O NH3·H2O
NH3·H2O NH
NH +OH-。
+OH-。
(1)向氨水中加入 固体时,平衡向
固体时,平衡向_______ (填“左”或“右”)移动,OH-的浓度_______ (填“增大”或“减小”,下同), 的浓度
的浓度_______ 。
(2)向氨水中加入浓盐酸,平衡向_______ (填“左”或“右”)移动,此时溶液中浓度减小的微粒有_______ 。
(3)向氨水中加入少量的NaOH固体,平衡向_______ (填“左”或“右”)移动。
Ⅱ.地下水中的氮污染主要是由 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:2NO
将硝酸盐还原成氮气:2NO +5H2
+5H2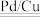 N2↑+2OH-+4H2O。
N2↑+2OH-+4H2O。
(4)下列说法错误的是_______ (填序号)。
A.氮肥 溶于水的过程中熵值增大
溶于水的过程中熵值增大
B.在酸性条件下,活泼金属与 反应属于自发反应
反应属于自发反应
C.Pd/Cu双金属催化剂是该反应是否能自发发生的决定因素
(5)已知:2NO +5H2
+5H2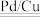 N2↑+2OH-+4H2O的
N2↑+2OH-+4H2O的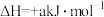 ,
,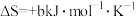 (a、b均为正值),该反应
(a、b均为正值),该反应_______ (填“能”“不能”或“无法判断是否能”)自发进行。
 NH3·H2O
NH3·H2O NH
NH +OH-。
+OH-。(1)向氨水中加入
 固体时,平衡向
固体时,平衡向 的浓度
的浓度(2)向氨水中加入浓盐酸,平衡向
(3)向氨水中加入少量的NaOH固体,平衡向
Ⅱ.地下水中的氮污染主要是由
 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:2NO
将硝酸盐还原成氮气:2NO +5H2
+5H2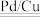 N2↑+2OH-+4H2O。
N2↑+2OH-+4H2O。(4)下列说法错误的是
A.氮肥
 溶于水的过程中熵值增大
溶于水的过程中熵值增大B.在酸性条件下,活泼金属与
 反应属于自发反应
反应属于自发反应C.Pd/Cu双金属催化剂是该反应是否能自发发生的决定因素
(5)已知:2NO
 +5H2
+5H2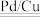 N2↑+2OH-+4H2O的
N2↑+2OH-+4H2O的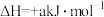 ,
,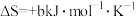 (a、b均为正值),该反应
(a、b均为正值),该反应
您最近一年使用:0次
2 . 已知: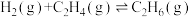
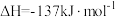 。请回答下列问题:
。请回答下列问题:
(1)该反应在_______ (填“低温”、“高温”或“任何温度”下能自发进行。
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
(3)若在10 L的密闭容器内2 mol H2(g)与a molC2H4(g)进行上述反应,测得 的平衡转化率与投料比X,
的平衡转化率与投料比X,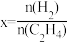 以及温度的关系如图所示。
以及温度的关系如图所示。
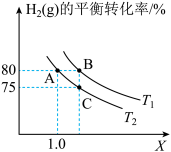
①反应从开始分别进行到A、B、C点时,_______ (填“吸收”或“放出”)的热量QA、QB、QC由大到小的顺序为_______ 。
②T1_______ (填“>”、“<”或“=”)T2。
③B点对应的体系中a=_______ 。A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。
(4)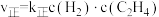 ,
,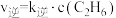 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
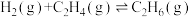
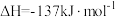 。请回答下列问题:
。请回答下列问题:(1)该反应在
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 | B.c正(H2)=c逆(C2H6) |
| C.容器内混合气体的压强不变 | D.容器内混合气体的密度不变 |
 的平衡转化率与投料比X,
的平衡转化率与投料比X,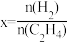 以及温度的关系如图所示。
以及温度的关系如图所示。
①反应从开始分别进行到A、B、C点时,
②T1
③B点对应的体系中a=
(4)
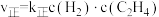 ,
,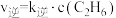 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。| A.k正增大的倍数大于k逆 | B.k正增大的倍数小于k逆 |
C.k正减小的倍数大于 | D.k正减小的倍数小于k逆 |
您最近一年使用:0次
2022-11-07更新
|
112次组卷
|
3卷引用:湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
名校
解题方法
3 . 下列表述正确的是
| A.△H>0和△S>0的反应,在任何温度下都不能自发进行 |
B.根据 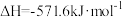 可知氢气的燃烧热为571.6 kJ/mol 可知氢气的燃烧热为571.6 kJ/mol |
| C.HCl溶液和NaOH溶液反应的中和热△H =-57.3 kJ/mol,则含2 mol硫酸的稀溶液与足量氢氧化钡溶液反应放热为114.6 kJ |
D.已知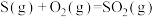 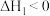 , ,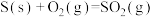 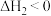 ,则△H1<△H2 ,则△H1<△H2 |
您最近一年使用:0次
2022-11-04更新
|
138次组卷
|
7卷引用:湖北省六校新高考联盟学校2022-2023学年高二上学期9月联考化学试题
名校
4 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
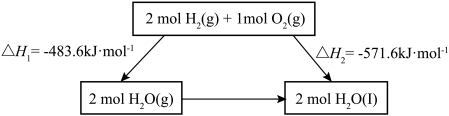
下列说法不正确 的是

下列说法
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
B. 的过程中, 的过程中, , , |
C.断裂2mol 和1mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量大于断裂2mol 中化学键所需能量 中化学键所需能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-11-04更新
|
620次组卷
|
9卷引用:湖北省襄阳市第五中学2022-2023学年高二下学期开学考试化学试题
名校
5 . 下列有关化学反应原理的说法中正确的是
| A.需要加热的反应都是非自发反应,不需要加热的反应都是自发反应 |
B.反应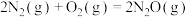  ,则该反应能自发进行 ,则该反应能自发进行 |
| C.100mL2mol/L的盐酸与锌片反应,加入少量NaCl固体,反应速率不变 |
| D.若反应可以自发,则该反应的速率一定较快 |
您最近一年使用:0次
2022-11-04更新
|
325次组卷
|
2卷引用:湖北省荆州市沙市中学2022-2023学年高二上学期11月期中考试化学试题
解题方法
6 . 光气(COCl2)是一种重要的有机中间体。反应CHCl3(l)+H2O2(l)=COCl2(g)+HCl(g)+H2O(l) ΔH<0可用于制备光气。下列有关叙述正确的是。
| A.CHCl3为非极性分子 | B.氯原子的结构示意图为 |
C.H2O2的电子式为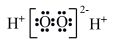 | D.该反应低温才能自发进行反应 |
您最近一年使用:0次
7 . 下列说法中正确的是
| A.△H<0、△S<0的反应在任何温度时均不能自发进行 |
| B.反应:CaCO3(s)=CaO(s)+CO2(g) △H>0,在高温时能自发进行 |
| C.增大压强,平衡向正反应方向移动,平衡常数K值增大 |
| D.增大反应物浓度,使活化分子百分数增加,化学反应速率增大 |
您最近一年使用:0次
2022-10-26更新
|
115次组卷
|
2卷引用:湖北省巴东县第三高级中学2022-2023学年高二上学期第一次月考化学试题
11-12高二上·安徽淮北·期中
名校
8 . 已知FeO(s) +C(s)= CO(g) + Fe(s) △H>0,下列叙述正确的是
| A.低温下为自发过程,高温下为非自发过程 | B.任何温度下为非自发过程 |
| C.高温下为自发过程,低温下为非自发过程 | D.任何温度下为自发过程 |
您最近一年使用:0次
2022-10-26更新
|
466次组卷
|
25卷引用:湖北省黄州中学2022--2023学年高二上学期10月月考化学试题
湖北省黄州中学2022--2023学年高二上学期10月月考化学试题(已下线)2011-2012学年安徽省濉溪县临涣中学高二上学期期中联考化学试卷(已下线)2014-2015学年山东安丘市实验中学期中考试高二化学模拟(A)卷(已下线)2014秋安徽省宿州市高二上学期期中化学(理)试卷2015-2016学年安徽省舒城晓天中学高二上学期期中测试化学试卷【全国百强校】江苏省南菁高级中学2017-2018学年高二下学期期中考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二上学期第一次月考(10月)化学试题安徽省新城高升学校2018-2019学年高二上学期期中考试化学试题广西南宁市“4N”高中联合体2018-2019学年高二下学期期末考试化学试题云南省普洱市澜沧县第一中学2018-2019学年高二下学期期末考试化学试题云南省普洱市澜沧县民族中学2018-2019学年高二下学期期末考试化学试题河南省鹤壁市浚县二中2019-2020学年高二上学期第二次月考化学试题安徽省亳州市第十八中学2019-2020学年高二上学期第一次月考化学试题2020年春季人教版高中化学选修4第二章《化学反应速率和化学平衡》测试卷人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第三节 化学反应的方向 作业帮(已下线)第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第1节 化学反应的方向安徽省蚌埠田家炳中学2020-2021学年高二12月月考化学试题重庆市铁路中学校2020-2021学年高二上学期11月月考化学试题贵州省贵阳市清镇养正学校2019-2020学年高二上学期期中考试化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题吉林省延吉市第一高级中学2021-2022年学年高二上学期期中考试化学试题四川省宜宾市第四中学校2022-2023学年高二上学期期中考试化学试题新疆喀什地区疏附县第一中学2022-2023学年高二上学期期末考试化学试题百所名校联考-化学反应速率与化学平衡
解题方法
9 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I. 脱硝: 已知:H2的燃烧热为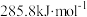 ;
;
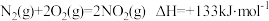 ;
; 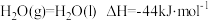
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为_______ 。
II.脱碳:
(2)向2L密闭容器中加入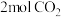 和
和 ,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) 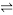 CH3OH(1)+H2O(l) △H<0
CH3OH(1)+H2O(l) △H<0
①该反应自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
②下列叙述能说明此反应达到平衡状态的是_______ (填字母)。
a.混合气体的平均相对分子质量保持不变 b. 和H2的体积分数保持不变
和H2的体积分数保持不变
c. 和H2的转化率相等 d.混合气体的密度保持不变
和H2的转化率相等 d.混合气体的密度保持不变
e.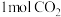 生成的同时有
生成的同时有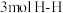 键断裂
键断裂
③ 的浓度随时间(
的浓度随时间(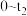 )变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出
)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出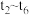 时间段
时间段 浓度随时间的变化。
浓度随时间的变化。_______
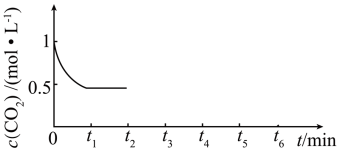
(3)改变温度,使反应CO2(g)+3H2(g)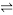 CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应I、II对比:平衡常数K(I)_______ K(II)(填“>”“<”或“=”,下同);平衡时 的浓度c(I)
的浓度c(I)_______ c(II)。
②对反应I,前10min内的平均反应速率 =
=_______ ;在其他条件不变的情况下,若30min时只向容器中再充入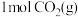 和
和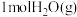 ,则平衡
,则平衡__ (填“正向”“逆向”或“不”)移动。
I. 脱硝: 已知:H2的燃烧热为
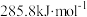 ;
;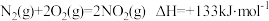 ;
; 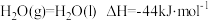
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
II.脱碳:
(2)向2L密闭容器中加入
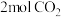 和
和 ,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) 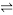 CH3OH(1)+H2O(l) △H<0
CH3OH(1)+H2O(l) △H<0①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.
 和H2的体积分数保持不变
和H2的体积分数保持不变c.
 和H2的转化率相等 d.混合气体的密度保持不变
和H2的转化率相等 d.混合气体的密度保持不变e.
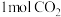 生成的同时有
生成的同时有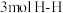 键断裂
键断裂③
 的浓度随时间(
的浓度随时间(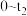 )变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出
)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出 时间段
时间段 浓度随时间的变化。
浓度随时间的变化。
(3)改变温度,使反应CO2(g)+3H2(g)
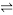 CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间(min) |  (mol) (mol) |  (mol) (mol) |  (mol) (mol) |  (mol) (mol) | |
| 反应I:恒温恒容 | 0 | 2 | 6 | 0 | 0 |
| 10 | 4.5 | ||||
| 20 | 1 | ||||
| 30 | 1 | ||||
| 反应II:绝热恒容 | 0 | 0 | 0 | 2 | 2 |
 的浓度c(I)
的浓度c(I)②对反应I,前10min内的平均反应速率
 =
=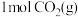 和
和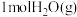 ,则平衡
,则平衡
您最近一年使用:0次
10 . 下列有关化学反应方向及其判据的说法中错误的是
A.1mol 在不同状态时的熵值: 在不同状态时的熵值: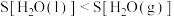 |
B.反应  能否自发进行与温度有关 能否自发进行与温度有关 |
C. 分解和HClO分解均是自发过程,故这两个反应的 分解和HClO分解均是自发过程,故这两个反应的 和 和 的变化相同 的变化相同 |
D.常温下,反应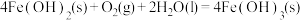 能自发进行,则该反应的 能自发进行,则该反应的 |
您最近一年使用:0次
2022-09-29更新
|
495次组卷
|
9卷引用:湖北省襄阳市部分学校2022-2023学年高二上学期9月联考化学试题
湖北省襄阳市部分学校2022-2023学年高二上学期9月联考化学试题河北省保定市部分学校2022-2023学年高二上学期第一次月考化学试题湖南省邵阳市武冈市2022-2023学年高二上学期期中考试化学试题山东省济宁市梁山县第一中学2022-2023学年高二10月月考化学试题山东省济宁市梁山一中2022-2023学年高二上学期11月月考化学试题(已下线)第07讲 化学反应的方向-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)河北省唐县第一中学2023-2024学年高二上学期10月考试化学化学 广东省东莞市万江中学2023届高三10月月考化学试题(已下线)第5讲 化学反应的调控



