名校
解题方法
1 . 下列有关化学反应方向及其判据的说法中错误的是
| A.1molH2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] |
| B.NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
C.CaCO3(s)  CaO(s)+CO2(g) △H>0能否自发进行与温度有关 CaO(s)+CO2(g) △H>0能否自发进行与温度有关 |
| D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的 △H>0 |
您最近一年使用:0次
2020-10-20更新
|
189次组卷
|
5卷引用:湖北省宜城市第三高级中学2020-2021学年高二上学期期中考试化学试题
名校
2 . 化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是
A.反应 的 的 |
B.  在不同状态时的熵值: 在不同状态时的熵值: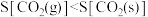 |
C.反应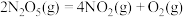  能否自发进行与温度有关 能否自发进行与温度有关 |
D. 或 或 的反应一定能自发进行 的反应一定能自发进行 |
您最近一年使用:0次
2021-06-12更新
|
2260次组卷
|
21卷引用:湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题
湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题河南名校联盟2020-2021学年高二下学期期中考试化学试题(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)吉林省延边第二中学2021-2022学年高二上学期第一次阶段检测化学试题吉林省四平市普通高中2021-2022学年高二上学期期中考试化学试题云南省昭通市镇雄县第四中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3 化学反应的方向(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)新疆乌鲁木齐市第八中学2022-2023学年高二上学期期中考试化学试题宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高二上学期期中考试化学试题山东省滕州市第一中学2022-2023学年高二上学期11月月考化学试题山东省2022-2023学年高二上学期12月联合调考化学试题(已下线)第07讲 化学反应的方向-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)新疆塔城地区塔城市2022-2023学年高二上学期11月期中考试化学试题安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题山东省青岛莱西市2022-2023学年高二上学期期中考试化学试题云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题
3 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法一定正确的是
| A.氢氧燃料电池的负极反应为:O2+2H2O+4e −= 4OH− |
| B.一定温度下,反应2H2(g)+O2(g)=2H2O(g)能自发进行,该反应的ΔH<0 |
| C.常温常压,氢氧燃料电池放电过程中转移电子的数目6.02×1023时,消耗 H2 11.2 L |
| D.反应2H2(g)+O2(g)=2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和−反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
名校
解题方法
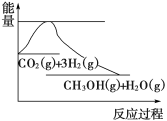
4 . 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化,关于该反应的下列说法中,正确的是( )
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化,关于该反应的下列说法中,正确的是( )
 CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化,关于该反应的下列说法中,正确的是( )
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化,关于该反应的下列说法中,正确的是( )
| A.高温下自发进行 | B.任何温度都不自发进行 |
| C.低温下自发进行 | D.任何温度都能自发进行 |
您最近一年使用:0次
2020-07-24更新
|
156次组卷
|
4卷引用:湖北省石首市第一中学2020-2021学年高二上学期10月月考化学试题
湖北省石首市第一中学2020-2021学年高二上学期10月月考化学试题福建省福州福清市2017-2018学年高二上学期期末考试化学试题(已下线)2.4化学反应进行的方向(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)贵州省金沙县精诚中学2021-2022学年高二上学期期中理综化学试题
名校
5 . 下列说法中正确的是
| A.生成物的总能量大于反应物的总能量时,ΔH<0 |
| B.已知反应H2(g)+I2(g)⇌2HI(g)的平衡常数为K,则2H2(g)+2I2(g)⇌4HI(g)的平衡常数为2K |
| C.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在低温下能自发进行,说明该反应的ΔH>0 |
您最近一年使用:0次
2020-12-18更新
|
279次组卷
|
2卷引用:湖北省荆州中学2021-2022学年高二上学期期末考试化学试题
解题方法
6 . 根据反应情况不同,反应热可分为多种,例如燃烧热、中和热、溶解热等,下列关于燃烧热的说法不正确的是
| A.已知:S(s)+O2 (g)=SO2 (g) ΔH1=—Q1 kJ•mol-1,S(g)+O2 (g)=SO2 (g) ΔH2=—Q2 kJ•mol-1,则Q1<Q2 |
| B.已知反应C(s)+CO2 (g)= 2CO(g)的ΔH>0,则该反应在高温下能自发进行 |
C.500℃、30MPa下,将0.5mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3,放出的热量为19.3 kJ,其热化学方程式为N2 (g)+3H2 (g)  2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 |
| D.已知中和热为—57.3 kJ•mol-1,若将含0.5 mol H2 SO4的稀溶液与含0.5 mol Ba(OH)2的稀溶液混合,放出的热量等于57.3 kJ |
您最近一年使用:0次
7 . 有关化学反应原理的下列说法中正确的是
| A.吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 |
B.常温下,反应C(s)+CO2(g) 2CO(g)不能自发进行,则该反应的ΔH>0 2CO(g)不能自发进行,则该反应的ΔH>0 |
| C.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 |
| D.电池的两个电极不可能材料相同 |
您最近一年使用:0次
2020-11-05更新
|
116次组卷
|
2卷引用:湖北省四地六校2020-2021学年高二上学期联合考试化学试题
解题方法
8 . 已知 2A(g)⇌3B(g)+C(g) ΔH>0,假设ΔH和ΔS不随温度而改变,下列说法中正确的是
| A.低温下能自发进行 | B.高温下能自发进行 |
| C.任何温度下都能自发进行 | D.任何温度下都不能自发进行 |
您最近一年使用:0次
2021-01-14更新
|
257次组卷
|
4卷引用:湖北省云学新高考联盟学校2022-2023学年高二上学期10月联考化学试题
解题方法
9 . 下列关于化学反应方向的说法正确的是
| A.凡是放热反应都是自发反应 | B.凡是熵增大的反应都是自发反应 |
| C.凡是吸热反应都不是自发反应 | D.反应是否自发,需要综合考虑反应焓变和熵变 |
您最近一年使用:0次
2021-02-20更新
|
187次组卷
|
2卷引用:湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题
10 . 下列有关说法正确的是
| A.吸热反应只有加热才能发生 |
| B.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH>0 |
| D.N2(g)+3H2(g)=2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
您最近一年使用:0次
2020-11-29更新
|
109次组卷
|
3卷引用:湖北省部分省重点中学2020-2021学年高二上学期期中联考化学试题



