2024高三下·全国·专题练习
1 . 研究CO2 加氢制CH4 对资源综合利用有重要意义。相关的主要化学反应如下:
Ⅰ.CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
Ⅲ.2CO(g)+2H2(g) CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=________ mol·L-1·min-1(用含a、b、V的代数式表示,下同),此时H2O(g) 的浓度为________ mol·L-1,反应Ⅱ的平衡常数为________ (列出计算式)。
Ⅰ.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2Ⅲ.2CO(g)+2H2(g)
 CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=
您最近一年使用:0次
2023高三·全国·专题练习
2 . 在2L密闭容器中进行反应: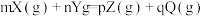 ,式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
,式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
已知 内
内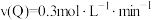 ,
, 。
。
(1)试确定以下物质的量:起始时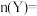
_______ ,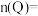
_______ 。
(2)化学方程式中m=_______ ,n=_______ ,p=_______ ,q=_______ 。
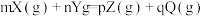 ,式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
,式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:| X | Y | Z | Q | |
| 起始/mol | 1.2 | 0 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
 内
内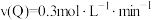 ,
, 。
。(1)试确定以下物质的量:起始时
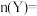
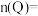
(2)化学方程式中m=
您最近一年使用:0次
2023高三·全国·专题练习
3 . 化学反应速率
(1)表示方法
通常用单位时间内反应物浓度的 1 或生成物浓度的 2 来表示。
(2)数学表达式及单位
v= ,单位为mol·L-1·min-1或mol·L-1·s-1。
,单位为mol·L-1·min-1或mol·L-1·s-1。
(3)化学反应速率与化学计量数的关系
同一反应在同一时间内,用不同物质来表示的反应速率可能 3 ,但反应速率的数值之比等于这些物质在化学方程式中的 4 之比。如在反应aA(g)+bB(g)⇌cC(g)+dD(g)中,存在v(A)∶v(B)∶v(C)∶v(D)=a∶b∶c∶d。
(4)同一化学反应中反应快慢的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能 5 ,所以比较反应的快慢不能只看数值的大小,而要进行一定的转化。
①看单位是否统一,若不统一,换算成相同的单位。
②换算成同一物质表示的速率,再比较数值的大小。
③比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB=cC+dD,比较 与
与 ,若
,若 >
> ,则A表示的反应速率比B的大。
,则A表示的反应速率比B的大。
(1)表示方法
通常用单位时间内反应物浓度的
(2)数学表达式及单位
v=
 ,单位为mol·L-1·min-1或mol·L-1·s-1。
,单位为mol·L-1·min-1或mol·L-1·s-1。(3)化学反应速率与化学计量数的关系
同一反应在同一时间内,用不同物质来表示的反应速率可能
(4)同一化学反应中反应快慢的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能
①看单位是否统一,若不统一,换算成相同的单位。
②换算成同一物质表示的速率,再比较数值的大小。
③比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB=cC+dD,比较
 与
与 ,若
,若 >
> ,则A表示的反应速率比B的大。
,则A表示的反应速率比B的大。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 我国力争在2060年前实现“碳中和”,综合利用CO2具有重要的意义。300MP、200oC条件下,CO2与H2反应可制得气态甲醇(CH3OH),其反应方程式为CO2+3H2 CH3OH+H2O(g)。
CH3OH+H2O(g)。
(1)该反应的能量变化如图所示:
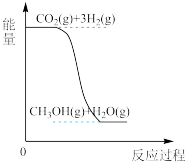
该反应是_______ 反应(填“吸热”或“放热”),判断的理由是 _______ 。
(2)为了加快该反应的速率,可以采取措施_______ (任写一种)。
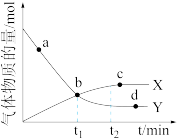
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表 的曲线是
的曲线是_______ (填“X”或“Y”),v(正)与v(逆)相等的点为_______ (填字母)。
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为_______ mol· L-1· min-1;
②2min末容器中H2的物质的量浓度_______ 。
 CH3OH+H2O(g)。
CH3OH+H2O(g)。(1)该反应的能量变化如图所示:

该反应是
(2)为了加快该反应的速率,可以采取措施
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表
 的曲线是
的曲线是
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内
 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为②2min末容器中H2的物质的量浓度
您最近一年使用:0次
2023·吉林长春·三模
名校
5 . 反应 的速率方程为
的速率方程为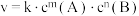 (k为速率常数,其中
(k为速率常数,其中 , A、R为常数,
, A、R为常数, 为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
 的速率方程为
的速率方程为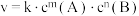 (k为速率常数,其中
(k为速率常数,其中 , A、R为常数,
, A、R为常数, 为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
为活化能,T为开氏温度,其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是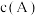 / / | 0.25 | 0.5 | 1 | 0.5 | 1 |
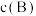 / / | 0.05 | 0.05 | 0.1 | 0.1 | 0.2 |
v/ | 1.6 | 3.2 | 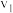 | 3.2 |  |
A.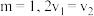 |
B. |
| C.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快 |
D.在过量的B存在时,A剩余12.5%所需的时间是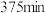 |
您最近一年使用:0次
2023高三·全国·专题练习
名校
6 . 一定条件下,在体积为10L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g),反应过程如图。下列说法不正确的是
2NH3(g),反应过程如图。下列说法不正确的是

 2NH3(g),反应过程如图。下列说法不正确的是
2NH3(g),反应过程如图。下列说法不正确的是
| A.t1min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间的变化关系 |
| C.0~8min,H2的平均反应速率v(H2)=0.01125mol•L-1•min-1 |
| D.10~12min,N2的平均反应速率v(N2)=0.0025mol•L-1•min-1 |
您最近一年使用:0次
23-24高三上·河南·阶段练习
7 . 一定条件下向10L的恒容密闭容器中通入2mol ,6mol
,6mol ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: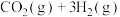

 ,经过10min时测得
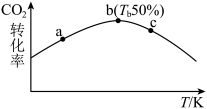
,经过10min时测得 的转化率与温度(T)的关系如图所示。下列分析中正确的是
的转化率与温度(T)的关系如图所示。下列分析中正确的是
 ,6mol
,6mol ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: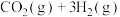

 ,经过10min时测得
,经过10min时测得 的转化率与温度(T)的关系如图所示。下列分析中正确的是
的转化率与温度(T)的关系如图所示。下列分析中正确的是
A.a点处对应体系中: |
B.与b点对应的反应,前10min内 |
C.该反应的 |
| D.当容器中气体密度保持不变时,表明该反应达到平衡状态 |
您最近一年使用:0次
22-23高一下·广东东莞·期中
名校
解题方法
8 . 一定温度下在2L密闭容器中进行着某一反应,X气体、Y气体的物质的量随时间变化的曲线如图,下列叙述正确的是
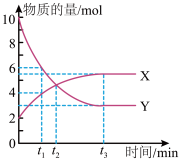
| A.反应的化学方程式为:2Y=X |
| B.t1min时,物质Y的转化率为60% |
| C.t2min时,反应物的正反应速率大于逆反应速率 |
| D.t3min时,反应停止 |
您最近一年使用:0次
2023·浙江·二模
名校
9 . 在恒温恒容条件下,发生反应 ,
,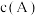 随时间的变化如图中曲线所示,其中
随时间的变化如图中曲线所示,其中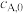 表示
表示 的初始浓度。下列说法
的初始浓度。下列说法不正确 的是
 ,
,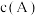 随时间的变化如图中曲线所示,其中
随时间的变化如图中曲线所示,其中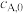 表示
表示 的初始浓度。下列说法
的初始浓度。下列说法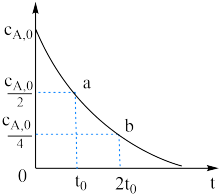
| A.a点的瞬时速率大于b点的瞬时速率 |
B.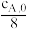 对应的时间为 对应的时间为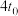 |
C.从a、b两点坐标可求得从 到 到 时间间隔内该化学反应的平均速率 时间间隔内该化学反应的平均速率 |
D.在不同时刻都存在关系: |
您最近一年使用:0次
2023-08-20更新
|
793次组卷
|
4卷引用:考点1 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
(已下线)考点1 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)浙江省名校协作体2022-2023学年高三二模化学试题广东省阳江市2023-2024学年高二上学期10月月考化学试题浙江省宁波市北仑中学2023-2024学年高二上学期期中考试化学试题
2023高三·全国·专题练习
名校
解题方法
10 . T0温度下,向2L真空密闭容器中加入N2O3固体,发生反应:N2O3(s) NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
 NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是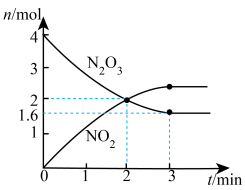
| A.X可能为N2 |
| B.0~2 min用N2O3表示的反应速率为1mol·min-1 |
| C.第2min时逆反应速率大于第4min时逆反应速率 |
| D.第4min时,保持温度和容积不变,向容器中再加入N2O3,混合气体颜色加深 |
您最近一年使用:0次
2023-08-19更新
|
1064次组卷
|
5卷引用:考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)选择题6-10河北省唐县第一中学2023-2024学年高二上学期9月月考化学试题安徽省安庆市岳西中学2023-2024学年高二上学期9月月考化学试题湖南省益阳市桃江县第四中学2023-2024学年高二上学期第一次月考化学试卷



