2020高三·全国·专题练习
解题方法
1 . 下列有关说法正确的是___________ 。
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
⑦浓度为1 mol·L-1的盐酸与过量的锌粉反应,若加入适量的CuSO4溶液,能减慢反应速率但又不影响氢气生成量
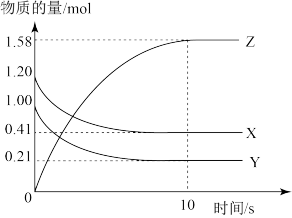
⑧一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图,则反应的化学方程式为X(g)+Y(g) Z(g)
Z(g)
⑨已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则 v(O2)=v(H2O)
v(O2)=v(H2O)
⑩分解水制氢气的工业制法之一是“硫碘循环法”,主要涉及下列反应:①SO2+2H2O+I2=H2SO4+2HI ②2HI H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
⑪某温度下,在容积一定的密闭容器中进行如下反应:2X(g)+Y(g) Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
⑫一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
⑦浓度为1 mol·L-1的盐酸与过量的锌粉反应,若加入适量的CuSO4溶液,能减慢反应速率但又不影响氢气生成量
⑧一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图,则反应的化学方程式为X(g)+Y(g)
 Z(g)
Z(g)
⑨已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则
 v(O2)=v(H2O)
v(O2)=v(H2O)⑩分解水制氢气的工业制法之一是“硫碘循环法”,主要涉及下列反应:①SO2+2H2O+I2=H2SO4+2HI ②2HI
 H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2
H2+I2 ③2H2SO4=2SO2+O2+2H2O,循环过程中产生1 mol O2的同时产生1 mol H2⑪某温度下,在容积一定的密闭容器中进行如下反应:2X(g)+Y(g)
 Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小
Z(g)+W(s) ΔH>0,则升高温度,正反应速率增大,逆反应速率减小⑫一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
2NO(g)在密闭容器中进行,恒压,充入He不改变化学反应速率
您最近一年使用:0次
名校
2 . 根据所学知识,回答下列问题:
(1)在反应N2(g)+3H2(g) 2NH3(g)中,若以N2表示的该反应的化学反应速率为0.2 mol/(L·min),则以H2表示此反应的化学反应速率为
2NH3(g)中,若以N2表示的该反应的化学反应速率为0.2 mol/(L·min),则以H2表示此反应的化学反应速率为 _____________ mol/(L·min)
(2)在5 L的恒容密闭容器中,充人0.1 mol N2和0.4 mol H2,在一定条件下发生反应,2s后测得N2的物质的量为0.09mol,则以NH3的浓度变化表示的反应速率为___________ mol/(L·s)
(3)将0.2 mol NH3充人容积为10 L的恒容密闭容器中,某温度下发生反应2NH3(g) N2(g) + 3H2(g),在0~2s内,消耗NH3的平均速率为0.002 mol/(L·s),则在2s时,容器中生成
N2(g) + 3H2(g),在0~2s内,消耗NH3的平均速率为0.002 mol/(L·s),则在2s时,容器中生成_____________ molH2,此时NH3的物质的量浓度为______________ mol/L。
(1)在反应N2(g)+3H2(g)
 2NH3(g)中,若以N2表示的该反应的化学反应速率为0.2 mol/(L·min),则以H2表示此反应的化学反应速率为
2NH3(g)中,若以N2表示的该反应的化学反应速率为0.2 mol/(L·min),则以H2表示此反应的化学反应速率为 (2)在5 L的恒容密闭容器中,充人0.1 mol N2和0.4 mol H2,在一定条件下发生反应,2s后测得N2的物质的量为0.09mol,则以NH3的浓度变化表示的反应速率为
(3)将0.2 mol NH3充人容积为10 L的恒容密闭容器中,某温度下发生反应2NH3(g)
 N2(g) + 3H2(g),在0~2s内,消耗NH3的平均速率为0.002 mol/(L·s),则在2s时,容器中生成
N2(g) + 3H2(g),在0~2s内,消耗NH3的平均速率为0.002 mol/(L·s),则在2s时,容器中生成
您最近一年使用:0次
2020-04-29更新
|
1083次组卷
|
6卷引用:第13讲 化学反应速率(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
(已下线)第13讲 化学反应速率(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)河北省承德市隆化县存瑞中学2019--2020学年高一下学期期中考试化学试题河北省邢台市2019-2020学年高一下学期期中考试化学试题陕西省西安市莲湖区2019-2020学年高一下学期期末联考试卷人教版2019必修第二册 第六章 第二节 第1课时 化学反应的速率河北省石家庄私立第一中学2020-2021学年高一下学期第二次调研考试化学试题
名校
3 . 根据图填空:
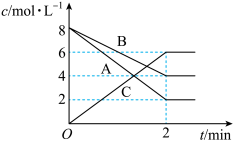
反应物是________ ;生成物是________ 。在2 min内A、B、C三者的反应速率值分别是____________ 、____________ 、____________ ,该反应的化学方程式是______________________ 。

反应物是
您最近一年使用:0次
2020-04-27更新
|
605次组卷
|
9卷引用:2018年9月4日 《每日一题》人教必修4-化学反应速率的计算
(已下线)2018年9月4日 《每日一题》人教必修4-化学反应速率的计算2015-2016学年山东省青岛市华侨中学高二上学期10月月考化学试卷新疆维吾尔自治区昌吉市第九中学2018-2019学年高二上学期期末考试化学试题【全国百强校】甘肃省天水市一中2018-2019学年高一(文)下学期第二学段考试化学试题江苏省东海县第二中学2019-2020学年高二下学期第一次学分认定测试化学试题安徽省亳州市涡阳县第九中学2018-2019学年高一下学期第四次月考(期末)化学试题北京师范大学珠海分校附属外国语学校2019-2020学年高一下学期期末考试化学试题(已下线)2.1 化学反应速率(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)2.1.1 化学反应速率——同步学习必备知识
4 . 解答下列问题:
Ⅰ.某同学做如下实验 图
图 ,以检验反应中的能量变化。
,以检验反应中的能量变化。
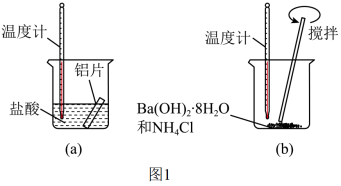


(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是______ 热反应;该反应中 ______ 能转化成 ______ 能。
(2)(b)中温度降低,下列各图 图
图 所表示的反应是(b)反应的是
所表示的反应是(b)反应的是 ______ 。
Ⅱ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图3所示。
(1)该反应中______ 是反应物,反应是 ______ 反应。
(2)反应开始到10s,用Z表示的反应速率为______  。
。
(3)反应开始到10s时,Y的物质的量浓度减少了______  。
。
(4)反应的化学方程式为______ 。
Ⅰ.某同学做如下实验
 图
图 ,以检验反应中的能量变化。
,以检验反应中的能量变化。 


(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
(2)(b)中温度降低,下列各图
 图
图 所表示的反应是(b)反应的是
所表示的反应是(b)反应的是 Ⅱ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图3所示。
(1)该反应中
(2)反应开始到10s,用Z表示的反应速率为
 。
。(3)反应开始到10s时,Y的物质的量浓度减少了
 。
。(4)反应的化学方程式为
您最近一年使用:0次
2020-02-26更新
|
147次组卷
|
2卷引用:2020届高三化学二轮复习实验题必练-化学平衡
解题方法
5 . (1)已知: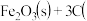 石墨
石墨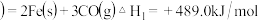
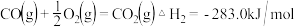
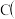 石墨
石墨
则4Fe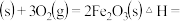
______
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图1所示:用Z表示的反应速率为______ 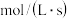 ,写出该反应的化学方程式
,写出该反应的化学方程式______ ,又反应开始到 10s时,Y 的转化率为______ 。

(3)图2为乙烷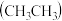 燃料电池的装置
燃料电池的装置 、B为多孔碳棒
、B为多孔碳棒 :
:______  填A或
填A或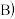 处电极入口通乙烷,其电极反应式为
处电极入口通乙烷,其电极反应式为______ 。
(4)用中和滴定法测定溶液碱溶液的浓度。
①滴定时,用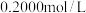 的盐酸来滴定待测溶液,若选用甲基橙作指示剂,滴定终点的判断方法是
的盐酸来滴定待测溶液,若选用甲基橙作指示剂,滴定终点的判断方法是______ 。
②下列操作 其他操作正确
其他操作正确 造成测定结果偏低是
造成测定结果偏低是______
A.滴定终点读数时俯视读数
B.酸式滴定管使用前水洗后未用标准盐酸溶液润洗
C.锥形瓶水洗用待测液润洗
D.酸式滴定管尖嘴部分有气泡,滴定后消失
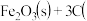 石墨
石墨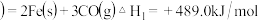
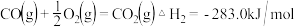
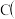 石墨
石墨
则4Fe
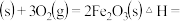
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图1所示:用Z表示的反应速率为
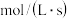 ,写出该反应的化学方程式
,写出该反应的化学方程式
(3)图2为乙烷
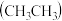 燃料电池的装置
燃料电池的装置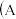 、B为多孔碳棒
、B为多孔碳棒 :
: 填A或
填A或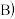 处电极入口通乙烷,其电极反应式为
处电极入口通乙烷,其电极反应式为(4)用中和滴定法测定溶液碱溶液的浓度。
①滴定时,用
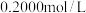 的盐酸来滴定待测溶液,若选用甲基橙作指示剂,滴定终点的判断方法是
的盐酸来滴定待测溶液,若选用甲基橙作指示剂,滴定终点的判断方法是②下列操作
 其他操作正确
其他操作正确 造成测定结果偏低是
造成测定结果偏低是A.滴定终点读数时俯视读数
B.酸式滴定管使用前水洗后未用标准盐酸溶液润洗
C.锥形瓶水洗用待测液润洗
D.酸式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
2019高二上·全国·专题练习
6 . 向体积为10 L的恒容密闭容器中通入3 mol X,在一定温度下发生如下反应:2X(g)  Y(g)+aZ(g),经5 min后反应达到反应限度(即达到平衡状态)。
Y(g)+aZ(g),经5 min后反应达到反应限度(即达到平衡状态)。
(1)平衡时,测得容器内的压强为起始时的1.2倍,此时X的物质的量浓度为0.24mol·L-1,则方程式中a=_____ ;用Y表示的反应速率为_____ mol·L-1·min-1。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得容器内的反应速率如下表所示:
若四个容器中仅反应温度不同,则反应温度最低的是_____ (填序号,下同);若四个容器中仅有一个加入了催化剂,则该容器是______ 。
 Y(g)+aZ(g),经5 min后反应达到反应限度(即达到平衡状态)。
Y(g)+aZ(g),经5 min后反应达到反应限度(即达到平衡状态)。(1)平衡时,测得容器内的压强为起始时的1.2倍,此时X的物质的量浓度为0.24mol·L-1,则方程式中a=
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得容器内的反应速率如下表所示:
| 容器 | 反应速率 |
| ① | v(X)=3.5mol·L-1·min-1 |
| ② | v(Y)=2mol·L-1·min-1 |
| ③ | v(Z)=4.5mol·L-1·min-1 |
| ④ | v(X)=0.075mol·L-1·s-1 |
若四个容器中仅反应温度不同,则反应温度最低的是
您最近一年使用:0次
2019高一下·全国·专题练习
7 . Ⅰ.将等质量的锌片和铜片用导线相连并插入500 mL CuSO4溶液中构成如图所示的装置。

(1)该装置中发生反应的离子方程式为______________ 。
(2)若锌2 min后的质量减少1.3 g,则导线中流过的电子为________ mol。
(3)若将该装置的电解质溶液换为FeCl3溶液,则其正极反应式为____________________ 。
Ⅱ.向2 L的密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g) pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应至2 min时,A的物质的量减少了
v(A);反应至2 min时,A的物质的量减少了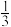 a mol,B的浓度减少了
a mol,B的浓度减少了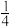 a mol·L−1,同时有a mol D生成。
a mol·L−1,同时有a mol D生成。
(1)0~2 min内,v(A)=________ 。
(2)该化学方程式中,y=________ 。
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较,反应速率_______ (填“增大”、“减小”或“不变”),理由是_______________ 。

(1)该装置中发生反应的离子方程式为
(2)若锌2 min后的质量减少1.3 g,则导线中流过的电子为
(3)若将该装置的电解质溶液换为FeCl3溶液,则其正极反应式为
Ⅱ.向2 L的密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)
 pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应至2 min时,A的物质的量减少了
v(A);反应至2 min时,A的物质的量减少了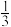 a mol,B的浓度减少了
a mol,B的浓度减少了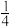 a mol·L−1,同时有a mol D生成。
a mol·L−1,同时有a mol D生成。(1)0~2 min内,v(A)=
(2)该化学方程式中,y=
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较,反应速率
您最近一年使用:0次
8 . 恒温恒容下,将2mol气体A和2mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g) xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_____________ 。
(2)x=________ 。
(3)下列各项可作为该反应达到平衡状态的标志是_________ (填字母)。
A.压强不再变化 B.气体密度不再变化
C.气体平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为2:1
 xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)下列各项可作为该反应达到平衡状态的标志是
A.压强不再变化 B.气体密度不再变化
C.气体平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为2:1
您最近一年使用:0次
2019-01-22更新
|
131次组卷
|
3卷引用:2.2.2 化学平衡状态(2)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
(已下线)2.2.2 化学平衡状态(2)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)【校级联考】甘肃省宁县2018-2019学年高二上学期期末联考化学试题甘肃省岷县第二中学2020-2021学年高二上学期期末考试化学试题
2018高二上·全国·专题练习
9 . 一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,生成的产物也是气体,反应中各物质的物质的量变化如图所示。请回答下列问题:

(1)反应进行到6 s时,B的平均反应速率为_____________ 。
(2)该反应的化学方程式为__________________ 。
(3)若该反应分别在甲、乙、丙、丁四个相同的密闭容器中进行,经相同的一段时间后,测得四个容器中的反应速率分别为
甲:v(A)=0.75 mol·L−1·min−1
乙:v(B)=0.01 mol·L−1·s−1
丙:v(C)=0.40 mol·L−1·min−1
丁:v(D)=0.45 mol·L−1·min−1
则甲、乙、丙、丁四个容器中反应速率由大到小的顺序为_____________________ 。

(1)反应进行到6 s时,B的平均反应速率为
(2)该反应的化学方程式为
(3)若该反应分别在甲、乙、丙、丁四个相同的密闭容器中进行,经相同的一段时间后,测得四个容器中的反应速率分别为
甲:v(A)=0.75 mol·L−1·min−1
乙:v(B)=0.01 mol·L−1·s−1
丙:v(C)=0.40 mol·L−1·min−1
丁:v(D)=0.45 mol·L−1·min−1
则甲、乙、丙、丁四个容器中反应速率由大到小的顺序为
您最近一年使用:0次
10 . 将等物质的量的A、B、C、D四种物质混和,发生如下反应:
aA+bB cC(s)+dD
cC(s)+dD
当反应进行一定时间后,测得A减少了n mol,B减少了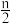 mol,C增加了
mol,C增加了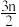 mol,D增加了n mol,此时达到化学平衡:
mol,D增加了n mol,此时达到化学平衡:
(1) 该化学方程式中各物质的化学计量数为:
a=_________ 、b=__________ 、c=___________ 、d=___________ 。
(2) 若只改变压强,反应速度发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A________ B___________ D_________
(3)若只升高温度,反应一段时间后,测知四种物质其物质的量又达到相等则该反应为__________ 反应(填“放热”或“吸热”)。
aA+bB
 cC(s)+dD
cC(s)+dD当反应进行一定时间后,测得A减少了n mol,B减少了
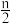 mol,C增加了
mol,C增加了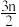 mol,D增加了n mol,此时达到化学平衡:
mol,D增加了n mol,此时达到化学平衡:(1) 该化学方程式中各物质的化学计量数为:
a=
(2) 若只改变压强,反应速度发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A
(3)若只升高温度,反应一段时间后,测知四种物质其物质的量又达到相等则该反应为
您最近一年使用:0次
2017-02-17更新
|
175次组卷
|
3卷引用:6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)2016-2017学年河南省师大附中高二上期中化学试卷2016-2017学年内蒙古集宁一中高二上期中化学卷



