解题方法
1 . 下列实验中,操作、现象及结论都正确,且有因果关系的是
选项 | 实验操作 | 现象 | 结论 |
A | 将 | 溶液pH变大 | 稀释后, |
B | 取两支试管,分别加入2mL5%的双氧水,试管1中加入 | 试管1产生气泡快 | 加入 |
C | 向含有ZnS和 | 生成黑色沉淀 |
|
D | 用pH试纸分别测定同浓度 | 测得NaClO溶液pH大 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 一定条件下CO与NO反应可实现汽车尾气净化,所涉及的三段反应历程及各物质的相对能量如图所示(TS代表过渡态,IM表示反应过程中的复杂中间产物,每段历程的反应物相对总能量定义为0)。下列说法正确的是


| A.由反应历程图可判断过渡态的相对能量:TS1>TS2>TS3 |
| B.采用对反应③选择性高的催化剂可以避免尾气中出现N2O |
| C.反应历程中反应②决定尾气转化的快慢 |
D.2NO(g) + 2CO(g) N2(g) + 2CO2(g) ΔH= – 621.9kJ·mol-1 N2(g) + 2CO2(g) ΔH= – 621.9kJ·mol-1 |
您最近一年使用:0次
名校
3 . 在一定条件下,一定浓度的甲酸溶液在密闭容器中发生分解反应(分解产物均溶于水):
Ⅰ.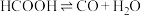 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
Ⅰ.
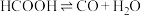 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
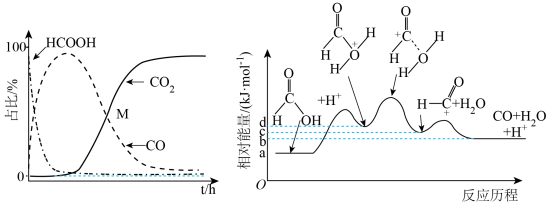
A.反应Ⅰ中 是该反应的催化剂,平衡前适当提高 是该反应的催化剂,平衡前适当提高 浓度有利于加快反应Ⅰ的速率 浓度有利于加快反应Ⅰ的速率 |
B.反应Ⅰ的热化学方程式可表示为: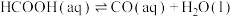 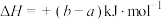 |
C.适当升高温度可降低平衡时CO和 的比例 的比例 |
| D.在反应Ⅰ的反应历程中,存在3种中间产物 |
您最近一年使用:0次
2024-01-12更新
|
343次组卷
|
3卷引用:浙江省宁波市镇海中学2023-2024学年高三上学期首考12月模拟卷化学试题
浙江省宁波市镇海中学2023-2024学年高三上学期首考12月模拟卷化学试题(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)湖南省衡阳市第八中学2024届高三下学期高考模拟预测化学试题
名校
解题方法
4 .  与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与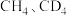 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
 与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与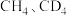 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是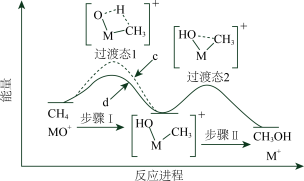
A. 与 与 反应的能量变化应为图中曲线d 反应的能量变化应为图中曲线d |
| B.步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是Ⅱ |
C. 与 与 反应,氘代甲醇的产量: 反应,氘代甲醇的产量: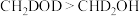 |
D.若 与 与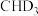 反应,生成的氘代甲醇有2种 反应,生成的氘代甲醇有2种 |
您最近一年使用:0次
2023-12-15更新
|
391次组卷
|
5卷引用:浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题
浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)河南省郑州市宇华实验学校2023-2024学年高三上学期1月期末化学试题(已下线)选择题11-15
名校
解题方法
5 . I. 可作大型船舶绿色燃科,可由CO或
可作大型船舶绿色燃科,可由CO或 制备。工业用
制备。工业用 制备
制备 原理如下:
原理如下:
反应1:
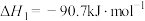
反应2:
 (副反应)
(副反应)
(1)反应3:
 ,该反应自发的条件
,该反应自发的条件________ (填“高温自发”、“低温自发”、“任意温度自发”或“任意温度不自发”)。
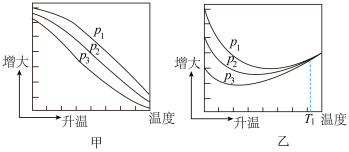
(2)不同压强下,按照 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知: 的平衡转化率
的平衡转化率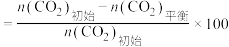 %
%
 的平衡产率
的平衡产率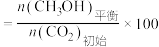 %
%
其中纵坐标表示 平衡转化率的是图
平衡转化率的是图___________ (填“甲”或“乙”);图乙中 温度时,三条曲线几乎交于一点且随温度升高而变大的原因是
温度时,三条曲线几乎交于一点且随温度升高而变大的原因是___________ 。
(3)在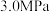 ,有催化剂的条件下,向密闭容器中充入
,有催化剂的条件下,向密闭容器中充入 和
和 ,
, 的平衡转化率与
的平衡转化率与 、CO的选择性随温度的变化如图所示,
、CO的选择性随温度的变化如图所示,
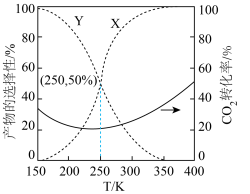
已知: (或CO)的选择性
(或CO)的选择性 %。
%。
若250℃反应达到平衡后, 的物质的量为
的物质的量为 ,则反应2的
,则反应2的
___________ 。
已知:对于气相反应,用组分B的平衡压强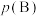 代替物质的量浓度
代替物质的量浓度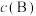 也可以表示平衡常数,记作
也可以表示平衡常数,记作 ,如
,如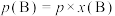 ,p为平衡压强,
,p为平衡压强,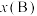 为平衡系统中B的物质的量分数。
为平衡系统中B的物质的量分数。
Ⅱ.已知水煤气反应:
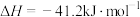 。
。
(4)以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,用两个化学方程式表示该催化反应历程(反应机理):
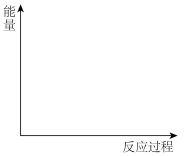
步骤I:___________ ;
步骤Ⅱ:___________ 。
(5)画出该反应无催化剂和有催化剂的能量与反应历程的关系图___________ 。
 可作大型船舶绿色燃科,可由CO或
可作大型船舶绿色燃科,可由CO或 制备。工业用
制备。工业用 制备
制备 原理如下:
原理如下:反应1:

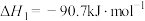
反应2:

 (副反应)
(副反应)(1)反应3:

 ,该反应自发的条件
,该反应自发的条件(2)不同压强下,按照
 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知:
 的平衡转化率
的平衡转化率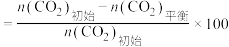 %
% 的平衡产率
的平衡产率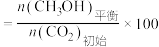 %
%其中纵坐标表示
 平衡转化率的是图
平衡转化率的是图 温度时,三条曲线几乎交于一点且随温度升高而变大的原因是
温度时,三条曲线几乎交于一点且随温度升高而变大的原因是(3)在
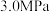 ,有催化剂的条件下,向密闭容器中充入
,有催化剂的条件下,向密闭容器中充入 和
和 ,
, 的平衡转化率与
的平衡转化率与 、CO的选择性随温度的变化如图所示,
、CO的选择性随温度的变化如图所示,
已知:
 (或CO)的选择性
(或CO)的选择性 %。
%。若250℃反应达到平衡后,
 的物质的量为
的物质的量为 ,则反应2的
,则反应2的
已知:对于气相反应,用组分B的平衡压强
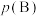 代替物质的量浓度
代替物质的量浓度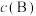 也可以表示平衡常数,记作
也可以表示平衡常数,记作 ,如
,如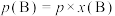 ,p为平衡压强,
,p为平衡压强,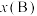 为平衡系统中B的物质的量分数。
为平衡系统中B的物质的量分数。Ⅱ.已知水煤气反应:

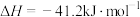 。
。(4)以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,用两个化学方程式表示该催化反应历程(反应机理):

步骤I:
步骤Ⅱ:
(5)画出该反应无催化剂和有催化剂的能量与反应历程的关系图
您最近一年使用:0次
2023-12-13更新
|
113次组卷
|
2卷引用:浙江省杭州第二中学2023-2024学年高二上学期期中考试化学试题
解题方法
6 . 乙醇在浓硫酸做催化剂的条件下发生脱水反应,反应历程和能量变化关系图如下,下列说法正确的是。
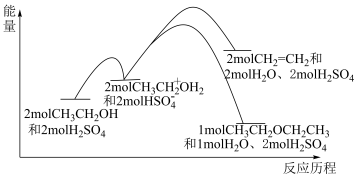
| A.采用较低温度,可获得产率更高的乙醚 |
| B.在上述相同条件下,正丙醇比异丙醇更容易反应 |
| C.为了获得更多的乙烯,温度越高越好 |
| D.选择合适的催化剂,可提高平衡时乙烯的产率 |
您最近一年使用:0次
名校
解题方法
7 . N2O是《联合国气候变化框架公约》所列六种温室气体之一。CO和N2O在Fe+作用下转化为N2和CO2,反应的能量变化及反应历程如图所示,两步基元反应为:① N2O+Fe +=N2+FeO+ K1,②CO+FeO+=CO2+Fe+ K2。下列说法不正确的是
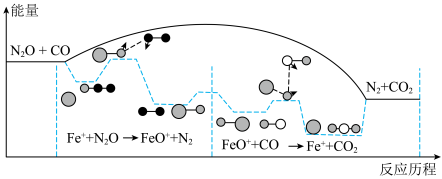

| A.该反应ΔH<0 |
| B.两步反应中,决定总反应速率的是反应① |
| C.升高温度,可提高 N2O 的平衡转化率 |
| D.Fe+增大了活化分子百分数,加快了化学反应速率,但不改变反应的ΔH |
您最近一年使用:0次
2023-07-24更新
|
820次组卷
|
5卷引用:浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题
浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题河南省宜阳县第一高级中学2023-2024学年高二上学期9月开学考试化学试题(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题11-14
8 .  是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某 (Ⅱ)催化剂(用
(Ⅱ)催化剂(用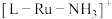 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。
,其反应机理如图所示。
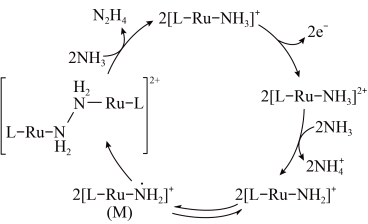
下列说法错误的是
 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某
是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某 (Ⅱ)催化剂(用
(Ⅱ)催化剂(用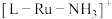 表示)能高效电催化氧化
表示)能高效电催化氧化 合成
合成 ,其反应机理如图所示。
,其反应机理如图所示。
下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅱ)被氧化至 (Ⅲ)后,配体 (Ⅲ)后,配体 失去质子能力增强 失去质子能力增强 |
B.M中 的化合价为 的化合价为 |
| C.该过程有非极性键的形成 |
D.该过程的总反应式: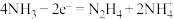 |
您最近一年使用:0次
2023-06-16更新
|
9366次组卷
|
17卷引用:浙江省名校协作体2023-2024学年高三上学期开学适应性考试化学试题
浙江省名校协作体2023-2024学年高三上学期开学适应性考试化学试题2023年高考湖南卷化学真题(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)第3讲 氧化还原反应(已下线)2023年湖南卷高考真题变式题(选择题11-14)河北省石家庄市正定中学2022- 2023学年高二下学期期末考试化学试题(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)湖北省华中师范大学第一附属中学2023-2024学年高二上学期10月月考化学试题陕西省西安中学2023-2024学年高三(实验版)上学期12月练考理科综合试题(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)江西省宜春市丰城市第九中学2023-2024学年高一上学期1月期末化学试题
解题方法
9 . 工业上,以 为原料,通过不同反应生产更高价值的
为原料,通过不同反应生产更高价值的 。
。
I. 直接分解生产
直接分解生产 :
:
反应①:
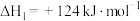
反应②: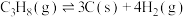

请回答:
(1)恒温下,往恒容(10L)反应釜中通入4mol (g)(仅考虑发生上述反应)。某时刻
(g)(仅考虑发生上述反应)。某时刻 转化率为20%,
转化率为20%, 选择性为40%,则该时刻反应①的浓度商
选择性为40%,则该时刻反应①的浓度商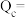
_______ 。
(2)下列说法正确的是_______。
(3)研究表明,在固体催化剂N存在下,反应①分三步进行,生成 步骤的活化能远大于生成
步骤的活化能远大于生成 步骤的活化能,且开始一段时间内
步骤的活化能,且开始一段时间内 与
与 的生成速率几乎相同(不考虑反应②)。画出步骤2和步骤3生成产物的反应过程能量示意图
的生成速率几乎相同(不考虑反应②)。画出步骤2和步骤3生成产物的反应过程能量示意图_______ 。

II. 辅助
辅助 生产
生产 :
:
反应③:
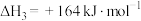
恒温恒压下, 和
和 按物质的量之比1:1以一定流速通入装有某复合催化剂的反应器中,反应过程如图所示:
按物质的量之比1:1以一定流速通入装有某复合催化剂的反应器中,反应过程如图所示:

(4)关于反应过程,下列说法正确的是_______。
(5)对该反应器催化剂表面上CO的生成速率和 的消耗速率进行测定,所得实验结果如图2,请结合具体反应说明CO的生成速率和
的消耗速率进行测定,所得实验结果如图2,请结合具体反应说明CO的生成速率和 的消耗速率不相等的可能原因
的消耗速率不相等的可能原因_______ 。

 为原料,通过不同反应生产更高价值的
为原料,通过不同反应生产更高价值的 。
。I.
 直接分解生产
直接分解生产 :
:反应①:

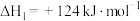
反应②:
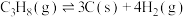

请回答:
(1)恒温下,往恒容(10L)反应釜中通入4mol
 (g)(仅考虑发生上述反应)。某时刻
(g)(仅考虑发生上述反应)。某时刻 转化率为20%,
转化率为20%, 选择性为40%,则该时刻反应①的浓度商
选择性为40%,则该时刻反应①的浓度商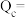
(2)下列说法正确的是_______。
| A.反应①能自发进行的条件是低温 |
| B.温度升高,反应②的平衡常数增大 |
| C.压强增大,活化分子百分数增多,导致反应①速率加快 |
| D.可通过C(s)的物质的量不再变化判断反应②达到平衡状态 |
 步骤的活化能远大于生成
步骤的活化能远大于生成 步骤的活化能,且开始一段时间内
步骤的活化能,且开始一段时间内 与
与 的生成速率几乎相同(不考虑反应②)。画出步骤2和步骤3生成产物的反应过程能量示意图
的生成速率几乎相同(不考虑反应②)。画出步骤2和步骤3生成产物的反应过程能量示意图
II.
 辅助
辅助 生产
生产 :
:反应③:

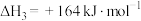
恒温恒压下,
 和
和 按物质的量之比1:1以一定流速通入装有某复合催化剂的反应器中,反应过程如图所示:
按物质的量之比1:1以一定流速通入装有某复合催化剂的反应器中,反应过程如图所示:
(4)关于反应过程,下列说法正确的是_______。
A.M可循环利用, 不可循环利用 不可循环利用 |
| B.过程1作用力a是氢键,过程2涉及极性键的形成和断裂 |
| C.温度升高,过程1和过程2的反应速率均加快,总反应速率一定加快 |
D.其他条件不变,更换不同催化剂,同样生产1mol  (g)所需能量不一定相同 (g)所需能量不一定相同 |
 的消耗速率进行测定,所得实验结果如图2,请结合具体反应说明CO的生成速率和
的消耗速率进行测定,所得实验结果如图2,请结合具体反应说明CO的生成速率和 的消耗速率不相等的可能原因
的消耗速率不相等的可能原因
您最近一年使用:0次
10 . 对苯二甲酸(TPA)是生产聚酯的主要原料。实验中,将初始浓度为0.08mol/L对甲基苯甲酸(p-TA)放入反应器中(用醋酸作为溶剂),在Co-Mn-Br的复合催化剂作用下进行反应,反应温度为186℃,反应过程中有充足的氧气供应,对甲基苯甲酸(p-TA)按照如下的路径发生反应:
 且有
且有
已知对甲基苯甲酸(p-TA)氧化的活化能比对醛基苯甲酸(4-CBA)氧化的活化能大得多。反应10min后,取样分析,对甲基苯甲酸(p-TA)和对醛基苯甲酸(4-CBA)含量基本为零。请回答:
(1)下列说法正确的是___________
(2)画出上述过程中p-TA制备TPA的物质相对能量-反应过程的示意图_________

(3)某研究小组进行了186℃下p-TA液相氧化反应并绘制了各物质浓度随时间的变化图像。
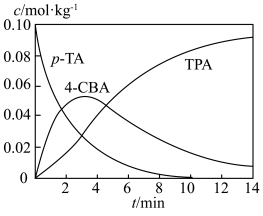
Ⅰ.已知图像中4-CBA的曲线有误,请说明错误的理由:___________ 。
Ⅱ.已知有两种溶剂a与b,p-TA、4-CBA和TPA在其中的溶解情况如下表所示,现欲收集反应的中间产物,选择溶剂___________ (填“a”或“b”)
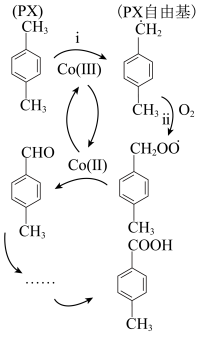
(4)已知原料对甲基苯甲酸(p-TA)可通过对二甲苯(PX)制取,PX液相氧化遵循自由基机理,部分反应历程如下所示,下列说法正确的是___________
 且有
且有
已知对甲基苯甲酸(p-TA)氧化的活化能比对醛基苯甲酸(4-CBA)氧化的活化能大得多。反应10min后,取样分析,对甲基苯甲酸(p-TA)和对醛基苯甲酸(4-CBA)含量基本为零。请回答:
(1)下列说法正确的是___________
A.反应Ⅰ 的平衡常数表达式 的平衡常数表达式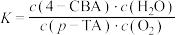 |
| B.CO-Mn-Br催化剂能改变反应历程 |
| C.相同条件下温度升高,反应Ⅰ的速率减慢,反应Ⅱ的速率加快 |
D.升高温度,副产物 的含量会增大 的含量会增大 |

(3)某研究小组进行了186℃下p-TA液相氧化反应并绘制了各物质浓度随时间的变化图像。

Ⅰ.已知图像中4-CBA的曲线有误,请说明错误的理由:
Ⅱ.已知有两种溶剂a与b,p-TA、4-CBA和TPA在其中的溶解情况如下表所示,现欲收集反应的中间产物,选择溶剂
| 溶解度 | 反应物质 | |||
| p-TA | 4-CBA | TPA | ||
| 溶剂 | a | 可溶 | 易溶 | 可溶 |
| b | 易溶 | 难溶 | 可溶 | |

A.Co(Ⅲ)使苯环上甲基的C-H键断裂生成PX自由基和 |
| B.该反应中Co(Ⅲ)作为催化剂 |
| C.PX自由基在反应ⅱ中发生还原反应 |
| D.该历程中原料的原子利用率达到100% |
您最近一年使用:0次

 溶液由
溶液由 稀释到
稀释到 ,测溶液pH
,测溶液pH 的水解程度增大
的水解程度增大 溶液2滴,试管2中加入
溶液2滴,试管2中加入
 时,双氧水分解反应的活化能较小
时,双氧水分解反应的活化能较小 的悬浊液中滴加
的悬浊液中滴加 溶液
溶液
 和NaClO溶液的pH
和NaClO溶液的pH 水解程度大于
水解程度大于


