1 .  催化重整能够有效去除大气中的
催化重整能够有效去除大气中的 ,是实现“碳中和”的重要途径之一,发生的反应如下:
,是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应:

积炭反应I: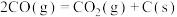

积炭反应II:

在恒压、起始投料比 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
 催化重整能够有效去除大气中的
催化重整能够有效去除大气中的 ,是实现“碳中和”的重要途径之一,发生的反应如下:
,是实现“碳中和”的重要途径之一,发生的反应如下:重整反应:


积炭反应I:
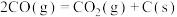

积炭反应II:


在恒压、起始投料比
 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
| A.升高温度积碳反应I,正反应速率减小,逆反应速率增大,平衡逆向移动 |
B.曲线B表示 平衡时物质的量随温度的变化 平衡时物质的量随温度的变化 |
C.积炭会导致催化剂失活,降低 的平衡转化率 的平衡转化率 |
D.低于600℃时,降低温度有利于减少积炭的量并去除 气体 气体 |
您最近一年使用:0次
名校
2 . 氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4=2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为___________ 。
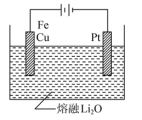
②CuFe2O4可用电化学方法得到,其原理如图所示,则阳极的电极反应式为___________ 。
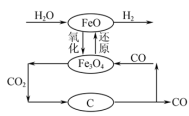
(2)可利用FeO/Fe3O4之间的相互转化,来裂解水制取氢气,其制氢流程如图所示。该工艺制氢的总反应为C(s)+H2O(g)=CO(g)+H2(g),对比水和碳在高温下直接接触反应制氢,分析该工艺制氢的最大优点是___________ 。
(3)硼氢化钠(NaBH4)的强碱溶液在催化剂作用下与水反应可获取氢气,其可能反应机理如图所示。已知:常温下,NaB(OH)4在水中的溶解度不大,易以NaBO2形式结晶析出。
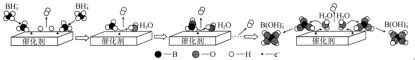
①若用D2O代替H2O,依据反应机理,则反应后生成的气体中含有___________ 。
②其他条件相同时,测得平均每克催化剂使用量下,NaBH4的浓度和放氢速率的变化关系如图所示。随着NaBH4浓度的增大,放氢速率先增大后减小,导致放氢速率下降的原因可能是___________ 。

(1)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4=2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图所示,则阳极的电极反应式为

(2)可利用FeO/Fe3O4之间的相互转化,来裂解水制取氢气,其制氢流程如图所示。该工艺制氢的总反应为C(s)+H2O(g)=CO(g)+H2(g),对比水和碳在高温下直接接触反应制氢,分析该工艺制氢的最大优点是

(3)硼氢化钠(NaBH4)的强碱溶液在催化剂作用下与水反应可获取氢气,其可能反应机理如图所示。已知:常温下,NaB(OH)4在水中的溶解度不大,易以NaBO2形式结晶析出。

①若用D2O代替H2O,依据反应机理,则反应后生成的气体中含有
②其他条件相同时,测得平均每克催化剂使用量下,NaBH4的浓度和放氢速率的变化关系如图所示。随着NaBH4浓度的增大,放氢速率先增大后减小,导致放氢速率下降的原因可能是

您最近一年使用:0次
3 . 二氧化碳合成二甲醚的主要反应有:
Ⅰ.
Ⅱ.
Ⅲ.
一定温度下,将 、
、 和双催化剂(通常由甲醇合成催化剂和甲醇脱水制醚催化剂组成),加入1L密闭容器中充分接触反应,测得各产物占所有含碳物质的物质的量分数(例:CO的物质的量分数
和双催化剂(通常由甲醇合成催化剂和甲醇脱水制醚催化剂组成),加入1L密闭容器中充分接触反应,测得各产物占所有含碳物质的物质的量分数(例:CO的物质的量分数 )随时间变化如图所示
)随时间变化如图所示
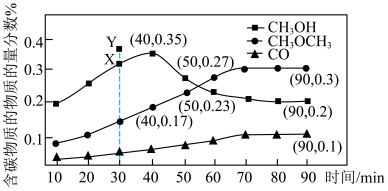
下列说法正确的是
Ⅰ.

Ⅱ.

Ⅲ.

一定温度下,将
 、
、 和双催化剂(通常由甲醇合成催化剂和甲醇脱水制醚催化剂组成),加入1L密闭容器中充分接触反应,测得各产物占所有含碳物质的物质的量分数(例:CO的物质的量分数
和双催化剂(通常由甲醇合成催化剂和甲醇脱水制醚催化剂组成),加入1L密闭容器中充分接触反应,测得各产物占所有含碳物质的物质的量分数(例:CO的物质的量分数 )随时间变化如图所示
)随时间变化如图所示
下列说法正确的是
A.40min前, |
| B.30min时,使用活性更高的甲醇合成催化剂,有可能使图中的X点升至Y点 |
C.40min后, 物质的量分数减小,原因可能是反应Ⅰ向逆反应方向移动 物质的量分数减小,原因可能是反应Ⅰ向逆反应方向移动 |
D.90min时, 的转化率为60% 的转化率为60% |
您最近一年使用:0次
名校
解题方法
4 . 肼( )及其衍生物的合成与利用具有重要意义。
)及其衍生物的合成与利用具有重要意义。
(1)“肼合成酶”以其中的 “配合物为催化中心,可将
“配合物为催化中心,可将 与
与 转化为肼,其反应历程如图所示。
转化为肼,其反应历程如图所示。
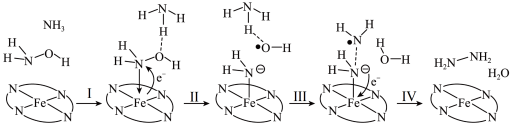
上图所示的反应步骤Ⅱ中Fe元素化合价的变化可描述为___________ 。
②将 替换为
替换为 ,反应所得产物的化学式为
,反应所得产物的化学式为___________ 。
(2)在碱性条件下,水合肼( )在催化剂Rh(铑)g-
)在催化剂Rh(铑)g- 作用下发生如下分解反应:
作用下发生如下分解反应:
反应Ⅰ: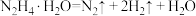
反应Ⅱ: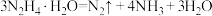
转化频率(TOF)能反映催化剂的性能。
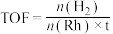 (t为反应时间),保持温度不变,相同时间内反应中不同
(t为反应时间),保持温度不变,相同时间内反应中不同 对应的TOF如图所示。
对应的TOF如图所示。
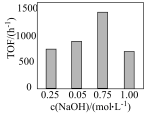
①催化剂载体g- 可由三聚氰胺(
可由三聚氰胺(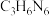 )在空气中焙烧得到。已知
)在空气中焙烧得到。已知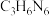 具有六元环结构,其结构简式可表示为
具有六元环结构,其结构简式可表示为___________ 。
②TOF随 变化的原因是
变化的原因是___________ 。
(3)相同条件下,测得 诱导肼、甲肼(
诱导肼、甲肼(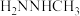 )和偏二甲肼[
)和偏二甲肼[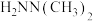 ]低温反应(均为吸热反应)产物与反应物能量差
]低温反应(均为吸热反应)产物与反应物能量差 、反应速率常数k值(k越大,反应越快)如下表。
、反应速率常数k值(k越大,反应越快)如下表。
①请补充上表所缺反应产物的结构简式___________ 。
②相较甲肼而言,肼、偏二甲肼与 的反应效果不佳的原因分别是
的反应效果不佳的原因分别是___________ 。
(4)液态肼也可以作为燃料电池,如图一种肼燃料电池,写成负极的电极反应___________ 。

 )及其衍生物的合成与利用具有重要意义。
)及其衍生物的合成与利用具有重要意义。(1)“肼合成酶”以其中的
 “配合物为催化中心,可将
“配合物为催化中心,可将 与
与 转化为肼,其反应历程如图所示。
转化为肼,其反应历程如图所示。
上图所示的反应步骤Ⅱ中Fe元素化合价的变化可描述为
②将
 替换为
替换为 ,反应所得产物的化学式为
,反应所得产物的化学式为(2)在碱性条件下,水合肼(
 )在催化剂Rh(铑)g-
)在催化剂Rh(铑)g- 作用下发生如下分解反应:
作用下发生如下分解反应:反应Ⅰ:
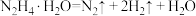
反应Ⅱ:
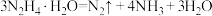
转化频率(TOF)能反映催化剂的性能。
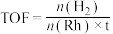 (t为反应时间),保持温度不变,相同时间内反应中不同
(t为反应时间),保持温度不变,相同时间内反应中不同 对应的TOF如图所示。
对应的TOF如图所示。
①催化剂载体g-
 可由三聚氰胺(
可由三聚氰胺(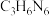 )在空气中焙烧得到。已知
)在空气中焙烧得到。已知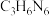 具有六元环结构,其结构简式可表示为
具有六元环结构,其结构简式可表示为②TOF随
 变化的原因是
变化的原因是(3)相同条件下,测得
 诱导肼、甲肼(
诱导肼、甲肼(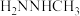 )和偏二甲肼[
)和偏二甲肼[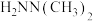 ]低温反应(均为吸热反应)产物与反应物能量差
]低温反应(均为吸热反应)产物与反应物能量差 、反应速率常数k值(k越大,反应越快)如下表。
、反应速率常数k值(k越大,反应越快)如下表。| 燃料 | 反应产物 |  | k值 |
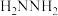 | 5.73 | 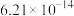 | |
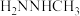 | 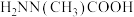 | 14.15 | 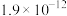 |
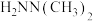 |  | 47.81 | - |
②相较甲肼而言,肼、偏二甲肼与
 的反应效果不佳的原因分别是
的反应效果不佳的原因分别是(4)液态肼也可以作为燃料电池,如图一种肼燃料电池,写成负极的电极反应

您最近一年使用:0次
名校
解题方法
5 . 选择性催化还原法(SCR法)去除 是脱硝问题研究的热点,催化剂的选取是技术的核心。
是脱硝问题研究的热点,催化剂的选取是技术的核心。
(1)以 为催化剂的催化原理:
为催化剂的催化原理: 与
与 形成能提供氢离子的酸性位(如图所示),
形成能提供氢离子的酸性位(如图所示), 吸附在酸性位上生成中间体继续与NO反应。
吸附在酸性位上生成中间体继续与NO反应。
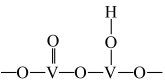
①五价钒在pH为10~13的溶液中会以焦钒酸根( )形式存在,请写出该离子的结构式
)形式存在,请写出该离子的结构式___________ ;
②其他条件相同, 、NO以一定速率,通过一定量
、NO以一定速率,通过一定量 催化剂催化脱硝,当NO含量一定,
催化剂催化脱硝,当NO含量一定,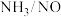 比值大于1.0后NO脱除率变化不大,其原因可能是
比值大于1.0后NO脱除率变化不大,其原因可能是___________ 。
(2)以 为催化剂的反应机理如图1所示:
为催化剂的反应机理如图1所示:

①请写出脱硝过程中总反应方程式:___________ 。
②NO脱除率随温度变化如图2所示,温度高于1000℃时NO脱除率明显下降,可能原因是:___________ 。
(3)以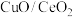 为催化剂
为催化剂
①理想 晶胞如图3所示,实际晶体中会含有部分氧空位。部分
晶胞如图3所示,实际晶体中会含有部分氧空位。部分 填充在由
填充在由 构成的
构成的___________ (填“四面体”或“八面体”)空隙中。

②Cu基催化剂对于使用CO脱去NO有着极为优异的催化性能,现探究不同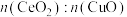 情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在
情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在 或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于
或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于___________ 上(填“ ”或“CuO”);
”或“CuO”);
③测定某催化剂中 质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用
质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用 硫酸亚铁铵[
硫酸亚铁铵[ ]溶液滴定,已知滴定时发生反应为
]溶液滴定,已知滴定时发生反应为 ,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为___________ (写出计算过程 ,计算结果保留4位有效数字)
 是脱硝问题研究的热点,催化剂的选取是技术的核心。
是脱硝问题研究的热点,催化剂的选取是技术的核心。(1)以
 为催化剂的催化原理:
为催化剂的催化原理: 与
与 形成能提供氢离子的酸性位(如图所示),
形成能提供氢离子的酸性位(如图所示), 吸附在酸性位上生成中间体继续与NO反应。
吸附在酸性位上生成中间体继续与NO反应。
①五价钒在pH为10~13的溶液中会以焦钒酸根(
 )形式存在,请写出该离子的结构式
)形式存在,请写出该离子的结构式②其他条件相同,
 、NO以一定速率,通过一定量
、NO以一定速率,通过一定量 催化剂催化脱硝,当NO含量一定,
催化剂催化脱硝,当NO含量一定,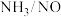 比值大于1.0后NO脱除率变化不大,其原因可能是
比值大于1.0后NO脱除率变化不大,其原因可能是(2)以
 为催化剂的反应机理如图1所示:
为催化剂的反应机理如图1所示:
①请写出脱硝过程中总反应方程式:
②NO脱除率随温度变化如图2所示,温度高于1000℃时NO脱除率明显下降,可能原因是:
(3)以
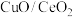 为催化剂
为催化剂①理想
 晶胞如图3所示,实际晶体中会含有部分氧空位。部分
晶胞如图3所示,实际晶体中会含有部分氧空位。部分 填充在由
填充在由 构成的
构成的
②Cu基催化剂对于使用CO脱去NO有着极为优异的催化性能,现探究不同
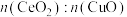 情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在
情况下脱硝、脱碳的情况。已知反应机理是CO首先吸附在 或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于
或CuO表面的活性位点上,由图像可以推断,CO反应的活性位点位于 ”或“CuO”);
”或“CuO”);③测定某催化剂中
 质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用
质量分数,取催化剂产品0.8000g,用30mL高氯酸和20mL磷酸混合液加热溶解,冷却至室温后,用 硫酸亚铁铵[
硫酸亚铁铵[ ]溶液滴定,已知滴定时发生反应为
]溶液滴定,已知滴定时发生反应为 ,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为
您最近一年使用:0次
名校
解题方法
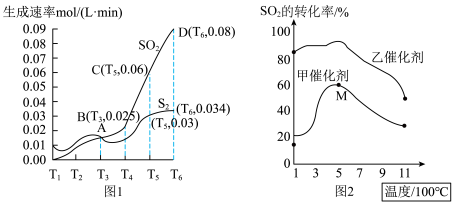
6 . 焦炭催化还原二氧化硫的化学方程式为 。一定压强下,向
。一定压强下,向 密闭容器中加入足量的焦炭和
密闭容器中加入足量的焦炭和 发生上述反应,反应相同时间时测得
发生上述反应,反应相同时间时测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1所示。其他条件相同的情况下,在甲、乙两种催化剂作用下,测得
的生成速率随温度变化的关系如图1所示。其他条件相同的情况下,在甲、乙两种催化剂作用下,测得 转化率与温度的关系如图2所示。下列说法正确的是
转化率与温度的关系如图2所示。下列说法正确的是
 。一定压强下,向
。一定压强下,向 密闭容器中加入足量的焦炭和
密闭容器中加入足量的焦炭和 发生上述反应,反应相同时间时测得
发生上述反应,反应相同时间时测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1所示。其他条件相同的情况下,在甲、乙两种催化剂作用下,测得
的生成速率随温度变化的关系如图1所示。其他条件相同的情况下,在甲、乙两种催化剂作用下,测得 转化率与温度的关系如图2所示。下列说法正确的是
转化率与温度的关系如图2所示。下列说法正确的是
A.该反应的 |
| B.图1中的A、B、C、D四个点对应的反应中处于平衡状态的是C |
C.图2在甲催化剂作用下,M点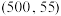 时 时 的转化率可能是该温度下 的转化率可能是该温度下 平衡转化率 平衡转化率 |
D.图2在相同的温度下,乙催化剂作用 的反应速率比甲催化剂作用 的反应速率比甲催化剂作用 反应速率小 反应速率小 |
您最近一年使用:0次
7 .  催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应1: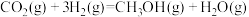

反应2:
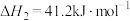
恒压下,将起始 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
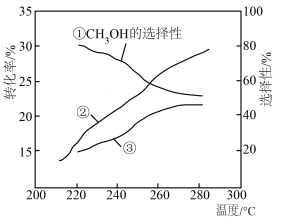
的选择性[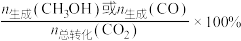 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法不 正确的是
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应1:
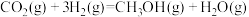

反应2:

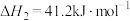
恒压下,将起始
 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
的选择性[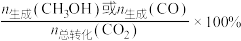 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法
A.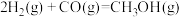 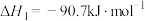 |
| B.曲线③表示CO的选择性 |
C.280℃时出口处 的物质的量分数比220℃时小 的物质的量分数比220℃时小 |
D.为提高 生产效率,需研发单位时间 生产效率,需研发单位时间 转化率高和 转化率高和 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
8 . 我国力争2060年前实现碳中和, 的资源化利用具有重要意义。
的资源化利用具有重要意义。
(1)钙循环捕集 与CaO/
与CaO/ 储热体系耦合工艺
储热体系耦合工艺
以石灰石为原料的钙循环耦合工艺流程如图所示。

①循环I中, 含量较高的是
含量较高的是___________ (填“A”或“B”)处。
②若仅进行循环II,控制不同水合温度反应相同时间,水合反应器中水合温度对CaO水合转化率的影响如题图所示,在最佳水合温度下发生反应的化学方程式为___________ 。
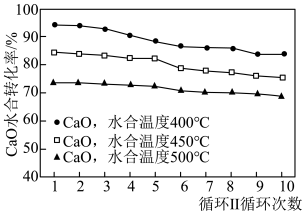
③经历多次循环I后,高温煅烧造成CaO孔隙大量减少,捕集 效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高
效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高 捕集效率的可能原因是
捕集效率的可能原因是___________ 。
④从能量转化与物质资源综合利用角度分析,该工艺的优点是___________ 。
(2)利用光催化还原 制HCOOH等液态燃料
制HCOOH等液态燃料
光催化过程包括催化剂的光激发、光生电子( )与缺电子空穴(
)与缺电子空穴( )的分离或复合、光生电子的迁移及后续的氧化与还原反应。
)的分离或复合、光生电子的迁移及后续的氧化与还原反应。
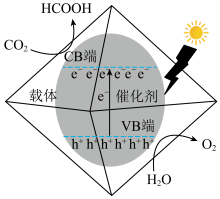
①光催化还原 制备HCOOH的原理如图所示,该过程机理可描述为
制备HCOOH的原理如图所示,该过程机理可描述为___________ 。
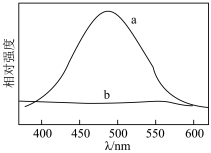
②催化剂对光的吸收强度是影响其光催化性能的重要因素之一。荧光强度越强,光生电子和空穴复合几率越大。催化剂a和b的荧光光谱如图所示,请判断哪一种催化剂催化效果更好,并说明理由___________ 。
 的资源化利用具有重要意义。
的资源化利用具有重要意义。(1)钙循环捕集
 与CaO/
与CaO/ 储热体系耦合工艺
储热体系耦合工艺以石灰石为原料的钙循环耦合工艺流程如图所示。

①循环I中,
 含量较高的是
含量较高的是②若仅进行循环II,控制不同水合温度反应相同时间,水合反应器中水合温度对CaO水合转化率的影响如题图所示,在最佳水合温度下发生反应的化学方程式为

③经历多次循环I后,高温煅烧造成CaO孔隙大量减少,捕集
 效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高
效率降低。分析经历多次循环I再经历多次循环II后的CaO能有效提高 捕集效率的可能原因是
捕集效率的可能原因是④从能量转化与物质资源综合利用角度分析,该工艺的优点是
(2)利用光催化还原
 制HCOOH等液态燃料
制HCOOH等液态燃料光催化过程包括催化剂的光激发、光生电子(
 )与缺电子空穴(
)与缺电子空穴( )的分离或复合、光生电子的迁移及后续的氧化与还原反应。
)的分离或复合、光生电子的迁移及后续的氧化与还原反应。①光催化还原
 制备HCOOH的原理如图所示,该过程机理可描述为
制备HCOOH的原理如图所示,该过程机理可描述为
②催化剂对光的吸收强度是影响其光催化性能的重要因素之一。荧光强度越强,光生电子和空穴复合几率越大。催化剂a和b的荧光光谱如图所示,请判断哪一种催化剂催化效果更好,并说明理由

您最近一年使用:0次
2023-11-10更新
|
334次组卷
|
2卷引用:江苏省无锡市2023-2024学年高三上学期期中教学质量调研测试化学试卷题
解题方法
9 . 一种催化还原 的机理如图所示,下列说法正确的是
的机理如图所示,下列说法正确的是

 的机理如图所示,下列说法正确的是
的机理如图所示,下列说法正确的是
A. 中所含 中所含 的基态电子排布式为 的基态电子排布式为 |
B.中间体X和中间体Z中 的化合价相同 的化合价相同 |
| C.转化①中既有极性共价键的形成,也有非极性共价键的形成 |
D.总转化过程中每吸收1mol 需要消耗1mol 需要消耗1mol |
您最近一年使用:0次
10 . 2023年全球电动汽车销量预计超过1400万辆,为全球经济复苏和环境保护做出较大贡献。燃油汽车尾气中除大量CO2外,还含有NO和CO气体。某研究小组用新型催化剂对CO、NO催化转化进行研究,测得一段时间内, 条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。
条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。

反应Ⅱ:

下列叙述不正确 的是
 条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。
条件下,NO的转化率、CO剩余的百分率以及无CO时NO直接分解为N2的转化率随温度的变化情况如图所示。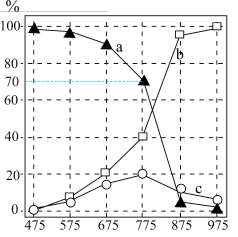


反应Ⅱ:


下列叙述
A.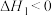 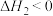 |
| B.曲线c表示:无CO时,NO直接分解为N2的转化率 |
C.775K, 时,不考虑其他反应,该时刻 时,不考虑其他反应,该时刻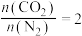 |
| D.温度在775K~875K时,催化剂活性较强 |
您最近一年使用:0次



