解题方法
1 . 利用Sb的参杂来实现对Bi的有效调制,优化了 和
和 偶联的限速步骤中间产物的对称性,以促进C―N偶联。其反应历程中能量变化如图所示。
偶联的限速步骤中间产物的对称性,以促进C―N偶联。其反应历程中能量变化如图所示。

下列有关说法错误的是
 和
和 偶联的限速步骤中间产物的对称性,以促进C―N偶联。其反应历程中能量变化如图所示。
偶联的限速步骤中间产物的对称性,以促进C―N偶联。其反应历程中能量变化如图所示。
下列有关说法错误的是
| A.尿素合成的主要决速步骤是C―N偶联 |
| B.Sb元素的参杂降低了热力学反应的焓变 |
| C.Sb元素掺杂不会减少副产物CO的产生 |
D.过程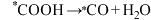 中存在O―H的形成 中存在O―H的形成 |
您最近一年使用:0次
2 . Ⅰ.对于 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

(1)定性分析:如图甲可通过观察___________ ,定性比较得出结论。有同学提出将 改为
改为 更为合理,其理由是
更为合理,其理由是___________ 。
(2)定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是___________ 。
Ⅱ.“碘钟”实验中, 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
回答下列问题:
(3)表中
___________ 。
(4)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间 的范围为___________(填字母)。
的范围为___________(填字母)。
(5)通过分析比较上表数据,得到的结论是___________ 。
 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察
 改为
改为 更为合理,其理由是
更为合理,其理由是(2)定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
Ⅱ.“碘钟”实验中,
 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
 /(mol·L /(mol·L ) ) | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
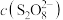 /(mol·L /(mol·L ) ) | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 |  |
(3)表中

(4)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间
 的范围为___________(填字母)。
的范围为___________(填字母)。A.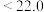 s s | B.22.0~44.0s | C.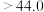 s s | D.数据不足,无法判断 |
(5)通过分析比较上表数据,得到的结论是
您最近一年使用:0次
解题方法
3 . 汽车尾气(含烃类、CO、NO、 等)是空气主要污染源之一,可以采用在汽车排气管上装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体的方法进行治理,其反应原理是
等)是空气主要污染源之一,可以采用在汽车排气管上装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体的方法进行治理,其反应原理是 。在298K、101kPa下,该反应的
。在298K、101kPa下,该反应的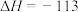 kJ·mol
kJ·mol ,
, J·mol
J·mol ·K
·K 。下列说法错误的是
。下列说法错误的是
 等)是空气主要污染源之一,可以采用在汽车排气管上装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体的方法进行治理,其反应原理是
等)是空气主要污染源之一,可以采用在汽车排气管上装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体的方法进行治理,其反应原理是 。在298K、101kPa下,该反应的
。在298K、101kPa下,该反应的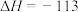 kJ·mol
kJ·mol ,
, J·mol
J·mol ·K
·K 。下列说法错误的是
。下列说法错误的是| A.该反应在常温下不能自发进行,因此需要高温和催化剂条件 |
| B.该反应中反应物的总能量高于生成物的总能量 |
| C.该反应在低温时能自发进行,高温和催化剂条件能加快反应的速率 |
| D.汽车尾气中NO、CO会与血红蛋白结合而使人中毒 |
您最近一年使用:0次
4 . 物理学将物质衰变(或消耗)一半所用时间叫“半衰期”。 时,在催化剂作用下M生成N,反应物起始浓度与催化剂、反应时间关系如图所示。下列叙述错误的是
时,在催化剂作用下M生成N,反应物起始浓度与催化剂、反应时间关系如图所示。下列叙述错误的是

 时,在催化剂作用下M生成N,反应物起始浓度与催化剂、反应时间关系如图所示。下列叙述错误的是
时,在催化剂作用下M生成N,反应物起始浓度与催化剂、反应时间关系如图所示。下列叙述错误的是
A.条件Ⅱ,M起始浓度为 时半衰期为 时半衰期为 |
B.条件Ⅲ,M的反应速率为 |
| C.其他条件相同,催化剂浓度越大,反应速率越大 |
| D.其他条件相同时,M起始浓度越大,反应速率越快 |
您最近一年使用:0次
解题方法
5 . 美国俄勒冈大学的化学家使用了新催化剂在常温下合成氨,下列有关说法正确的是
| A.新法合成氨能在常温下进行是因为不需要断裂化学键 |
| B.新法合成氨在常温下进行,可节约大量能源 |
C.新型合成氨方法的 ,传统合成氨方法的 ,传统合成氨方法的 |
| D.新催化剂提高了单位体积内活化分子数目,加快了化学反应速率,使平衡正向移动 |
您最近一年使用:0次
解题方法
6 . Operando光谱和DFT计算明确了在负载WO3的CeO2上NH3(NH3-SCR)选择性催化还原NO的还原/氧化半循环的过程如下。下列说法正确的是
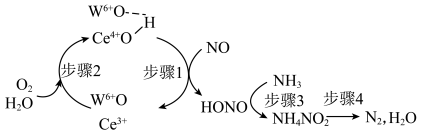

| A.步骤1中氧化剂与还原剂的物质的量之比:2∶1 |
B.氧化性强弱顺序: |
C.每生成1mol 理论上消耗0.25mol 理论上消耗0.25mol |
D.上述过程的总反应方程式: |
您最近一年使用:0次
7 . 一定条件下, 可催化
可催化 在水中发生反应,过程分为两步
在水中发生反应,过程分为两步
i.
ⅱ.
某小组设计以下实验探究上述反应速率的影响因素(如图),
已知:(1)试管①中是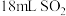 的稀溶液;②③④中是
的稀溶液;②③④中是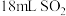 的饱和溶液
的饱和溶液
(2)四组实验中溶液出现混浊所用时间:①>②>③>④

下列说法错误的是
 可催化
可催化 在水中发生反应,过程分为两步
在水中发生反应,过程分为两步i.

ⅱ.

某小组设计以下实验探究上述反应速率的影响因素(如图),
已知:(1)试管①中是
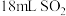 的稀溶液;②③④中是
的稀溶液;②③④中是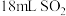 的饱和溶液
的饱和溶液(2)四组实验中溶液出现混浊所用时间:①>②>③>④

下列说法错误的是
A.通过实验①②可探究 的浓度对反应速率的影响 的浓度对反应速率的影响 |
B.实验①③可证明酸性条件下 的催化效果更好 的催化效果更好 |
C.实验④开始加入 ,发生反应ⅱ生成 ,发生反应ⅱ生成 和 和 ,加快了反应速率 ,加快了反应速率 |
D.总反应为: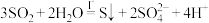 |
您最近一年使用:0次
8 . 工业合成氨的流程图如下图所示.下列说法不正确 的是
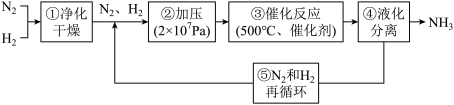

| A.步骤①中“净化”可以防止催化剂中毒 |
| B.步骤②中“加压”的目的是提高原料的转化率,同时也可以加快反应速率 |
| C.步骤③、④、⑤不是都有利于提高原料平衡的转化率 |
| D.为提高反应物的转化率和加快反应速率应及时将氨从混合气中分离出去 |
您最近一年使用:0次
解题方法
9 . 据文献报道,某含矾物质催化反应的机理如图所示.下列叙述正确的是


A.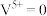 降低该反应的焓变 降低该反应的焓变 | B.该反应利用了 的还原性除去 的还原性除去 ,减少了空气污染 ,减少了空气污染 |
C.过量的 有利于 有利于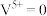 催化该反应 催化该反应 | D.该催化循环过程中V的价态变化为 |
您最近一年使用:0次
名校
10 . 填空。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 的氢气和碘蒸气放入密闭容器中进行反应:
的氢气和碘蒸气放入密闭容器中进行反应: ,反应经过5分钟测得碘化氢的浓度为
,反应经过5分钟测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为 。前5分钟平均反应速率
。前5分钟平均反应速率
__________ , 的初始浓度是
的初始浓度是__________ 。
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为 的
的 、
、 、KI、
、KI、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为
反应分两步进行:
反应A:……
反应B:
①反应A的离子方程式是___________ 。对于总反应, 的作用是
的作用是___________ 。
②探究溶液变蓝快慢的影响因素,实验I、II.(溶液浓度均为 )
)
i.溶液从混合时的无色变为蓝色的时间:实验I是30min、实验II是40min。实验II中,x、y、z所对成的数值分别是___________ 、___________ 、___________ ;
ii.对比实验I、II,可得出的实验结论是___________ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为
 的氢气和碘蒸气放入密闭容器中进行反应:
的氢气和碘蒸气放入密闭容器中进行反应: ,反应经过5分钟测得碘化氢的浓度为
,反应经过5分钟测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为 。前5分钟平均反应速率
。前5分钟平均反应速率
 的初始浓度是
的初始浓度是(2)某小组同学在室温下进行“碘钟实验”:将浓度均为
 的
的 、
、 、KI、
、KI、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为

反应分两步进行:
反应A:……
反应B:

①反应A的离子方程式是
 的作用是
的作用是②探究溶液变蓝快慢的影响因素,实验I、II.(溶液浓度均为
 )
)| 用量试剂 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 | KI溶液(含淀粉) |  |
| 实验I | 5 | 4 | 8 | 3 | 0 |
| 实验II | 5 | 2 | x | y | z |
ii.对比实验I、II,可得出的实验结论是
您最近一年使用:0次



