名校
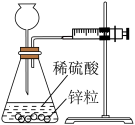
1 . 下列装置与设计不能达到实验目的的是
选项 | A | B |
装置与设计 |
|
|
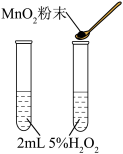
目的 | 测定锌与稀硫酸反应生成氢气的速率 | 探究催化剂对反应速率的影响 |
选项 | C | D |
装置与设计 |
|
|
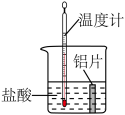
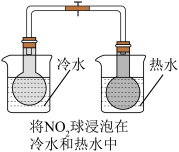
目的 | 证明铝片与盐酸的反应为放热反应 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 某反应的反应机理、能量与反应进程的关系如下图所示,下列说法正确的是
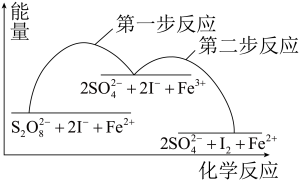

A. 是该反应的催化剂 是该反应的催化剂 | B.该反应焓变 <0可知,该反应可自发进行 <0可知,该反应可自发进行 |
C.加入催化剂后,反应的 变小 变小 | D.第一步反应的活化能比第二步反应的小 |
您最近半年使用:0次
解题方法
3 . 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如图所示。下列说法不正确的是
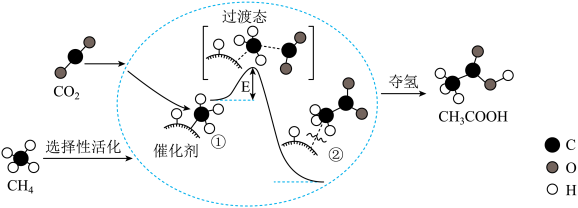
| A.生成CH3COOH总反应的原子利用率为 100% |
| B.反应过程中有极性共价键的断裂和非极性共价键的形成 |
C.① ②吸收能量并形成了C-C键 ②吸收能量并形成了C-C键 |
| D.该催化剂可有效降低活化能,提高反应速率 |
您最近半年使用:0次
名校
解题方法
4 . 工业上利用黄铁矿(FeS2)制取硫酸,其反应流程如下:

| A.反应①矿石粉碎的目的是提高反应速率 |
| B.反应②中即使通入过量的氧气,也不能将SO2全部转化成SO3 |
| C.接触室选择500℃左右的温度是因为比常温更有利于合成SO3 |
| D.过量的氨水吸收SO2的化学方程式:2NH3·H2O+SO2=(NH4)2SO3+H2O |
您最近半年使用:0次
2024-03-20更新
|
68次组卷
|
2卷引用:广东省惠州一中实验学校2023-2024学年高二上学期期中考试化学试题
解题方法
5 . 某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)补全方程式:_______ 。
5 H2C2O4+2 +_______=2Mn2++_______+8H2O
+_______=2Mn2++_______+8H2O
(2)实验过程使用了“控制变量法”,则V1=_______ ,V2=_______ ;根据上表中的实验数据,可以得到的结论是_______ 。
(3)该小组同学查阅已有的资料后,提出假设:生成物中的MnSO4为该反应的催化剂,请你帮助该小组同学完成实验方案验证假设。
①再向试管中加入的少量固体的化学式为_______ 。
②若该小组同学提出的假设成立,应观察到的现象是_______ 。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 2.0mol∙L-1 H2C2O4溶液 | H2O | 0.2mol∙L-1 KMnO4 | 3mol∙L-1稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | V1 | 4.0 |
| 2 | 2.0 | V2 | 3.0 | 2.0 | 5.2 |
| 3 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
5 H2C2O4+2
 +_______=2Mn2++_______+8H2O
+_______=2Mn2++_______+8H2O(2)实验过程使用了“控制变量法”,则V1=
(3)该小组同学查阅已有的资料后,提出假设:生成物中的MnSO4为该反应的催化剂,请你帮助该小组同学完成实验方案验证假设。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 2.0mol∙L-1 H2C2O4溶液 | H2O | 0.2mol∙L-1 KMnO4溶液 | 3mol∙L-1稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | _______ | t |
②若该小组同学提出的假设成立,应观察到的现象是
您最近半年使用:0次
解题方法
6 . 实验小组探究Cu和 溶液的反应原理。
溶液的反应原理。
(1)配制溶液
用 标准试剂配制
标准试剂配制 溶液,下列仪器中无需使用的有
溶液,下列仪器中无需使用的有_______ (填名称)。
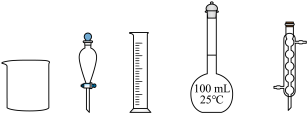
(2)测定 溶液的pH
溶液的pH
用_______ (填仪器名称)测得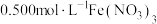 溶液的pH为1.10。
溶液的pH为1.10。
(3)提出假设
假设ⅰ:_______ ,反应的离子方程式为:
假设ⅱ: 将Cu氧化,反应的离子方程式为:
将Cu氧化,反应的离子方程式为:
(4)实验探究
实验Ⅰ:向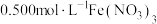 溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组取少量上层清液于另一洁净试管中,往其中滴加
溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组取少量上层清液于另一洁净试管中,往其中滴加_______ (填化学式)溶液,观察到_______ 的实验现象,证明了反应中有 生成。
生成。
实验Ⅱ:向pH=1.10的_______ (填化学式)溶液中加入过量铜粉并充分振荡,无明显现象。
探究结论:综合“实验Ⅰ”和“实验Ⅱ”可知,假设_______ (填“ⅰ”或“ⅱ”)成立。
(5)查阅资料知,铜粉与 溶液可能涉及的反应有;
溶液可能涉及的反应有;
反应①: ;
;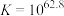 ;速率很慢。
;速率很慢。
反应②: ;
;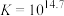 ,速率较快。
,速率较快。
反应③: ;
;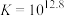 ;速率很快。
;速率很快。
反应④: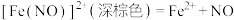
(a)对反应①来说, 起到的作用为
起到的作用为_______ ;为验证这一作用,设计的实验方案为_______ 。
(b)“实验Ⅰ”反应中无论Cu过量多少,始终都能检测到 的存在,原因是
的存在,原因是_______ 。
 溶液的反应原理。
溶液的反应原理。(1)配制溶液
用
 标准试剂配制
标准试剂配制 溶液,下列仪器中无需使用的有
溶液,下列仪器中无需使用的有
(2)测定
 溶液的pH
溶液的pH用
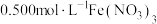 溶液的pH为1.10。
溶液的pH为1.10。(3)提出假设
假设ⅰ:

假设ⅱ:
 将Cu氧化,反应的离子方程式为:
将Cu氧化,反应的离子方程式为:
(4)实验探究
实验Ⅰ:向
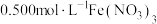 溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组取少量上层清液于另一洁净试管中,往其中滴加
溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组取少量上层清液于另一洁净试管中,往其中滴加 生成。
生成。实验Ⅱ:向pH=1.10的
探究结论:综合“实验Ⅰ”和“实验Ⅱ”可知,假设
(5)查阅资料知,铜粉与
 溶液可能涉及的反应有;
溶液可能涉及的反应有;反应①:
 ;
;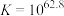 ;速率很慢。
;速率很慢。反应②:
 ;
;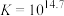 ,速率较快。
,速率较快。反应③:
 ;
;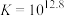 ;速率很快。
;速率很快。反应④:
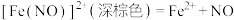
(a)对反应①来说,
 起到的作用为
起到的作用为(b)“实验Ⅰ”反应中无论Cu过量多少,始终都能检测到
 的存在,原因是
的存在,原因是
您最近半年使用:0次
7 . 2021年中国政府工作报告中提出碳中和目标:在2030年前达到最高值,2060年前达到碳中和。因此对二氧化碳的综合利用显得尤为重要。
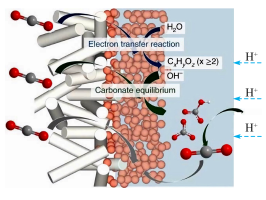

(1)通过电解的方式可实现对二氧化碳的综合利用。2022年7月香港中文大学王莹教授研发新型电解槽实现二氧化碳回收转化效率达到60%以上。转化示意图如图所示,请写出其电极反应方程式:_____ 。
(2)在席夫碱(含“—RC=N—”有机物)修饰的纳米金催化剂上,CO2直接催化加氢成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。该历程中起决速步骤的化学方程式是_____ 。
(3)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应1:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.01KJ/mol
CH3OH(g)+H2O(g) △H=-49.01KJ/mol
反应2:2CH3OH(g) CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
反应3:CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.17KJ/mol
CO(g)+H2O(g) △H=+41.17KJ/mol
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H=
CH3OCH3(g)+3H2O(g) △H=_____ KJ/mol
起始压强为4.0MPa、恒压条件下,通入氢气和二氧化碳的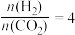 的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是_____ 。在图中,在200℃时,若经过0.2s该平衡体系即达到平衡。计算CO2分压的平均变化速率为_____ MPa/s;此时对于反应1的Kp=_____ (MPa)-2(计算的表达式)。



(1)通过电解的方式可实现对二氧化碳的综合利用。2022年7月香港中文大学王莹教授研发新型电解槽实现二氧化碳回收转化效率达到60%以上。转化示意图如图所示,请写出其电极反应方程式:
(2)在席夫碱(含“—RC=N—”有机物)修饰的纳米金催化剂上,CO2直接催化加氢成甲酸。其反应历程如图所示,其中吸附在催化剂表面上的物质用*标注。该历程中起决速步骤的化学方程式是
(3)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应1:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.01KJ/mol
CH3OH(g)+H2O(g) △H=-49.01KJ/mol反应2:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol
CH3OCH3(g)+H2O(g) △H=-24.52KJ/mol反应3:CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.17KJ/mol
CO(g)+H2O(g) △H=+41.17KJ/mol2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H=
CH3OCH3(g)+3H2O(g) △H=起始压强为4.0MPa、恒压条件下,通入氢气和二氧化碳的
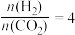 的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:
的情况下,不同温度下CO2的平衡转化率和产物的选择性(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)如图所示:当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是

您最近半年使用:0次
8 . 恒温恒容密闭容器中发生:CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
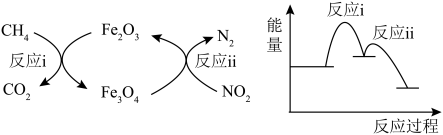
 CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
| A.使用更高效的催化剂能提高该反应平衡时的转化率 |
| B.反应一段时间后(未达平衡),Fe3O4会远远多于Fe2O3 |
| C.容器内气体的平均相对分子质量不再发生变化时,该反应达到平衡状态 |
| D.起始条件相同,其他条件不变,仅改为绝热密闭容器,CH4和NO2的转化率增大 |
您最近半年使用:0次
名校
9 . 氮及其化合物在工农业生产中有广泛的应用。请回答下列问题:
(1)氨气是一种重要的工业原料,工业上利用氮气和氢气在一定条件下合成氨气:N2(g)+3H2(g) 2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是___________ ,反应热ΔH的表达式为___________ (用E1,E2表示)

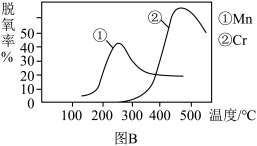
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广的烟气氮氧化物脱除技术。反应原理如图A所示:

①图B是催化剂Mn和Cr在不同温度下对应的脱氧率,由图综合考虑可知最佳的催化剂和相应的温度分别为___________ 、___________
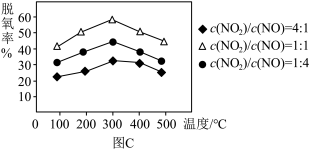
②用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氧率如图C所示,脱氧效果最佳的
对应的脱氧率如图C所示,脱氧效果最佳的
___________
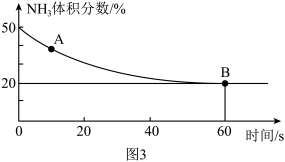
(3)工业上合成尿素的反应:2NH3(g)+CO2(g) H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)___________ B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”),CO2的平衡转化率为___________
(4)尿液也能发电。化学家正在研究尿素动力燃料电池,用这种电池直接除去城市废水中的尿素,既能产生净化的水又能发电,其工作原理为2CO(NH2)+3O2=2N2+2CO2+4H2O。电解质溶液为硫酸,则负极的电极反应式为___________ 。
(1)氨气是一种重要的工业原料,工业上利用氮气和氢气在一定条件下合成氨气:N2(g)+3H2(g)
 2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
2NH3(g) ΔH,该反应过程中的能量变化如图1所示(E1>0,E2>0),图中E1代表的意义是
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广的烟气氮氧化物脱除技术。反应原理如图A所示:

①图B是催化剂Mn和Cr在不同温度下对应的脱氧率,由图综合考虑可知最佳的催化剂和相应的温度分别为

②用Fe做催化剂时,在氨气足量的情况下,不同
 对应的脱氧率如图C所示,脱氧效果最佳的
对应的脱氧率如图C所示,脱氧效果最佳的

(3)工业上合成尿素的反应:2NH3(g)+CO2(g)
 H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
H2O(g)+CO(NH2)2(l) ΔH,在一个真空恒容密闭容器中充入CO2和NH3发生上述反应,恒定温度下混合气体中NH3的体积分数如图3所示,则A点的正反应速率v正(CO2)
(4)尿液也能发电。化学家正在研究尿素动力燃料电池,用这种电池直接除去城市废水中的尿素,既能产生净化的水又能发电,其工作原理为2CO(NH2)+3O2=2N2+2CO2+4H2O。电解质溶液为硫酸,则负极的电极反应式为
您最近半年使用:0次
名校
10 . 反应物(S)转化为产物(P或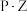 )的能量与反应进程的关系如图所示:
)的能量与反应进程的关系如图所示:
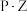 )的能量与反应进程的关系如图所示:
)的能量与反应进程的关系如图所示:
| A.进程I是吸热反应 | B.平衡时P的产率:II>I |
| C.生成P的速率:III>II | D.进程IV中,Z没有催化作用 |
您最近半年使用:0次
2024-01-17更新
|
217次组卷
|
12卷引用:广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题
广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2022-2023学年高三2 月初阶段性质量检测化学试题江苏省盐城市阜宁县2022-2023学年高一下学期4月期中考试化学试题福建省莆田第一中学2023-2024学年高二上学期期中考试化学试题辽宁省沈阳市东北育才学校高中部2023-2024学年高三上学期第三次模拟考试 化学试题陕西省西安市长安区第一中学2023-2024学年高三上学期第二次教学质量检测化学试题安徽省宣城中学2023-2024学年高二上学期12月月考化学试题陕西省西安中学2023-2024学年高三上学期实验班11月练考理科综合能力测试题福建省泉州科技中学2023-2024学年高二上学期期中考试化学试题湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题陕西省咸阳市实验中学 2022-2023学年高二上学期第三次月考化学试题天津市南开中学2023-2024学年高三下学期第四次月考化学试卷