名校
解题方法
1 . 某研究性学习小组向一定量的NaHSO3溶液(加入少量淀粉)中加入稍过量的KIO3溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:
(1)查阅资料知:NaHSO3与过量KIO3反应分为两步进行,第一步反应的离子方程式为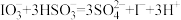 ,第二步反应的离子方程式为
,第二步反应的离子方程式为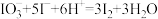 ;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是
;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是___________ (填“第一步”或“第二步”)反应。
(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
实验①②是探究___________ 对反应速率的影响,表中t1___________ (填“>”、“=”或“<”)t2;实验②③是探究温度对反应速率的影响,表中a=___________ ,b=___________ 。
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出假设,认为是生成的SO 对反应起催化作用,故设计实验验证,试完成表中的内容。
对反应起催化作用,故设计实验验证,试完成表中的内容。
(1)查阅资料知:NaHSO3与过量KIO3反应分为两步进行,第一步反应的离子方程式为
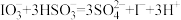 ,第二步反应的离子方程式为
,第二步反应的离子方程式为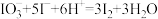 ;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是
;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
| 编号 | 0.01mol·L-1 溶液/mL 溶液/mL | 0.01mol·L-1KIO3溶液/mL | H2O/mL | 反应温度/℃ | 液变蓝所用时间t/s |
| ① | 4.0 | 14.0 | 2.0 | 15 | t1 |
| ② | 6.0 | 14.0 | 0 | 15 | t2 |
| ③ | 6.0 | a | b | 25 | t3 |
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出假设,认为是生成的SO
 对反应起催化作用,故设计实验验证,试完成表中的内容。
对反应起催化作用,故设计实验验证,试完成表中的内容。| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| Ⅰ.在烧杯甲中将一定量的NaHSO3溶液与KIO3溶液混合,用速率检测仪测定起始时的反应速率v(甲) Ⅱ.在烧杯乙中先加入少量 | 若v(甲) 若v(甲) |
您最近一年使用:0次
2023-10-24更新
|
233次组卷
|
2卷引用:广东省湛江市第二十一中学2023-2024学年高二10月月考化学试题
名校
解题方法
2 . 在Fe2O3的催化作用下,向200℃的恒温恒容密闭容器中充入1molCH4和2molNO2,发生反应CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是

 CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
| A.容器内气体的密度不再发生变化时,该反应达到平衡状态 |
| B.反应一段时间后(未达平衡),Fe3O4会远远多于Fe2O3 |
| C.起始条件相同,其他条件不变,仅改为绝热密闭容器,CH4和NO2的转化率降低 |
| D.使用更高效的催化剂能提高该反应平衡时的转化率 |
您最近一年使用:0次
名校
3 . Ⅰ.H2O2被称为绿色氧化剂,对其性质进行研究极其重要。某同学以H2O2分解为例,进行了以下实验:
(1)问题一:设计实验②和③的目的是:_______ 。
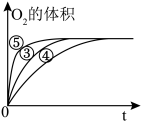
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论______ 。
Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g) N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是______ (填标号)。
(4)两个10L的密闭容器中分别都加入活性炭(足量)和1.0molNO,发生反应:C(s)+2NO(g)  N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
①T1时,0~5min内,反应速率v(CO2)=______ mol•L-1•min-1。
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是______ min~10min,此时,容器中CO2的物质的量浓度是______ mo/L。
③两容器中温度关系为T1______ T2(填“>”“<”或“=”)。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20mL2%H2O2溶液+2mLH2O | 无 | 20℃ |
| ② | 20mL5%H2O2溶液+2mLH2O | 无 | 20℃ |
| ③ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20mL5%H2O2溶液+2mL1mol/LHCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 40℃ |
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论

Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g)
 N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是| A.压缩容器体积 | B.降低温度 |
| C.使用合适催化剂 | D.恒温恒容充入稀有气体 |
 N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:| 物质的量/mol | 容器1(T1℃) | 容器2(T2℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
2023-05-23更新
|
178次组卷
|
4卷引用:广东省湛江市第二十一中学2022-2023学年高一下学期期中考试(选考)化学试题
名校
4 . 下列有关化学反应速率的说法正确的是
| A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
| B.锌片跟足量的的盐酸反应,加入适量的硫酸铜溶液,反应速率减慢 |
| C.SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢 |
| D.用过氧化氢溶液制氧气时添加少量二氧化锰粉末可以加快反应速率 |
您最近一年使用:0次
5 . 2SO2(g)+O2(g)=2SO3(g) △H=-196.6kJ•mol-1是工业制硫酸的重要反应,向某恒温恒容密闭容器甲中充入2molSO2和1molO2,适当温度下加入催化剂充分反应,下列说法正确的是
| A.SO2和SO3的VSEPR模型均为平面三角形,但SO2空间结构为V形,SO3空间结构为平面三角形 |
| B.加入催化剂能提高该反应的平衡转化率 |
| C.充分反应后,容器甲中释放196.6kJ的热量 |
| D.升高温度能加快该反应速率,工业生产中该反应温度越高越好 |
您最近一年使用:0次
6 . 一定条件下热解制取 :
: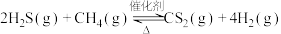 。已知其他条件不变时,温度对
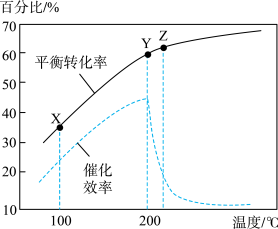
。已知其他条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
 :
: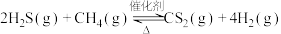 。已知其他条件不变时,温度对
。已知其他条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
A.平衡常数: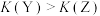 |
B.达到平衡所需时间: |
C.总能量: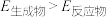 |
D.单位时间的转化率。: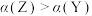 |
您最近一年使用:0次
2023-04-28更新
|
884次组卷
|
7卷引用:广东省湛江市2023届高三第二次模拟化学试题
7 . 在相同条件下研究催化剂Ⅰ、Ⅱ对反应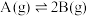 的影响,各物质浓度c随反应时间t的部分变化曲线如图所示。下列说法正确的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图所示。下列说法正确的是
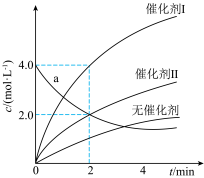
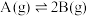 的影响,各物质浓度c随反应时间t的部分变化曲线如图所示。下列说法正确的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图所示。下列说法正确的是
| A.无催化剂时,反应不能进行 |
| B.催化剂Ⅱ比催化剂Ⅰ效率更高 |
| C.a曲线表示使用催化剂Ⅰ时A的浓度随t的变化 |
D.使用催化剂Ⅱ时,0~2min内, |
您最近一年使用:0次
2023-03-24更新
|
415次组卷
|
3卷引用:广东省湛江市普通高中2023届高三下学期4月模拟考试化学试题
名校
解题方法
8 . 2022年10月5日,诺贝尔化学奖授予了在“铜催化”领域贡献突出的卡罗琳等人。利用铜催化剂可实现甲醇( )的催化制氢,反应机理如下图所示,下列说法正确的是
)的催化制氢,反应机理如下图所示,下列说法正确的是
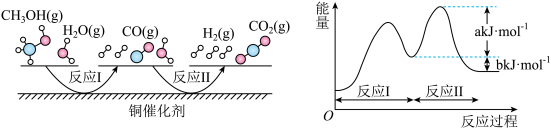
 )的催化制氢,反应机理如下图所示,下列说法正确的是
)的催化制氢,反应机理如下图所示,下列说法正确的是
A.该反应的 |
| B.CO属于反应过程中的中间产物 |
| C.反应过程中有非极性键的断裂与形成 |
D.反应Ⅱ的正反应活化能为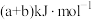 |
您最近一年使用:0次
2023-03-02更新
|
432次组卷
|
5卷引用:广东省湛江市第二十一中学2023-2024学年高二10月月考化学试题
名校
解题方法
9 . 高粱酿酒过程中部分操作如图所示。下列说法错误的是
 |  |  |  |
| “蒸粮”时加热 | “拌曲”前摊晾 | “堆酵”时升温 | “馏酒”时控温 |
| A.“蒸粮”时可适当鼓风加快燃烧速率 |
| B.““拌曲”加入的酒曲在酿酒时起到催化作用 |
| C.“堆酵”时升温是因为吸收环境中的热量 |
| D.“馏酒”的原理即实验操作中的“蒸馏” |
您最近一年使用:0次
2023-02-08更新
|
2082次组卷
|
9卷引用:广东省湛江市普通高中2023届高三下学期4月模拟考试化学试题
广东省湛江市普通高中2023届高三下学期4月模拟考试化学试题山东省济南市2023届高三下学期学情检测(一模)化学试题(已下线)山东省青岛市2023届高三下学期一模化学试题变式题(选择题1-5)江苏省盐城市响水县清源高级中学2022-2023学年高一下学期3月学情分析考试(选修)化学试题广东省惠州市惠州中学2022-2023学年高二下学期化学考试题(已下线)专题卷01 化学与STSE-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题01 化学与STSE山东省聊城市2022-2023学年高三下学期开学考试化学试题安徽省六安第一中学2023-2024学年高三上学期第三次月考化学试题
名校
10 . 利用低温技术可处理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
 5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是| A.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中NO的转化率减小 |
| C.单位时间内生成NH3和H2O的物质的量之比为2∶3时,反应达到平衡 |
| D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
您最近一年使用:0次
2022-11-06更新
|
127次组卷
|
4卷引用:广东省湛江市第二十一中学2023-2024学年高二上学期期中考试化学试题



