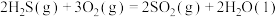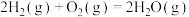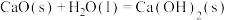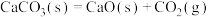广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
广西
高二
阶段练习
2023-12-05
357次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、认识化学科学、化学实验基础
广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
广西
高二
阶段练习
2023-12-05
357次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、认识化学科学、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
1. 第19届亚运会秉持“绿色、智能、节俭、文明”的办会理念。下列说法不正确的是


| A.会场“莲花碗”(如图)采取自然采光方式有利于实现“碳中和” |
| B.吉祥物“江南忆”机器人所采用芯片的主要成分为二氧化硅 |
| C.火炬“薪火”使用的1070铝合金具有硬度高、耐高温的特点 |
| D.特许商品“亚运莲花尊”的艺术载体青瓷属于无机非金属材料 |
您最近一年使用:0次
2023-10-14更新
|
80次组卷
|
2卷引用:江苏省南京市秦淮中学、溧水二高等四校2023-2024学年高二上学期第一次学情调研化学试题
单选题
|
较易(0.85)
2. 下列事实不能用勒夏特列原理解释的是
| A.用排饱和食盐水法收集氯气 |
| B.实验室制备乙酸乙酯时,将乙酸乙酯不断蒸出 |
| C.高炉炼铁时,将焦炭和铁矿石预先粉碎 |
| D.夏天打开可乐有大量泡沫溢出 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
3. 下列实验操作规范且能达到实验目的的是
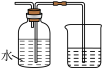 | 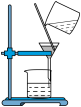 | 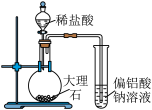 |  |
| A.用排水法收集NO | B.分离 胶体 胶体 | C.验证酸性: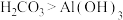 | D.加热  制取无水 制取无水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-26更新
|
2132次组卷
|
13卷引用:河南省豫北名校2024届高三毕业班上学期一轮复习联考(二)化学试题
河南省豫北名校2024届高三毕业班上学期一轮复习联考(二)化学试题山西省部分学校2023-2024学年高三上学期10月月考(一轮复习联考(二))化学试题河北省石家庄部分高中2023-2024学年高三上学期10月期中考试化学试题甘肃省部分校2024届高三上学期10月月考化学试题辽宁省部分学校2023-2024学年高三上学期一轮复习联考(二)化学试题新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期11月月考化学试题重庆市百师联盟2024届高三一轮复习联考(二)(已下线)选择题11-15广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)安徽省合肥卓越中学2023-2024学年高二上学期期中考试化学试题天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 下列问题与盐的水解有关的是
①草木灰(主要成分 )与铵态氮肥不能混合施用
)与铵态氮肥不能混合施用
② 与
与 两种溶液可作泡沫灭火剂
两种溶液可作泡沫灭火剂
③实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞
溶液的试剂瓶不能用磨口玻璃塞
④ 与
与 溶液可作焊接金属时的除锈剂
溶液可作焊接金属时的除锈剂
⑤加热蒸干 溶液并灼烧,可以得到
溶液并灼烧,可以得到 固体
固体
⑥ 溶液不能保存在玻璃试剂瓶中
溶液不能保存在玻璃试剂瓶中
①草木灰(主要成分
 )与铵态氮肥不能混合施用
)与铵态氮肥不能混合施用②
 与
与 两种溶液可作泡沫灭火剂
两种溶液可作泡沫灭火剂③实验室中盛放
 溶液的试剂瓶不能用磨口玻璃塞
溶液的试剂瓶不能用磨口玻璃塞④
 与
与 溶液可作焊接金属时的除锈剂
溶液可作焊接金属时的除锈剂⑤加热蒸干
 溶液并灼烧,可以得到
溶液并灼烧,可以得到 固体
固体⑥
 溶液不能保存在玻璃试剂瓶中
溶液不能保存在玻璃试剂瓶中| A.①②③ | B.①②③④ | C.①②③④⑤ | D.①②③④⑤⑥ |
您最近一年使用:0次
2023-12-03更新
|
314次组卷
|
3卷引用:广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
单选题
|
适中(0.65)
解题方法
5. 下列方程式书写正确的是
A. 在水中的电离方程式: 在水中的电离方程式: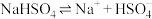 |
B. 的电离方程式 的电离方程式 |
C. 的水解方程式: 的水解方程式: |
D.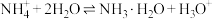 |
【知识点】 电离方程式解读 水解的离子方程式书写解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 下列各组离子在指定溶液中一定能大量共存的是
A.75%酒精溶液中: 、 、 、 、 、 、 |
B.中性溶液中: 、 、 、 、 、 、 |
C.澄清透明溶液中: 、 、 、 、 、 、 |
D.由水电离产生的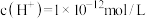 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
7.  和
和 在酸性溶液中的反应过程和机理较复杂,一般认为分以下①~④步反应(未配平),下列说法错误的是
在酸性溶液中的反应过程和机理较复杂,一般认为分以下①~④步反应(未配平),下列说法错误的是
① (反应速率慢)
(反应速率慢)
②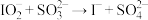 (反应速率快)
(反应速率快)
③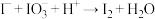 (反应速率快)
(反应速率快)
④ (反应速率快)
(反应速率快)
 和
和 在酸性溶液中的反应过程和机理较复杂,一般认为分以下①~④步反应(未配平),下列说法错误的是
在酸性溶液中的反应过程和机理较复杂,一般认为分以下①~④步反应(未配平),下列说法错误的是①
 (反应速率慢)
(反应速率慢)②
 (反应速率快)
(反应速率快)③
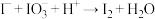 (反应速率快)
(反应速率快)④
 (反应速率快)
(反应速率快)A.反应①与反应③中 均失去电子 均失去电子 |
B.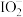 、 、 、 、 是该反应的中间产物 是该反应的中间产物 |
| C.以上4步反应中反应①的活化能最大 |
D.反应④的离子方程式为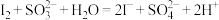 |
【知识点】 氧化还原反应的定义及实质 活化能及其对反应速率的影响解读
您最近一年使用:0次
单选题
|
适中(0.65)
8. 设NA代表阿伏加德罗常数的值。下列说法正确的是
A.101kPa、25℃,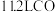 中含有的原子数为NA 中含有的原子数为NA |
B.25℃时 的氨水中 的氨水中 的数目为0.001 NA 的数目为0.001 NA |
C.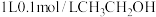 溶液中 溶液中 键数等于0.1 NA 键数等于0.1 NA |
D.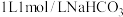 溶液中, 溶液中, 数目少于NA 数目少于NA |
【知识点】 物质结构基础与NA相关推算解读 盐类水解规律理解及应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下述描述中,正确的是
A.已知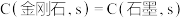  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
B.由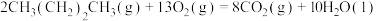 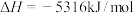 可知,正丁烷标准燃烧热为 可知,正丁烷标准燃烧热为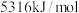 |
C.已知: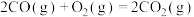 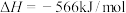 ,则说明该反应中断裂反应物化学键所吸收的能量高于形成生成物化学键所放出的能量 ,则说明该反应中断裂反应物化学键所吸收的能量高于形成生成物化学键所放出的能量 |
D.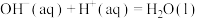  ,故 ,故 醋酸与 醋酸与 完全反应,放出的热量少于 完全反应,放出的热量少于 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 25℃时,水的电离达到平衡:
 ,下列叙述正确的是
,下列叙述正确的是

 ,下列叙述正确的是
,下列叙述正确的是A.将水加热, 增大, 增大, 减小,但仍然呈中性 减小,但仍然呈中性 |
B.向水中加入少量 固体, 固体, 增大,溶液呈酸性 增大,溶液呈酸性 |
C.向水中加入冰醋酸,水的电离平衡逆向移动, 减小 减小 |
D.向水中加入少量固体 ,水的电离平衡逆向移动, ,水的电离平衡逆向移动, 增大 增大 |
【知识点】 影响水电离的因素解读 盐类水解规律理解及应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
12. 在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力Ⅰ随加入水的体积 变化的曲线如图所示,下列说法正确的是
变化的曲线如图所示,下列说法正确的是

 变化的曲线如图所示,下列说法正确的是
变化的曲线如图所示,下列说法正确的是
A.a、b、c三点对应的溶液中, 由小到大的顺序为c<b<a 由小到大的顺序为c<b<a |
B.a、b、c三点对应的溶液中, 的电离程度最大的是c点 的电离程度最大的是c点 |
C.用润湿的 试纸测量a点溶液的 试纸测量a点溶液的 ,测量结果偏大 ,测量结果偏大 |
D.在稀释过程中,随着醋酸浓度的减小, 保持增大趋势 保持增大趋势 |
【知识点】 测定溶液pH的方法解读 弱电解质在水溶液中的电离平衡解读
您最近一年使用:0次
2023-12-03更新
|
259次组卷
|
2卷引用:广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
单选题
|
适中(0.65)
名校
解题方法
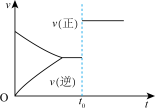
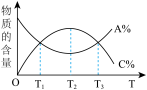
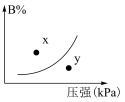
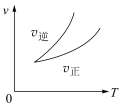
13. 以下图像对应的叙述正确的是
 |  |  |  |
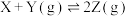 | 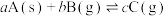 | 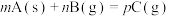 |  |
| 甲 | 乙 | 丙 | 丁 |
A.图甲:若 时刻改变的条件为增大压强,则 时刻改变的条件为增大压强,则 一定是气体 一定是气体 |
| B.图乙:升高温度,该反应平衡常数增大 |
C.图丙: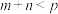 ,且 ,且 点的 点的 |
| D.图丁:该反应反应物的总能量小于生成物的总能量 |
您最近一年使用:0次
2023-12-03更新
|
344次组卷
|
4卷引用:广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省宜宾市第四中学校2023-2024学年高二上学期12月月考化学试题天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题
单选题
|
适中(0.65)
14. 相同温度下,根据三种酸的电离常数,下列判断正确的是
| 酸 |  |  | 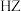 |
电离常数 | 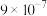 | 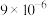 | 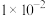 |
A.三种酸的强弱关系: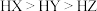 |
B.反应 能够发生 能够发生 |
C.相同温度下, 的 的 、 、 、 、 溶液, 溶液, 溶液 溶液 最大 最大 |
D.相同温度下,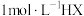 溶液的电离常数大于 溶液的电离常数大于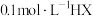 |
您最近一年使用:0次
2023-12-03更新
|
406次组卷
|
4卷引用:广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题福建省厦门市集美区2023-2024学年高二上学期12月月考化学试题(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)天津北京师范大学静海附属学校2023-2024学年高三上学期第三次月考化学试题
单选题
|
适中(0.65)
解题方法
15. 下列说法中正确的是
A.等浓度等体积的 溶液与 溶液与 溶液混合: 溶液混合: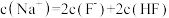 |
B.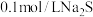 的溶液中: 的溶液中: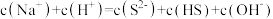 |
C.常温下 的某酸式盐 的某酸式盐 的水溶液中: 的水溶液中: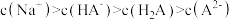 |
D.浓度均为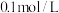 的① 的① ② ② ③ ③ ④ ④ , , 由小到大的顺序:④<③<①<② 由小到大的顺序:④<③<①<② |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
16. 室温条件下,将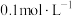 的
的 溶液逐滴滴入
溶液逐滴滴入 溶液中。所得溶液
溶液中。所得溶液 随
随 溶液体积的变化如图,下列说法正确的是
溶液体积的变化如图,下列说法正确的是
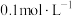 的
的 溶液逐滴滴入
溶液逐滴滴入 溶液中。所得溶液
溶液中。所得溶液 随
随 溶液体积的变化如图,下列说法正确的是
溶液体积的变化如图,下列说法正确的是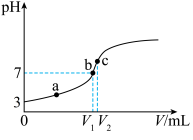
A. | B. 的电离平衡常数 的电离平衡常数 约为 约为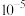 |
| C.该中和滴定可采用甲基橙作为指示剂 | D. 点溶液中: 点溶液中: |
您最近一年使用:0次
2023-12-03更新
|
228次组卷
|
2卷引用:广西玉林市博白县六校2023-2024学年高二上学期11月联考化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
17. 某研究性学习小组向一定量的NaHSO3溶液(加入少量淀粉)中加入稍过量的KIO3溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:
(1)查阅资料知:NaHSO3与过量KIO3反应分为两步进行,第一步反应的离子方程式为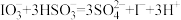 ,第二步反应的离子方程式为
,第二步反应的离子方程式为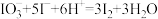 ;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是
;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是___________ (填“第一步”或“第二步”)反应。
(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
实验①②是探究___________ 对反应速率的影响,表中t1___________ (填“>”、“=”或“<”)t2;实验②③是探究温度对反应速率的影响,表中a=___________ ,b=___________ 。
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出假设,认为是生成的SO 对反应起催化作用,故设计实验验证,试完成表中的内容。
对反应起催化作用,故设计实验验证,试完成表中的内容。
(1)查阅资料知:NaHSO3与过量KIO3反应分为两步进行,第一步反应的离子方程式为
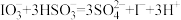 ,第二步反应的离子方程式为
,第二步反应的离子方程式为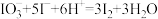 ;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是
;分两步进行的反应,其反应速率主要由慢反应决定,所以NaHSO3与过量KIO3反应中,慢反应是(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
| 编号 | 0.01mol·L-1 溶液/mL 溶液/mL | 0.01mol·L-1KIO3溶液/mL | H2O/mL | 反应温度/℃ | 液变蓝所用时间t/s |
| ① | 4.0 | 14.0 | 2.0 | 15 | t1 |
| ② | 6.0 | 14.0 | 0 | 15 | t2 |
| ③ | 6.0 | a | b | 25 | t3 |
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出假设,认为是生成的SO
 对反应起催化作用,故设计实验验证,试完成表中的内容。
对反应起催化作用,故设计实验验证,试完成表中的内容。| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| Ⅰ.在烧杯甲中将一定量的NaHSO3溶液与KIO3溶液混合,用速率检测仪测定起始时的反应速率v(甲) Ⅱ.在烧杯乙中先加入少量 | 若v(甲) 若v(甲) |
您最近一年使用:0次
2023-10-24更新
|
257次组卷
|
2卷引用:广东省湛江市第二十一中学2023-2024学年高二10月月考化学试题
三、解答题 添加题型下试题
解答题-实验探究题
|
较易(0.85)
解题方法
18. 利用草酸( )及草酸盐的性质可测定人体血液中钙离子的浓度。
)及草酸盐的性质可测定人体血液中钙离子的浓度。
实验流程:取血样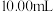 ,加适量的草酸铵[
,加适量的草酸铵[ ]溶液,析出草酸钙[
]溶液,析出草酸钙[ ]沉淀,将此沉淀洗涤后溶于强酸得草酸(
]沉淀,将此沉淀洗涤后溶于强酸得草酸( ),再用硫酸酸化的
),再用硫酸酸化的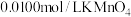 标准液平行滴定三次,平均消耗
标准液平行滴定三次,平均消耗 溶液
溶液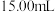 。即可计算出血液中钙离子的浓度。
。即可计算出血液中钙离子的浓度。
(1) 标准溶液应用
标准溶液应用___________ (填“酸式”或“碱式”)滴定管盛装,注入 标准溶液之前,滴定管需要检查滴定管是否漏水、洗涤和
标准溶液之前,滴定管需要检查滴定管是否漏水、洗涤和___________ 。
(2)①滴定前,装有 标准液的滴定管排气泡时,应选择下图中的
标准液的滴定管排气泡时,应选择下图中的_______ (填标号,下同)。
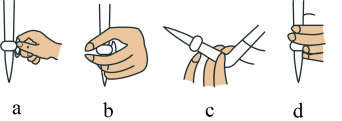
②若用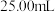 滴定管进行实验,当滴定管中的液面在刻度“8.00”处,则管内液体的体积
滴定管进行实验,当滴定管中的液面在刻度“8.00”处,则管内液体的体积_______ 。
A.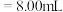 B.
B.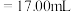 C.
C.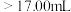 D.
D.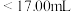
(3)请写出滴定过程中发生的离子反应方程式:___________ 。
(4)判断达到滴定终点的现象是___________ 。
(5)血液样品中 浓度为
浓度为___________  (保留2位有效数字)。
(保留2位有效数字)。
(6)判断下列操作对血液中钙离子的浓度测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①滴定前盛装酸性 标准溶液的滴定管未润洗,使测定结果
标准溶液的滴定管未润洗,使测定结果_______ 。
②滴定结束时俯视读数,使测定结果___________ 。
 )及草酸盐的性质可测定人体血液中钙离子的浓度。
)及草酸盐的性质可测定人体血液中钙离子的浓度。实验流程:取血样
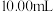 ,加适量的草酸铵[
,加适量的草酸铵[ ]溶液,析出草酸钙[
]溶液,析出草酸钙[ ]沉淀,将此沉淀洗涤后溶于强酸得草酸(
]沉淀,将此沉淀洗涤后溶于强酸得草酸( ),再用硫酸酸化的
),再用硫酸酸化的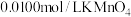 标准液平行滴定三次,平均消耗
标准液平行滴定三次,平均消耗 溶液
溶液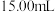 。即可计算出血液中钙离子的浓度。
。即可计算出血液中钙离子的浓度。(1)
 标准溶液应用
标准溶液应用 标准溶液之前,滴定管需要检查滴定管是否漏水、洗涤和
标准溶液之前,滴定管需要检查滴定管是否漏水、洗涤和(2)①滴定前,装有
 标准液的滴定管排气泡时,应选择下图中的
标准液的滴定管排气泡时,应选择下图中的
②若用
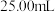 滴定管进行实验,当滴定管中的液面在刻度“8.00”处,则管内液体的体积
滴定管进行实验,当滴定管中的液面在刻度“8.00”处,则管内液体的体积A.
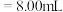 B.
B.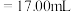 C.
C.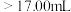 D.
D.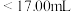
(3)请写出滴定过程中发生的离子反应方程式:
(4)判断达到滴定终点的现象是
(5)血液样品中
 浓度为
浓度为 (保留2位有效数字)。
(保留2位有效数字)。(6)判断下列操作对血液中钙离子的浓度测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①滴定前盛装酸性
 标准溶液的滴定管未润洗,使测定结果
标准溶液的滴定管未润洗,使测定结果②滴定结束时俯视读数,使测定结果
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
19. 草酸钴是一种重要的化工材料。现以某工业废渣[主要成分是 ,还含少量
,还含少量 、
、 等杂质]为原料生产草酸钴(
等杂质]为原料生产草酸钴( )的工艺流程如下:
)的工艺流程如下:

已知:氧化性: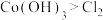
回答下列问题:
(1)加快“酸浸”速率的措施有:___________ (任写两种),“酸浸”时稀硫酸可用浓盐酸代替,但缺点是会产生污染性气体,该反应的化学方程式为___________ ,其中氧化剂与还原剂的物质的量之比为___________ 。
(2)已知酸浸液中铝元素主要以 形式存在,“除铝”时加入
形式存在,“除铝”时加入 产生沉淀的离子方程式为
产生沉淀的离子方程式为___________ 。
(3)“萃取”过程可简单表示为 ,萃取需要用到的玻璃仪器有:
,萃取需要用到的玻璃仪器有:___________ ,实际生产过程中需要进行多次萃取,其目的是___________ 。操作 为反萃取,其与萃取过程相反,反萃取使被萃取物从萃取剂中返回水溶液中,反萃取中试剂
为反萃取,其与萃取过程相反,反萃取使被萃取物从萃取剂中返回水溶液中,反萃取中试剂 最好选用
最好选用___________ (填化学式)。
 ,还含少量
,还含少量 、
、 等杂质]为原料生产草酸钴(
等杂质]为原料生产草酸钴( )的工艺流程如下:
)的工艺流程如下:
已知:氧化性:
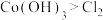
回答下列问题:
(1)加快“酸浸”速率的措施有:
(2)已知酸浸液中铝元素主要以
 形式存在,“除铝”时加入
形式存在,“除铝”时加入 产生沉淀的离子方程式为
产生沉淀的离子方程式为(3)“萃取”过程可简单表示为
 ,萃取需要用到的玻璃仪器有:
,萃取需要用到的玻璃仪器有: 为反萃取,其与萃取过程相反,反萃取使被萃取物从萃取剂中返回水溶液中,反萃取中试剂
为反萃取,其与萃取过程相反,反萃取使被萃取物从萃取剂中返回水溶液中,反萃取中试剂 最好选用
最好选用
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
20. 目前工业上可用 来生产燃料甲醇,某温度下,向体积为2L的恒容密闭容器中,充入
来生产燃料甲醇,某温度下,向体积为2L的恒容密闭容器中,充入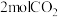 和
和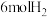 ,5min后达到化学平衡状态,此时
,5min后达到化学平衡状态,此时 的平衡转化率为75%。下图表示该反应进行过程中能量的变化。
的平衡转化率为75%。下图表示该反应进行过程中能量的变化。
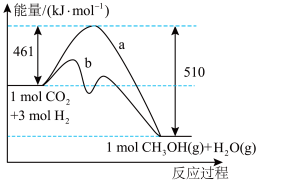
(1)由图可知该反应正逆反应活化能的大小关系为
___________  (填“>”、“<”或“=”),其中
(填“>”、“<”或“=”),其中 、
、 两种途径反应速率较快的是
两种途径反应速率较快的是___________ (填“ ”或“
”或“ ”),该反应的热化学方程式为
”),该反应的热化学方程式为___________ ,该反应的平衡常数表达式为:___________ 。
(2)从反应开始到平衡,用 的浓度变化表示平均反应速率
的浓度变化表示平均反应速率 =
=___________ 。
(3)反应过程中,下列能说明该反应达到平衡状态的是_______ (填字母)。
A.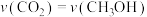 B.混合气体的密度保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.体系压强保持不变
E. F.每生成
F.每生成 的同时生成
的同时生成
(4)工业上也可用 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入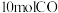 与
与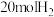 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: 。
。 的平衡转化率(
的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
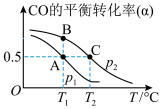
①由图可知,该反应在A、B、C三点条件下的平衡常数 、
、 和
和 由大到小的顺序为:
由大到小的顺序为:___________ 。
②若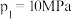 ,计算
,计算 条件下的
条件下的 =
=___________ ( 等于平衡时生成物分压幂之积除以反应物分压幂之积,某物质的分压=总压×该物质的物质的量分数)。
等于平衡时生成物分压幂之积除以反应物分压幂之积,某物质的分压=总压×该物质的物质的量分数)。
(5)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

正极的电极反应式为___________ 。
 来生产燃料甲醇,某温度下,向体积为2L的恒容密闭容器中,充入
来生产燃料甲醇,某温度下,向体积为2L的恒容密闭容器中,充入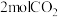 和
和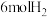 ,5min后达到化学平衡状态,此时
,5min后达到化学平衡状态,此时 的平衡转化率为75%。下图表示该反应进行过程中能量的变化。
的平衡转化率为75%。下图表示该反应进行过程中能量的变化。
(1)由图可知该反应正逆反应活化能的大小关系为

 (填“>”、“<”或“=”),其中
(填“>”、“<”或“=”),其中 、
、 两种途径反应速率较快的是
两种途径反应速率较快的是 ”或“
”或“ ”),该反应的热化学方程式为
”),该反应的热化学方程式为(2)从反应开始到平衡,用
 的浓度变化表示平均反应速率
的浓度变化表示平均反应速率 =
=(3)反应过程中,下列能说明该反应达到平衡状态的是
A.
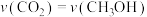 B.混合气体的密度保持不变
B.混合气体的密度保持不变C.混合气体的平均相对分子质量保持不变 D.体系压强保持不变
E.
 F.每生成
F.每生成 的同时生成
的同时生成
(4)工业上也可用
 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入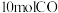 与
与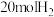 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: 。
。 的平衡转化率(
的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
①由图可知,该反应在A、B、C三点条件下的平衡常数
 、
、 和
和 由大到小的顺序为:
由大到小的顺序为:②若
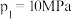 ,计算
,计算 条件下的
条件下的 =
= 等于平衡时生成物分压幂之积除以反应物分压幂之积,某物质的分压=总压×该物质的物质的量分数)。
等于平衡时生成物分压幂之积除以反应物分压幂之积,某物质的分压=总压×该物质的物质的量分数)。(5)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

正极的电极反应式为
您最近一年使用:0次
试卷分析
导出
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、化学反应原理、认识化学科学、化学实验基础
试卷题型(共 20题)
题型
数量
单选题
16
填空题
1
解答题
3
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硅的物理性质与用途 化学科学对人类文明发展的意义 金属与合金性能比较 绿色化学与可持续发展 | |
| 2 | 0.85 | 勒夏特列原理的应用 | |
| 3 | 0.85 | 胶体的性质和应用 制备与水解有关的物质 常见气体的制备与收集 物质性质实验方案的设计 | |
| 4 | 0.65 | 二氧化硅的化学性质 盐类水解规律理解及应用 盐类双水解反应 盐溶液的酸碱性判断 | |
| 5 | 0.65 | 电离方程式 水解的离子方程式书写 | |
| 6 | 0.65 | 限定条件下的离子共存 影响水电离的因素 盐类双水解反应 | |
| 7 | 0.65 | 氧化还原反应的定义及实质 活化能及其对反应速率的影响 | |
| 8 | 0.65 | 物质结构基础与NA相关推算 盐类水解规律理解及应用 | |
| 9 | 0.65 | 反应热大小比较 | |
| 10 | 0.65 | 化学能与物质稳定性之间的关系 中和热概念 燃烧热概念 根据△H=生成物的总能量之和-反应物的总能量之和进行计算 | |
| 11 | 0.65 | 影响水电离的因素 盐类水解规律理解及应用 | |
| 12 | 0.65 | 测定溶液pH的方法 弱电解质在水溶液中的电离平衡 | |
| 13 | 0.65 | 化学平衡图像分析 温度对化学平衡移动的影响 压强对化学平衡移动的影响 | |
| 14 | 0.65 | 电离平衡常数及影响因素 盐类水解规律理解及应用 弱电解质的电离平衡常数 | |
| 15 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 16 | 0.65 | 酸碱中和滴定 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 弱电解质的电离平衡常数 | |
| 二、填空题 | |||
| 17 | 0.65 | 浓度对化学反应速率的影响 温度对化学反应速率的影响 催化剂对化学反应速率的影响 化学实验探究 | |
| 三、解答题 | |||
| 18 | 0.85 | 氧化还原反应方程式的书写与配平 酸碱中和滴定原理的应用 探究物质组成或测量物质的含量 | 实验探究题 |
| 19 | 0.65 | 离子方程式的书写 盐类双水解反应 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 20 | 0.65 | 化学反应热的计算 化学平衡的有关计算 化学平衡状态的判断方法 原电池电极反应式书写 | 原理综合题 |

 的是
的是
 ;
;