名校
解题方法
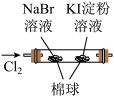
1 . 由下列实验现象一定能得出相应结论的是
| 选项 | A | B |
| 装置图 |
|
|
| 现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 |
| 结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 |
| 选项 | C | D |
| 装置图 |
|
|
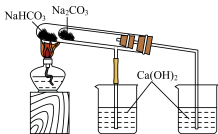
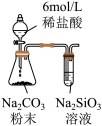
| 现象 | 左边烧杯出现白色浑浊,右边烧杯无明显现象 | 试管中液体变浑浊 |
| 结论 | 稳定性:NaHCO3<Na2CO3 | 非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验事实不能 用平衡移动原理解释的是
 |  |  |  |
将 球浸泡在冷水和热水中 球浸泡在冷水和热水中 | 将 加入 加入 溶液中 溶液中 | 不同温度下水的离子积常数 | 不同浓度 的pH 的pH |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 能使反应 的反应速率增大,且平衡向正反应方向移动的是
的反应速率增大,且平衡向正反应方向移动的是
 的反应速率增大,且平衡向正反应方向移动的是
的反应速率增大,且平衡向正反应方向移动的是A.及时分离出 气体 气体 | B.增大 的浓度 的浓度 |
| C.适当降低温度 | D.选择高效催化剂 |
您最近一年使用:0次
名校
4 . 用下列实验装置进行相应的实验,能达到实验目的的是
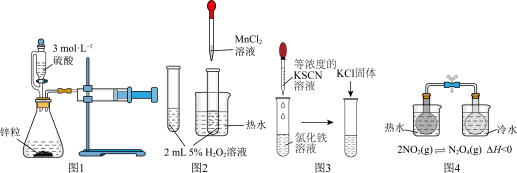

A.图1测量锌粒和稀硫酸反应中生成 的体积,计算该反应的速率 的体积,计算该反应的速率 |
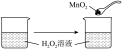
B.图2验证 对过氧化氢的分解有催化作用 对过氧化氢的分解有催化作用 |
| C.图3验证勒夏特列原理中KCl的浓度对该反应平衡的影响 |
| D.图4探究温度对化学平衡的影响 |
您最近一年使用:0次
2023-12-23更新
|
113次组卷
|
2卷引用:广东省深圳市高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
5 . NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应: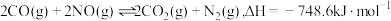 ,
, ,反应速率较小,有关该反应的说法正确的是
,反应速率较小,有关该反应的说法正确的是
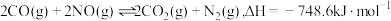 ,
, ,反应速率较小,有关该反应的说法正确的是
,反应速率较小,有关该反应的说法正确的是| A.K很大,说明NO与CO在排入大气之前就已反应完全 |
B.增大压强,反应速率增大,平衡将向右移动,K>2.5 106 106 |
| C.升高温度,既加快反应速率又可以提高有害气体的平衡转化率 |
| D.选用适宜催化剂可以使尾气排放达到标准 |
您最近一年使用:0次
2023-12-22更新
|
73次组卷
|
3卷引用:广东省深圳市罗湖高级中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
6 . 小组同学探究影响 分解反应速率的因素。
分解反应速率的因素。
(1)在 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为_______________ 。
【实验方案】
(2)对比实验①和实验②,目的是探究______ 对 分解反应速率的影响。
分解反应速率的影响。
(3)对比实验②和实验③,目的是_____ 对 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是_____ 。
(4)如果实验②中 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的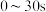 的平均反应速率为
的平均反应速率为__________  。
。
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。
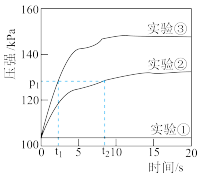
(5)上述实验中, 分解速率最快的是
分解速率最快的是_______ (填序号 );
(6)图中能证明 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是__________ 。
 分解反应速率的因素。
分解反应速率的因素。(1)在
 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为【实验方案】
| 实验编号 |  溶液 溶液 | 蒸馏水 | 催化剂 | 温度 | |
 |  |  | |||
| ① | 3 | 10 | 20 | 无催化剂 | 20 |
| ② | 3 | 10 | 20 | 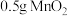 固体 固体 | 20 |
| ③ | 3 | 15 | x | 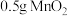 固体 固体 | 20 |
(2)对比实验①和实验②,目的是探究
 分解反应速率的影响。
分解反应速率的影响。(3)对比实验②和实验③,目的是
 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是(4)如果实验②中
 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的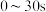 的平均反应速率为
的平均反应速率为 。
。【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。

(5)上述实验中,
 分解速率最快的是
分解速率最快的是(6)图中能证明
 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是
您最近一年使用:0次
名校
解题方法
7 . 工业上 是一种重要的绿色氧化还原试剂,某小组对
是一种重要的绿色氧化还原试剂,某小组对 的催化分解实验进行探究。回答下列问题:
的催化分解实验进行探究。回答下列问题:
(1)在同浓度 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。实验装置如图所示:
分解反应速率的影响。实验装置如图所示:

①写出 溶液在
溶液在 催化下分解的化学方程式
催化下分解的化学方程式___________ ;除了图中所示仪器之外,该实验还必需的仪器是___________ 。
②请按要求写出下面表格中的实验记录内容或数据:
I=___________ ,Ⅱ=___________ ,Ⅲ的内容为:___________ 。
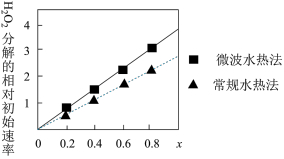
(2) 也是
也是 分解的催化剂,下图表示两种不同方法制得的
分解的催化剂,下图表示两种不同方法制得的 在相同条件下催化分解
在相同条件下催化分解 的初始速率随
的初始速率随 变化的曲线。由图可知
变化的曲线。由图可知___________ 法制取得到的催化剂活性更高,推测 两种离子中催化效果更好的是
两种离子中催化效果更好的是___________ 。
 是一种重要的绿色氧化还原试剂,某小组对
是一种重要的绿色氧化还原试剂,某小组对 的催化分解实验进行探究。回答下列问题:
的催化分解实验进行探究。回答下列问题:(1)在同浓度
 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。实验装置如图所示:
分解反应速率的影响。实验装置如图所示:
①写出
 溶液在
溶液在 催化下分解的化学方程式
催化下分解的化学方程式②请按要求写出下面表格中的实验记录内容或数据:
| 实验序号 | 0.1mol/L Fe2(SO4)3溶液的体积/mL | 30%H2O2溶液的体积/mL | 蒸馏水的体积/mL | Ⅲ | O2的体积/mL |
| 1 | a | b | c | - | - |
| 2 | I | c | Ⅱ | - | - |
(2)
 也是
也是 分解的催化剂,下图表示两种不同方法制得的
分解的催化剂,下图表示两种不同方法制得的 在相同条件下催化分解
在相同条件下催化分解 的初始速率随
的初始速率随 变化的曲线。由图可知
变化的曲线。由图可知 两种离子中催化效果更好的是
两种离子中催化效果更好的是
您最近一年使用:0次
8 . Operando光谱和DFT计算明确了在负载WO3的CeO2上NH3(NH3-SCR)选择性催化还原NO的还原/氧化半循环的过程如下。下列说法正确的是
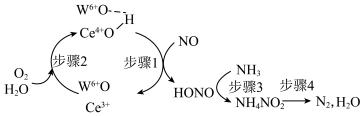

A.步骤1中氧化剂与还原剂的物质的量之比: |
B.氧化性强弱顺序: |
C.每生成 理论上消耗 理论上消耗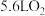 |
D.上述过程的总反应方程式: |
您最近一年使用:0次
2023-12-19更新
|
152次组卷
|
2卷引用:广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题
名校
解题方法
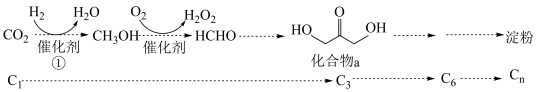
9 . 2021年我国科学家以 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
①
②
③
④
 为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
为原料人工合成淀粉,其效率约为传统农业生产淀粉的8.5倍,其部分合成路线如图所示,下列有关说法正确的是
①

②

③

④

| A.第①步反应断裂了非极性键与极性键 |
| B.催化剂降低了反应的活化能,改变了反应的焓变,降低了合成淀粉的难度 |
C. |
| D.反应④是吸热反应,活化能较大,所以是决速步 |
您最近一年使用:0次
名校
10 . 汽车尾气中的NO和CO在催化转化器中反应生成无毒无害的气体:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0,下列叙述正确的是
N2(g)+2CO2(g) ΔH<0,下列叙述正确的是
 N2(g)+2CO2(g) ΔH<0,下列叙述正确的是
N2(g)+2CO2(g) ΔH<0,下列叙述正确的是| A.尾气中的NO主要来自于汽油的不完全燃烧 |
| B.在高温下有利于该反应自发进行 |
| C.若反应速率分别用v(CO)、v(N2)表示,则2v(CO)=v(N2) |
| D.添加催化剂可使反应物中活化分子的百分数增大,因而加快反应速率 |
您最近一年使用:0次