1 . 下列事实不能用勒夏特列原理解释的是
| A.100℃时,纯水的pH≈6 |
| B.实验室常用排饱和食盐水的方法收集氯气 |
| C.实验室用过氧化氢制取氧气时,常常加入MnO2固体 |
| D.工业上采用高压条件合成氨气 |
您最近一年使用:0次
名校
解题方法
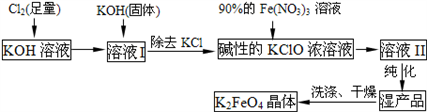
2 . 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其制取如下:
已知:①2KOH +Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO3+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)高铁酸钾(K2FeO4)应在_______ (填“温度较高”或“温度较低”)情况下进行;
(2)0.1 mol/LKClO溶液中c (ClO-) +c (HClO)_______ 0.1 mol/L (填>、<、=)
(3)K2FeO4具有强氧化性的原因____________________________ ;
(4)配制KOH溶液时,是在每100mL水中溶解56 gKOH固体(该溶液的密度为1.56g/mL),它的物质的量浓度为_________________ ;
(5)在“反应液Ⅰ”中加KOH固体的目的是_______________ ;
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液Ⅱ”中分离出K2FeO4后,会有副产品__________ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途_____________________ 。
已知:①2KOH +Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO3+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)高铁酸钾(K2FeO4)应在
(2)0.1 mol/LKClO溶液中c (ClO-) +c (HClO)
(3)K2FeO4具有强氧化性的原因
(4)配制KOH溶液时,是在每100mL水中溶解56 gKOH固体(该溶液的密度为1.56g/mL),它的物质的量浓度为
(5)在“反应液Ⅰ”中加KOH固体的目的是
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液Ⅱ”中分离出K2FeO4后,会有副产品
您最近一年使用:0次



