名校
1 . 下列说法正确的是
A. , , 的反应在温度低时不能自发进行 的反应在温度低时不能自发进行 |
| B.室温下冰自动融化成水,这是熵增的过程 |
| C.海水提溴:一般需要经过浓缩、氧化、用热空气吹出及冷凝、精制等步骤 |
D.硫酸工业:采用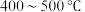 的高温,有利于增大反应正向进行的程度 的高温,有利于增大反应正向进行的程度 |
您最近一年使用:0次
23-24高三上·陕西汉中·阶段练习
解题方法
2 .  (简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、
(简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、 、LiCl和
、LiCl和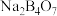 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。
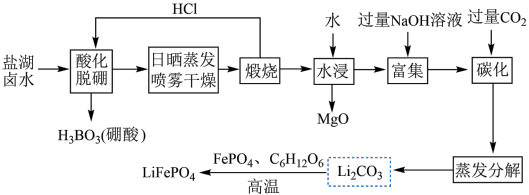
注:日晒蒸发、喷雾干燥后固体含NaCl、LiCl、 等。
等。
(1) 中Li在元素周期表中的位置为第
中Li在元素周期表中的位置为第___________ 周期___________ 族。
(2)硼酸在水中的溶解度随温度的变化关系如图所示。
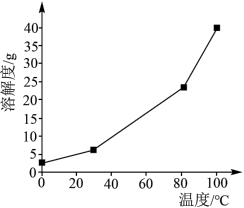
已知: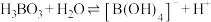
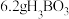 最多与
最多与___________  溶液完全反应。“酸化脱硼”中采用
溶液完全反应。“酸化脱硼”中采用___________ (填“加热”或“冷却”),采用该操作的目的是___________ 。
(3)“煅烧”过程中,常需要搅拌,搅拌的目的是___________ 。
(4)“蒸发分解”的化学方程式为___________ 。
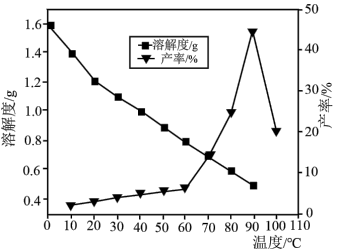
(5)已知不同温度下蒸发分解得到 的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是
的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是___________ ,制得 后需要洗涤,具体操作为
后需要洗涤,具体操作为___________ 。
(6)用 、
、 、
、 制备
制备 时,有
时,有 产生,则参与反应的
产生,则参与反应的 和
和 的物质的量之比为
的物质的量之比为___________ 。
 (简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、
(简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、 、LiCl和
、LiCl和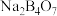 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。
注:日晒蒸发、喷雾干燥后固体含NaCl、LiCl、
 等。
等。(1)
 中Li在元素周期表中的位置为第
中Li在元素周期表中的位置为第(2)硼酸在水中的溶解度随温度的变化关系如图所示。

已知:
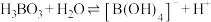
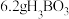 最多与
最多与 溶液完全反应。“酸化脱硼”中采用
溶液完全反应。“酸化脱硼”中采用(3)“煅烧”过程中,常需要搅拌,搅拌的目的是
(4)“蒸发分解”的化学方程式为
(5)已知不同温度下蒸发分解得到
 的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是
的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是 后需要洗涤,具体操作为
后需要洗涤,具体操作为
(6)用
 、
、 、
、 制备
制备 时,有
时,有 产生,则参与反应的
产生,则参与反应的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 .  可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备
可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备 以及含量测定的实验。已知:常温下
以及含量测定的实验。已知:常温下 不溶于水,较稳定,与酸反应生成
不溶于水,较稳定,与酸反应生成 ;加热时会分解生成
;加热时会分解生成 和
和 。
。
请回答下列问题:
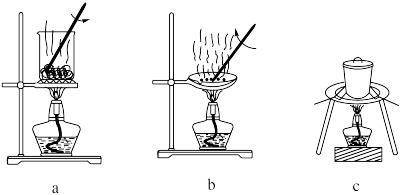
(1)灼烧。灼烧 制
制 时,可使用的实验装置有
时,可使用的实验装置有___________ (填字母)。
(2)转化。向 中先加入稳定剂和
中先加入稳定剂和 溶液,充分反应后,过滤、洗涤、干燥,可得粗品
溶液,充分反应后,过滤、洗涤、干燥,可得粗品 。
。
①写出制备 时发生反应的化学方程式:
时发生反应的化学方程式:___________ 。
②“转化”阶段有大量热量放出,为了提高 的产率,添加
的产率,添加 溶液时,比较理想的操作方法为
溶液时,比较理想的操作方法为___________ 。
(3)测定。某研究小组拟用下图装置测定样品(含 杂质)中
杂质)中 的含量。
的含量。

①实验时在稀盐酸中加入 溶液的作用是
溶液的作用是___________ (用化学方程式表示)。
②为了减小实验误差,在每次读数前需要进行的操作是___________ 、___________ 。
③该小组记录的实验数据如下:样品的质量为 ;反应开始前量气管的读数为
;反应开始前量气管的读数为 ;反应结束冷却到室温后量气管的读数为
;反应结束冷却到室温后量气管的读数为 ,已知:室温条件下气体摩尔体积为
,已知:室温条件下气体摩尔体积为 ,则样品中过氧化镁的质量分数为
,则样品中过氧化镁的质量分数为___________  (用含
(用含 的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得
的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得 的质量分数
的质量分数___________ (填“偏大”“偏小”或“无影响”)。
 可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备
可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备 以及含量测定的实验。已知:常温下
以及含量测定的实验。已知:常温下 不溶于水,较稳定,与酸反应生成
不溶于水,较稳定,与酸反应生成 ;加热时会分解生成
;加热时会分解生成 和
和 。
。请回答下列问题:
(1)灼烧。灼烧
 制
制 时,可使用的实验装置有
时,可使用的实验装置有
(2)转化。向
 中先加入稳定剂和
中先加入稳定剂和 溶液,充分反应后,过滤、洗涤、干燥,可得粗品
溶液,充分反应后,过滤、洗涤、干燥,可得粗品 。
。①写出制备
 时发生反应的化学方程式:
时发生反应的化学方程式:②“转化”阶段有大量热量放出,为了提高
 的产率,添加
的产率,添加 溶液时,比较理想的操作方法为
溶液时,比较理想的操作方法为(3)测定。某研究小组拟用下图装置测定样品(含
 杂质)中
杂质)中 的含量。
的含量。
①实验时在稀盐酸中加入
 溶液的作用是
溶液的作用是②为了减小实验误差,在每次读数前需要进行的操作是
③该小组记录的实验数据如下:样品的质量为
 ;反应开始前量气管的读数为
;反应开始前量气管的读数为 ;反应结束冷却到室温后量气管的读数为
;反应结束冷却到室温后量气管的读数为 ,已知:室温条件下气体摩尔体积为
,已知:室温条件下气体摩尔体积为 ,则样品中过氧化镁的质量分数为
,则样品中过氧化镁的质量分数为 (用含
(用含 的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得
的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得 的质量分数
的质量分数
您最近一年使用:0次
2023-10-06更新
|
799次组卷
|
5卷引用:安徽省巢湖市第一中学2024届高三10月月考化学试题
解题方法
4 . 下列说法错误的是
| A.合成氨反应采取循环操作主要是为了提高化学反应速率 |
B.  、 、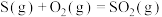  ,则 ,则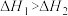 |
C.反应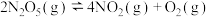  ,能自发进行的原因是 ,能自发进行的原因是 |
D.一定温度下,对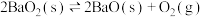 平衡体系缩小体积,再次达到平衡时 平衡体系缩小体积,再次达到平衡时 不变 不变 |
您最近一年使用:0次
2023-02-21更新
|
189次组卷
|
6卷引用:安徽省明光市第二中学2023-2024学年高二上学期期中考试化学试卷
安徽省明光市第二中学2023-2024学年高二上学期期中考试化学试卷 河南省商开大联考2022~2023学年高二上学期期末考试化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)河北省沧州市2023-2024学年高二上学期12月月考化学试题江西省部分学校2023-2024学年高二下学期开学考试化学试题陕西省榆林市府谷县府谷中学2023-2024学年高二下学期开学化学试题
名校
5 . 哈伯工业合成氨的流程如图,为提高原料平衡转化率采取的措施是
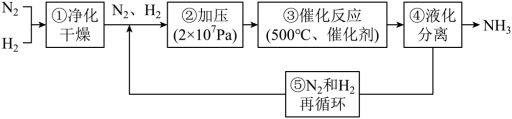

| A.①②③④⑤ | B.②③④⑤ | C.②④⑤ | D.②③④ |
您最近一年使用:0次
2022-10-21更新
|
177次组卷
|
18卷引用:安徽省宣城市2018-2019学年高二下学期期末考试化学试题
安徽省宣城市2018-2019学年高二下学期期末考试化学试题山西省长治市第二中学2019-2020学年高二上学期12月月考化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮山东省淄博市沂源县第二中学2020-2021学年高二下学期期中考试化学试题江西省九江市第一中学2021-2022学年高二上学期第一次月考化学试题山西省长治市第二中学校2021-2022学年高二上学期第一次月考化学试题(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省齐齐哈尔市第八中学2022-2023学年高二上学期10月月考化学试题重庆市南川中学2022-2023学年高二上学期第一学月考试化学试题宁夏回族自治区银川一中2022-2023学年高二上学期期末考试化学试题山西省太原市2019-2020学年高二上学期期中测评化学试题天津市部分区2022-2023 学年高三上学期1月期末考试化学试题广东省湛江市第二十一中学2022-2023学年高二上学期期中考试化学试题第二章 化学反应速率与化学平衡 第四节 化学反应的调控河南省濮阳市第一高级中学2023-2024学年高二上学期9月月考化学试题四川省内江市威远中学校2023-2024学年高二上学期期中考试化学试题四川省内江市威远中学校2023-2024学年高二上学期第二次月考(期中)化学试卷湖北省武汉市重点中学5G联合体2023-2024学年高二上学期期中考试化学试题
6 . 某镍矿石的主要成分为NiO,另含CoO、FeO、Fe2O3、Al2O3、MgO、CaO和SiO2等杂质,按以下流程可制备NiSO4•6H2O晶体和金属钴。

回答下列问题:
(1)“预处理”时需将Fe2+全部氧化为Fe3+,试剂X最好选用_______ (填序号),写出发生反应的化学方程式_______ 。
a.稀硝酸 b.双氧水 c.高锰酸钾溶液 d.新制氯水
(2)常温下,一些金属难溶氢氧化物的溶解度(用阳离子的浓度表示)与pH的关系图如图:

加入NiO调pH=5可除去_______ (填金属离子符号)。
(3)滤渣Z的成分为MgF2和CaF2。若原溶液中c(Ca2+)=1.0×10-3mol/L,沉淀后溶液中c(Mg2+)=1.5×10-6mol/L,则除钙率为_______ (忽略沉淀前后溶液体积变化)。(已知:Ksp(CaF2)=1.5×10-10、Ksp(MgF2)=7.5×10-11)
(4)影响P507萃取率的因素有很多,在其他条件相同时,根据如图分析分离镍、钴的最佳条件:相比(油相O:水相A)=_______ ;P507萃取金属离子的原理为nHR(Org)+Mn+(aq) MRn(Org)+nH+(aq),在一定范围内,随着pH升高,萃取率升高的原因是
MRn(Org)+nH+(aq),在一定范围内,随着pH升高,萃取率升高的原因是_______ 。

(5)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
从NiSO4溶液获得稳定的NiSO4•6H2O晶体的操作a依次是_______ 。

回答下列问题:
(1)“预处理”时需将Fe2+全部氧化为Fe3+,试剂X最好选用
a.稀硝酸 b.双氧水 c.高锰酸钾溶液 d.新制氯水
(2)常温下,一些金属难溶氢氧化物的溶解度(用阳离子的浓度表示)与pH的关系图如图:

加入NiO调pH=5可除去
(3)滤渣Z的成分为MgF2和CaF2。若原溶液中c(Ca2+)=1.0×10-3mol/L,沉淀后溶液中c(Mg2+)=1.5×10-6mol/L,则除钙率为
(4)影响P507萃取率的因素有很多,在其他条件相同时,根据如图分析分离镍、钴的最佳条件:相比(油相O:水相A)=
 MRn(Org)+nH+(aq),在一定范围内,随着pH升高,萃取率升高的原因是
MRn(Org)+nH+(aq),在一定范围内,随着pH升高,萃取率升高的原因是
(5)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8℃—53.8℃ | 53.8℃—280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
您最近一年使用:0次
7 . 化学和生活密切相关,下列生产生活中实例不能用勒夏特列原理解释的是
| A.摇晃后的可乐开启后有大量气泡 |
| B.合成氨工业中温度选择400-500℃ |
| C.酸遇紫色石蕊试剂变红 |
| D.生产硫酸的过程中用过量的空气和二氧化硫反应 |
您最近一年使用:0次
2022-04-16更新
|
209次组卷
|
3卷引用:安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题
安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
解题方法
8 . 我国提出2060年前实现碳中和,降低大气中CO2含量是当今世界重要科研课题之一,以CO2为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。问答下列问题:
(1)CO2在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-1
副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1
①已知2H2(g)+O2(g)=2H2O(g) ΔH3=-395.6kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=___________
②加氢合成甲烷时,通常控制温度为500℃左右,其原因为该温度下有较高的化学反应速率和___________
③500℃时,向1L恒容密闭容器中充入4molCO2和12molH2,初始压强为p,20min时主、副反应都达到平衡状态,测得c(H2O)=5mol·L-1,体系压强为 ,则0~20min内v(CH4)=
,则0~20min内v(CH4)=___________ mol·L-lmin-1,平衡时CH4选择性=___________ (CH4选择性=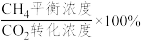 )。
)。
(2)我国科研人员将CO2和H2在Na-Fe3O4/HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。
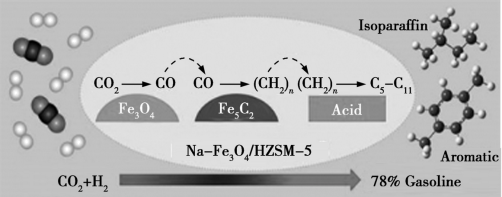
①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为___________
②催化剂中的Fe3O4可用电解法制备。电解时以Fe做电极,电解质溶液为稀硫酸,其阳极反应式为___________
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH⇌C3H6(g)+H2O(g);
反应2:2CH3OH(g)⇌C2H4(g)+2H2O(g)
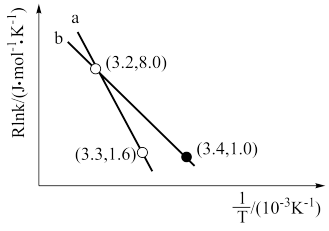
反应I的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式Rlnk= (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能(10K)Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能(10K)Ea=___________ kJ·mol-1。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是___________
(1)CO2在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH1=-156.9kJ·mol-1
副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41.1kJ·mol-1
①已知2H2(g)+O2(g)=2H2O(g) ΔH3=-395.6kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=
②加氢合成甲烷时,通常控制温度为500℃左右,其原因为该温度下有较高的化学反应速率和
③500℃时,向1L恒容密闭容器中充入4molCO2和12molH2,初始压强为p,20min时主、副反应都达到平衡状态,测得c(H2O)=5mol·L-1,体系压强为
 ,则0~20min内v(CH4)=
,则0~20min内v(CH4)=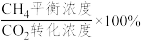 )。
)。(2)我国科研人员将CO2和H2在Na-Fe3O4/HZSM-5催化下转变为汽油(C5~C11的烃),反应过程如下图所示。

①若CO2在该条件下转化为戊烷(C5H12),则该反应的化学方程式为
②催化剂中的Fe3O4可用电解法制备。电解时以Fe做电极,电解质溶液为稀硫酸,其阳极反应式为
(3)甲醇催化制取乙烯的过程中发生如下反应:
反应1:3CH3OH⇌C3H6(g)+H2O(g);
反应2:2CH3OH(g)⇌C2H4(g)+2H2O(g)
反应I的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式Rlnk=
 (Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能(10K)Ea=
(Ea为活化能,k为速率常数,R和C为常数)。则该反应的活化能(10K)Ea=
您最近一年使用:0次
2022-02-02更新
|
893次组卷
|
4卷引用:安徽省马鞍山市 2021-2022学年高三第一次教学质量监测理综化学试题
安徽省马鞍山市 2021-2022学年高三第一次教学质量监测理综化学试题(已下线)押江苏卷第18题 化学反应原理综合题 -备战2022年高考化学临考题号押题(江苏卷)四川省成都附属实验中学2021-2022学年高三下学期第一次模拟考试理科综合化学试题(已下线)题型26 多反应体系中的化学平衡
名校
解题方法
9 . 使用SNCR脱硝技术的原理是6NO(g)+4NH3(g) 5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是

 5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
| A.从图1判断,该反应的正反应方向是放热反应 |
| B.从图2判断,减少氨气的浓度有助于提高NO的转化率 |
| C.从图1判断,脱硝的最佳温度约为900℃ |
| D.从图2判断,综合考虑脱硝效率和运行成本最佳氨氮摩尔比应为1.5-2.0 |
您最近一年使用:0次
2021-12-13更新
|
167次组卷
|
2卷引用:安徽省亳州市第二中学2021-2022学年高二上学期期中考试化学试题
10 . 我国提出争取在2030年前实现碳达峰,2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。因此,研发 利用技术,降低空气中
利用技术,降低空气中 的含量成为研究热点。当前,科学家成功利用
的含量成为研究热点。当前,科学家成功利用 和
和 合成了
合成了 ,这对节能减排、降低碳排放具有重大意义。回答下列问题:
,这对节能减排、降低碳排放具有重大意义。回答下列问题:
(1)在一定压强下,测得某一密闭容器中由 和
和 制备
制备 的实验数据中,起始投料比、温度与
的实验数据中,起始投料比、温度与 转化率的关系如图所示。
转化率的关系如图所示。

已知: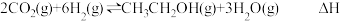 。
。
①每生成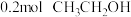 产生的热量为
产生的热量为 ,则
,则
_______  (用含a的代数式表示)。
(用含a的代数式表示)。
②在上述条件下,发生该反应,适宜的温度为_______ (填“500”、“600”、“700”或“800”)K,判断的理由为_______ 。
③在某温度下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,
, 末,反应达到平衡,此时测得反应前后的总压强之比为
末,反应达到平衡,此时测得反应前后的总压强之比为 ,则
,则 的转化率为
的转化率为_______  ,
, 内,
内,
_______  ,平衡常数
,平衡常数
_______ (列出计算式即可)。
(2)对于 和
和 合成
合成 的反应,下列说法正确的是
的反应,下列说法正确的是_______ (填标号)。
a.混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
b.加入合适的催化剂,正、逆反应速率均增大,同时 的产率也提高
的产率也提高
c. 的物质的量分数不再发生改变时,该反应达到平衡
的物质的量分数不再发生改变时,该反应达到平衡
d.增大压强.可提高 的转化率,同时平衡常数也增大
的转化率,同时平衡常数也增大
 利用技术,降低空气中
利用技术,降低空气中 的含量成为研究热点。当前,科学家成功利用
的含量成为研究热点。当前,科学家成功利用 和
和 合成了
合成了 ,这对节能减排、降低碳排放具有重大意义。回答下列问题:
,这对节能减排、降低碳排放具有重大意义。回答下列问题:(1)在一定压强下,测得某一密闭容器中由
 和
和 制备
制备 的实验数据中,起始投料比、温度与
的实验数据中,起始投料比、温度与 转化率的关系如图所示。
转化率的关系如图所示。
已知:
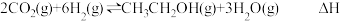 。
。①每生成
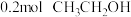 产生的热量为
产生的热量为 ,则
,则
 (用含a的代数式表示)。
(用含a的代数式表示)。②在上述条件下,发生该反应,适宜的温度为
③在某温度下,向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,
, 末,反应达到平衡,此时测得反应前后的总压强之比为
末,反应达到平衡,此时测得反应前后的总压强之比为 ,则
,则 的转化率为
的转化率为 ,
, 内,
内,
 ,平衡常数
,平衡常数
(2)对于
 和
和 合成
合成 的反应,下列说法正确的是
的反应,下列说法正确的是a.混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
b.加入合适的催化剂,正、逆反应速率均增大,同时
 的产率也提高
的产率也提高c.
 的物质的量分数不再发生改变时,该反应达到平衡
的物质的量分数不再发生改变时,该反应达到平衡d.增大压强.可提高
 的转化率,同时平衡常数也增大
的转化率,同时平衡常数也增大
您最近一年使用:0次
2021-11-13更新
|
123次组卷
|
2卷引用:安徽省芜湖市示范中学2021-2022学年高二上学期期中考试化学试题



