名校
解题方法
1 . 科学家设计了一种新型 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。 分子构型与乙烯类似。
分子构型与乙烯类似。
① ;
;
② 。
。
下列关于二者净化气体的说法中,正确的一项是
 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。
 分子构型与乙烯类似。
分子构型与乙烯类似。①
 ;
;②
 。
。下列关于二者净化气体的说法中,正确的一项是
A. 捕获的气体所有原子共平面, 捕获的气体所有原子共平面, 捕获的气体空间构型为正四面体 捕获的气体空间构型为正四面体 |
B. 置入废气后,废气颜色变深, 置入废气后,废气颜色变深, 置入废气后,废气颜色变浅 置入废气后,废气颜色变浅 |
C. 适宜在较低温度下净化气体, 适宜在较低温度下净化气体, 适宜在较高温度下净化气体 适宜在较高温度下净化气体 |
D. 适宜在较高压强下净化气体, 适宜在较高压强下净化气体, 适宜在较低压强下净化气体 适宜在较低压强下净化气体 |
您最近半年使用:0次
7日内更新
|
81次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
2 . 某兴趣小组以重铬酸钾( )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。
已知:在水溶液中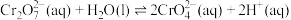
查阅资料:①含铬元素的离子在溶液中的颜色: (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);
② 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
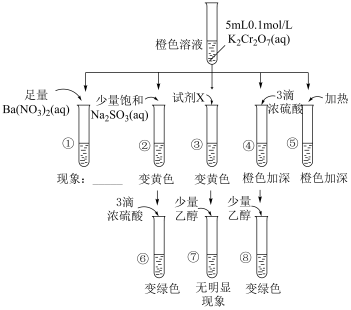
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为___________ ,试剂X是___________ (填化学式)。
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是___________ ,实验⑥中发生反应的离子方程式为___________ 。
(3)结合③、④、⑦、⑧可得出结论为___________ 。
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?___________ (填“能”或“否”)。
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:
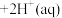 正反应的焓变
正反应的焓变
_______ 0(填“>”、“<”或“=”)。
 )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。已知:在水溶液中
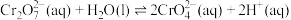
查阅资料:①含铬元素的离子在溶液中的颜色:
 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);②
 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是
(3)结合③、④、⑦、⑧可得出结论为
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:

 正反应的焓变
正反应的焓变
您最近半年使用:0次
2024-01-09更新
|
45次组卷
|
2卷引用:安徽省安庆市田家炳中学(安庆市第十中学)2023-2024学年高二上学期期中考试化学试题
名校
3 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计和现象 | 结论 |
| A | 证明 是弱电解质 是弱电解质 | 用pH计分别测量醋酸溶液和盐酸的pH,醋酸溶液的pH大 |  是弱电解质 是弱电解质 |
| B | 探究压强对化学平衡的影响 | 先将注射器充满 气体,然后将活塞往里推,注射器内气体颜色加深 气体,然后将活塞往里推,注射器内气体颜色加深 | 加压,平衡向生成 气体的方向移动 气体的方向移动 |
| C | 探究浓度对化学平衡的影响 | 向 (黄色)溶液中缓慢滴加硫酸,溶液由黄色变为橙色 (黄色)溶液中缓慢滴加硫酸,溶液由黄色变为橙色 | 增大 浓度,平衡向生成 浓度,平衡向生成 (橙色)方向移动 (橙色)方向移动 |
| D | 比较 、 、 催化分解 催化分解 的效率 的效率 | 向两份等浓度、等体积且等温的过氧化氢溶液中分别加入2滴等浓度的 溶液和 溶液和 溶液,前者产生气泡较快 溶液,前者产生气泡较快 | 催化效率: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 恒温恒容条件下,反应 分两步进行,①
分两步进行,① 、②
、② 的能量-反应过程图如下所示。
的能量-反应过程图如下所示。
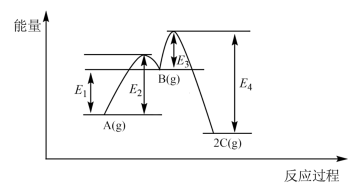
下列有关该反应的叙述正确的是
 分两步进行,①
分两步进行,① 、②
、② 的能量-反应过程图如下所示。
的能量-反应过程图如下所示。
下列有关该反应的叙述正确的是
A.加入催化剂, 减小 减小 |
B.总反应的能量变化为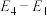 |
C.起始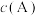 越大,A的转化率越高 越大,A的转化率越高 |
| D.反应②在升高温度时,平衡向逆反应方向移动 |
您最近半年使用:0次
名校
解题方法
5 . 反应
 ,达到平衡后,下列说法
,达到平衡后,下列说法不正确 的是

 ,达到平衡后,下列说法
,达到平衡后,下列说法| A.对氯水进行光照产生氧气时发生了氧化还原反应 |
| B.氯水中加入少量醋酸钠固体,上述平衡正向移动 |
C.取氯水进行加水稀释,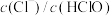 增大 增大 |
D.取两份氯水分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝,说明上述反应存在限度 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝,说明上述反应存在限度 |
您最近半年使用:0次
名校
解题方法
6 . 在一密闭容器中,反应 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增大了 | D. |
您最近半年使用:0次
2023-11-14更新
|
357次组卷
|
25卷引用:安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题
安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题(已下线)【浙江新东方】双师118天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题黑龙江省大庆市东风中学2021-2022学年高二下学期开学考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题天津市第二南开学校2022-2023学年高二上学期9月阶段性线上练习化学试题 天津市宁河区芦台第一中学2022-2023学年高二上学期第一次学习诊断化学试题浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)新疆石河子第一中学2023-2024学年高二上学期11月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题河北省石家庄市第十五中学2023-2024学年高二上学期12月阶段考试化学试题广东省汕头市潮阳区河溪中学2023-2024学年高二上学期月考化学试题
名校
解题方法
7 . 某同学研究浓度对化学平衡的影响,下列说法正确的是
已知: ΔH=+13.8kJ/mol ΔH=+13.8kJ/mol | |
步骤: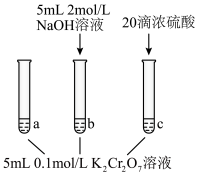 | 现象:待试管b中颜色不变后与试管a比较,溶液颜色变浅。 滴加浓硫酸、试管c温度略有升高,溶液颜色与试管a相比,变深。 |
| A.该实验不能证明减小生成物浓度,平衡正向移动 |
B.待试管b中溶液颜色不变的目的是使 完全反应 完全反应 |
| C.该反应是一个氧化还原反应 |
D.试管c中的现象说明影响平衡的主要因素是 浓度 浓度 |
您最近半年使用:0次
名校
8 . 根据下列实验操作和现象所得到的结论正确的是
 | 将 NO2 球浸泡在冷水和热水中2NO2(g)  N2O4(g) △H<0 N2O4(g) △H<0 | A.气体在热水中比在冷水中颜色浅 |
 | H2(g)+I2(g)  2HI(g) 2HI(g) | B.平衡体系加压后颜色先变深后变浅 |
 | 推动注射器活塞 | C.加压后气体颜色变深后不再变化 |
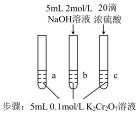 |  (aq)(橙色) + H2O(l) (aq)(橙色) + H2O(l)  2 2 (aq)(黄色)+ 2H+(aq) △H=+13.8 kJ/mol (aq)(黄色)+ 2H+(aq) △H=+13.8 kJ/mol | D.与a 颜色相比,b 溶液颜色变浅不能证明减小生成物浓度使平衡正向移动;c 溶液颜色变深能证明增加生成物浓度平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-10-27更新
|
27次组卷
|
2卷引用:安徽省淮北市第一中学2023-2024学年高二上学期第三次月考化学试题
名校
9 . 在硫酸工业中,通过下列反应使SO2氧化为SO3:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是___________ 。
(2)在实际生产中,选定的温度为400℃~500℃,原因是___________
(3)在实际生产中,采用的压强为常压,原因是___________
(4)在实际生产中,通入过量的空气,原因是___________
(5)尾气中的SO2必须回收,原因是___________ 。
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=___________ 。
 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 95.0 | 97.7 | 98.3 |
(2)在实际生产中,选定的温度为400℃~500℃,原因是
(3)在实际生产中,采用的压强为常压,原因是
(4)在实际生产中,通入过量的空气,原因是
(5)尾气中的SO2必须回收,原因是
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=
您最近半年使用:0次
10 . 从下列实验事实所得出的现象解释或结论错误的是
| 选项 | 实验事实 | 现象解释或结论 |
| A | 将0.1mol/L5mL的Na2S2O3溶液和0.1mol/L5mL的H2SO4溶液混合后平均分装在2支试管中,一支放入冷水中,另一支放入热水中 | 放置在热水的试管中的溶液先出现浑浊,说明升高温度,化学反应速率会加快 |
| B | 锌与稀硫酸反应过程中,开始反应后速率逐渐增大 | 该反应是放热反应 |
| C | 压缩针筒内的NO2和N2O4混合气体,颜色先变深后变浅 | 颜色先变深是浓度变大的原因,后变浅是压强变化对化学平衡的影响 |
| D | 向2mL0.1mol/L的FeCl3溶液中加入1滴KSCN溶液变为红色后,再加入少量KCl固体 | 溶液红色变浅,说明增大生成物浓度会使平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-09-10更新
|
360次组卷
|
4卷引用:安徽省芜湖市无为襄安中学2022-2023学年高二上学期11月期中考试化学试题



