名校
1 . 在 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是
 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是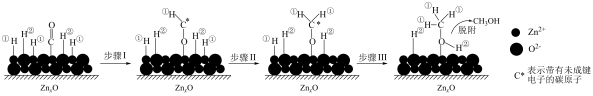
A.吸附在 上的H带正电荷 上的H带正电荷 |
| B.步骤Ⅰ、Ⅱ、Ⅲ均吸收能量 |
C.该过程中有s—  键的形成 键的形成 |
D.合成 过程中不断分离出 过程中不断分离出 ,有利于平衡正向移动 ,有利于平衡正向移动 |
您最近半年使用:0次
2024高三下·全国·专题练习
2 . 推动 的综合利用、实现碳中和是党中央作出的重大战略决策。
的综合利用、实现碳中和是党中央作出的重大战略决策。
(1) 一定条件可转化为
一定条件可转化为 ,
,
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,分子筛膜能选择性分离出 。P点甲醇产率高于T点的原因为
。P点甲醇产率高于T点的原因为___________ 。 与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对
与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对 转化率的影响如图所示,
转化率的影响如图所示, 时
时 转化率低于
转化率低于 和
和 的原因可能为
的原因可能为___________ 。
 的综合利用、实现碳中和是党中央作出的重大战略决策。
的综合利用、实现碳中和是党中央作出的重大战略决策。(1)
 一定条件可转化为
一定条件可转化为 ,
,
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,分子筛膜能选择性分离出
 。P点甲醇产率高于T点的原因为
。P点甲醇产率高于T点的原因为
 与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对
与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对 转化率的影响如图所示,
转化率的影响如图所示, 时
时 转化率低于
转化率低于 和
和 的原因可能为
的原因可能为
您最近半年使用:0次
2024高三下·全国·专题练习
3 . 丙烯是三大合成材料的基本原料之一,可用于生产多种重要有机化工原料。由丙烷制丙烯的两种方法如下:
I.丙烷无氧脱氢法:
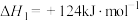
II.丙烷氧化脱氢法: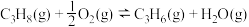

请回答下列问题:
(1)对于反应I,下列条件有利于提高 的平衡转化率的是___________(填字母)
的平衡转化率的是___________(填字母)
(2)某温度下,在刚性密闭容器中充入 发生反应I,起始压强为
发生反应I,起始压强为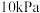 ,平衡时总压强为
,平衡时总压强为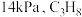 的平衡转化率为
的平衡转化率为___________ 。
(3)一定压强下,向密闭容器中充入一定量的 和
和 ,发生反应
,发生反应
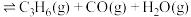 ,
, 的平衡转化率在不同投料比
的平衡转化率在不同投料比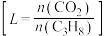 下与温度的关系如图所示,投料比L由小到大的顺序为
下与温度的关系如图所示,投料比L由小到大的顺序为___________ ,判断依据是___________ 。 等副产物,在催化剂的作用下,
等副产物,在催化剂的作用下, 的转化率和
的转化率和 的产率随温度的变化关系如图所示,
的产率随温度的变化关系如图所示, 的选择性:550℃
的选择性:550℃___________ 575℃(填“>”或“<”)。
I.丙烷无氧脱氢法:

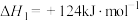
II.丙烷氧化脱氢法:
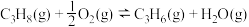

请回答下列问题:
(1)对于反应I,下列条件有利于提高
 的平衡转化率的是___________(填字母)
的平衡转化率的是___________(填字母)| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
 发生反应I,起始压强为
发生反应I,起始压强为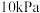 ,平衡时总压强为
,平衡时总压强为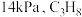 的平衡转化率为
的平衡转化率为(3)一定压强下,向密闭容器中充入一定量的
 和
和 ,发生反应
,发生反应
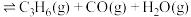 ,
, 的平衡转化率在不同投料比
的平衡转化率在不同投料比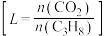 下与温度的关系如图所示,投料比L由小到大的顺序为
下与温度的关系如图所示,投料比L由小到大的顺序为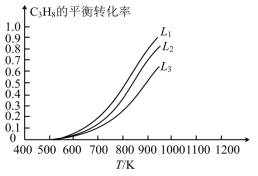
 等副产物,在催化剂的作用下,
等副产物,在催化剂的作用下, 的转化率和
的转化率和 的产率随温度的变化关系如图所示,
的产率随温度的变化关系如图所示, 的选择性:550℃
的选择性:550℃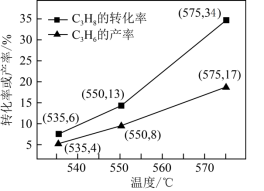
您最近半年使用:0次
4 . 用K2Cr2O7溶液进行下列实验,结合实验,下列说法错误的是
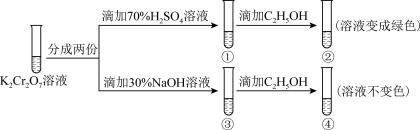
| A.①中溶液橙色加深,③中溶液变黄 |
B.②中 被C2H5OH还原 被C2H5OH还原 |
| C.K2Cr2O7的氧化性强于K2CrO4 |
| D.若向④中加入70%H2SO4溶液至过量,溶液恢复橙色 |
您最近半年使用:0次
名校
5 . 下列事实不能用勒夏特列原理解释的是
| A.25℃时,纯水pH=7;100℃时,纯水的pH<7 |
B.实验室用过氧化氢制取氧气时,常常加入 固体 固体 |
| C.实验室常用排饱和食盐水的方法收集氯气 |
| D.新制的氯水在光照条件下颜色变浅 |
您最近半年使用:0次
6 . 铜盐是五颜六色的。某学习小组发现固体 (白色)、固体
(白色)、固体 (棕黄色)、固体
(棕黄色)、固体 (深褐色)。
(深褐色)。 和
和 溶液呈蓝色,
溶液呈蓝色, 溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
【查阅资料】
1.固体铜盐的颜色与阴离子极化能力有关,随化学键共价性增强,吸收光的能量下降,因此颜色加深。
2.在 溶液中存在如下平衡:
溶液中存在如下平衡:

【提出假设】
1.铜盐的颜色不同与离子种类有关。
2. 溶液呈绿色的原因是溶液中既有黄色的
溶液呈绿色的原因是溶液中既有黄色的 ,又有蓝色的
,又有蓝色的 ,根据光学原理蓝色和黄色的混合色为绿色。
,根据光学原理蓝色和黄色的混合色为绿色。
【设计方案】
回答下列问题:
(1)解释 的颜色深于
的颜色深于 的原因
的原因___________ 。
(2)配制 溶液的方法是
溶液的方法是___________ 。
(3)根据表中信息,补充试剂和数据:饱和___________ 、a=___________ 。
(4)实验4和5中溶液颜色差异的原因___________ (用平衡移动原理解释)。
(5)以上实验说明影响 溶液颜色的因素主要有
溶液颜色的因素主要有___________ 。(答两点即可)
【实验结论】假设1,2成立。
(6) 溶液呈现不同颜色的根本原因与
溶液呈现不同颜色的根本原因与 、
、 和
和___________ 微粒(写结构式)的浓度有关。
 (白色)、固体
(白色)、固体 (棕黄色)、固体
(棕黄色)、固体 (深褐色)。
(深褐色)。 和
和 溶液呈蓝色,
溶液呈蓝色, 溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。【查阅资料】
1.固体铜盐的颜色与阴离子极化能力有关,随化学键共价性增强,吸收光的能量下降,因此颜色加深。
2.在
 溶液中存在如下平衡:
溶液中存在如下平衡:
【提出假设】
1.铜盐的颜色不同与离子种类有关。
2.
 溶液呈绿色的原因是溶液中既有黄色的
溶液呈绿色的原因是溶液中既有黄色的 ,又有蓝色的
,又有蓝色的 ,根据光学原理蓝色和黄色的混合色为绿色。
,根据光学原理蓝色和黄色的混合色为绿色。【设计方案】
| 序号 | 温度/℃ | V( 氯化铜)/mL 氯化铜)/mL | V(饱和硫酸铜)/mL | V(饱和___________)/mL | V(饱和氯化钠)/mL | V(水)/mL | 溶液颜色 |
| 1 | 25 | 4.0 | 无色 | ||||
| 2 | 25 | 4.0 | 无色 | ||||
| 3 | 25 | 4.0 | 蓝色 | ||||
| 4 | 25 | 4.0 | 绿色 | ||||
| 5 | 25 | 2.0 | a | 蓝绿色 | |||
| 6 | 25 | 2.0 | 2.0 | 蓝绿色 | |||
| 7 | 25 | 2.0 | 2.0 | 黄绿色 | |||
| 8 | 50 | 4.0 | 黄绿色 |
(1)解释
 的颜色深于
的颜色深于 的原因
的原因(2)配制
 溶液的方法是
溶液的方法是(3)根据表中信息,补充试剂和数据:饱和
(4)实验4和5中溶液颜色差异的原因
(5)以上实验说明影响
 溶液颜色的因素主要有
溶液颜色的因素主要有【实验结论】假设1,2成立。
(6)
 溶液呈现不同颜色的根本原因与
溶液呈现不同颜色的根本原因与 、
、 和
和
您最近半年使用:0次
2024-01-13更新
|
627次组卷
|
4卷引用:辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题
7 . 血红蛋白可与 结合,更易与
结合,更易与 配位,血红蛋白与
配位,血红蛋白与 配位示意如图所示。血红蛋白
配位示意如图所示。血红蛋白 与
与 、
、 结合的反应可表示为
结合的反应可表示为
②
下列说法中错误的是
 结合,更易与
结合,更易与 配位,血红蛋白与
配位,血红蛋白与 配位示意如图所示。血红蛋白
配位示意如图所示。血红蛋白 与
与 、
、 结合的反应可表示为
结合的反应可表示为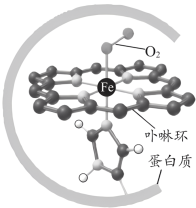

②

下列说法中错误的是
A.相同温度下, | B.反应①②的 、 、 均小于0 均小于0 |
C.图中 的配位数为6 的配位数为6 | D.用高压氧舱治疗 中毒时,平衡①②均逆向移动 中毒时,平衡①②均逆向移动 |
您最近半年使用:0次
2024-01-13更新
|
1066次组卷
|
7卷引用:辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题
辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题2024届辽宁省沈阳市高三教学质量检测(一模)化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)辽宁省沈阳市2024届高三一模化学试题天津市红桥区2024届高三下学期二模化学试题江西省宜春市丰城市第九中学2023-2024学年高三上学期期末考试化学试题
8 . 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
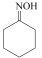 (环己酮肟)
(环己酮肟)
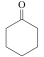 (环己酮)
(环己酮)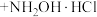
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
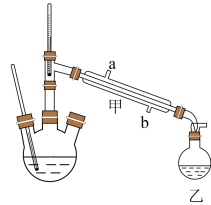
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵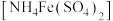 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①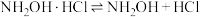
②
③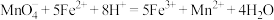
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)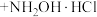
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(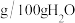 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
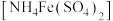 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
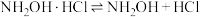
②

③
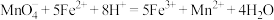
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 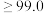 |  |  |

您最近半年使用:0次
2024-01-13更新
|
347次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
名校
解题方法
9 . 工业制硫酸的关键反应为 。T℃时,向
。T℃时,向 恒容密闭容器中按照物质的量之比
恒容密闭容器中按照物质的量之比 通入
通入 和
和 ,测得容器内某些物质的量随时间变化如图。下列说法正确的是
,测得容器内某些物质的量随时间变化如图。下列说法正确的是
 。T℃时,向
。T℃时,向 恒容密闭容器中按照物质的量之比
恒容密闭容器中按照物质的量之比 通入
通入 和
和 ,测得容器内某些物质的量随时间变化如图。下列说法正确的是
,测得容器内某些物质的量随时间变化如图。下列说法正确的是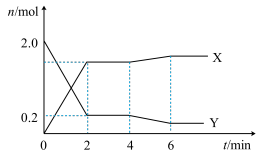
A.用 表示 表示 内的平均反应速率为 内的平均反应速率为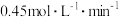 |
B. 时改变的条件可能是降温或增加 时改变的条件可能是降温或增加 的量 的量 |
| C.T℃,正反应的化学平衡常数K为810 |
D. 时,若再加入 时,若再加入 和 和 各 各 ,平衡逆向移动 ,平衡逆向移动 |
您最近半年使用:0次
2024-01-07更新
|
237次组卷
|
4卷引用:湖南省长沙市长郡中学2023-2024学年高三上学期月考(四)化学试题
湖南省长沙市长郡中学2023-2024学年高三上学期月考(四)化学试题(已下线)提升练05 化学平衡常数的计算-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题
名校
10 . 氯水中存在平衡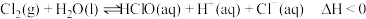 ,下列说法正确的是
,下列说法正确的是
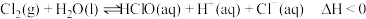 ,下列说法正确的是
,下列说法正确的是A.升高温度,氯水中的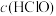 增大 增大 |
| B.氯水中加入少量醋酸钠固体,平衡不发生移动 |
C.该平衡可解释用饱和食盐水除去氯气中混有的 气体的原因 气体的原因 |
D.取两份氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液,若前者产生白色沉淀,后者溶液变蓝色,可以证明上述反应为可逆反应 溶液,若前者产生白色沉淀,后者溶液变蓝色,可以证明上述反应为可逆反应 |
您最近半年使用:0次



