解题方法
1 . 芙蓉洞位于武隆乌江最大支流芙蓉江畔的半山腰上,形成于100万年前,在2007年被列人世界遗产名录,属于武隆喀斯特地质的一部分。某小组研究发现,芙蓉洞内石样质量与温度、日游客流量关系如图所示。

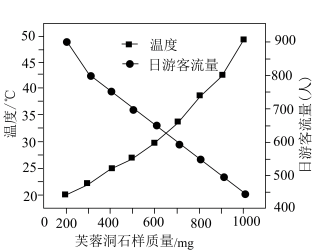
下列叙述错误的是


下列叙述错误的是
| A.芙蓉洞的形成与气候、地理环境有密切关系 |
| B.芙蓉洞形成与风化过程中只发生了物理变化 |
C.日游客流量增大, 浓度增大导致芙蓉洞石样质量减小 浓度增大导致芙蓉洞石样质量减小 |
| D.芙蓉洞石样质量减小过程中发生了化合反应 |
您最近半年使用:0次
2023·浙江·模拟预测
解题方法
2 . 将二氧化碳转化为高附加值化学品是目前研究的热点之一,甲醇是重要的化工原料和优良的替代燃料,因此加氢制甲醇被广泛关注。在催化剂作用下主要发生以下反应。
Ⅰ.

Ⅱ.
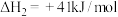
Ⅲ.

(1)反应Ⅲ自发进行的条件是______ 。
(2)恒温恒容条件下,原料气 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
______ 。(对于气相反应,用组分B的平衡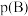 代替
代替 ,记作
,记作 。
。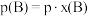 ,p为平衡压强,
,p为平衡压强,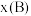 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。)
在 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
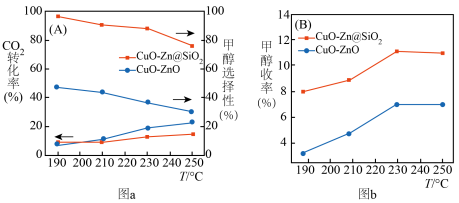
(3)分析在该压强下的最适合反应条件为______ 。
(4)推测在一定温度范围内,随着反应温度的升高, 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是______ 。
(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
(6)在 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线__________ 。
Ⅰ.


Ⅱ.

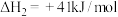
Ⅲ.


(1)反应Ⅲ自发进行的条件是
(2)恒温恒容条件下,原料气
 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
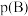 代替
代替 ,记作
,记作 。
。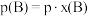 ,p为平衡压强,
,p为平衡压强,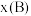 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。) 在
 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
(3)分析在该压强下的最适合反应条件为
(4)推测在一定温度范围内,随着反应温度的升高,
 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
A. 催化剂中 催化剂中 抑制了 抑制了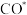 的解吸附,从而抑制 的解吸附,从而抑制 的生成。 的生成。 |
B. 催化剂上主要通过甲酸盐路径加氢生成甲醇。 催化剂上主要通过甲酸盐路径加氢生成甲醇。 |
| C.增大流速,原料气与催化剂碰撞机会多,甲醇产率一定增加。 |
D.随着温度升高,有利于 在催化剂表面反应,平衡转化率增大。 在催化剂表面反应,平衡转化率增大。 |
(6)在
 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
您最近半年使用:0次
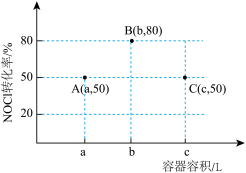
3 . 一定温度下,向三个容积不等的恒容密闭容器中分别投入2molNOCl,发生反应:2NOCl(g) 2NO(g)+Cl2(g)。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2NO(g)+Cl2(g)。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
 2NO(g)+Cl2(g)。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2NO(g)+Cl2(g)。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
| A.A点加入适当催化剂,可以提高NOCl的转化率 |
B.容积为aL的容器达到平衡后再投入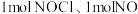 ,平衡不移动 ,平衡不移动 |
| C.A、B两点的压强之比为25:28 |
| D.容积为cL的容器NOCl的平衡转化率小于80% |
您最近半年使用:0次
2023-12-05更新
|
599次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷
吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷重庆市第七中学校2023-2024学年高三上学期月考(12月)化学试题(已下线)专题06 化学反应速率与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
4 . 在一密闭容器中,反应 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增大了 | D. |
您最近半年使用:0次
2023-11-14更新
|
357次组卷
|
25卷引用:吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题
吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题(已下线)【浙江新东方】双师118安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题黑龙江省大庆市东风中学2021-2022学年高二下学期开学考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题天津市第二南开学校2022-2023学年高二上学期9月阶段性线上练习化学试题 天津市宁河区芦台第一中学2022-2023学年高二上学期第一次学习诊断化学试题浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)新疆石河子第一中学2023-2024学年高二上学期11月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题河北省石家庄市第十五中学2023-2024学年高二上学期12月阶段考试化学试题安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题广东省汕头市潮阳区河溪中学2023-2024学年高二上学期月考化学试题
名校
5 . 已知: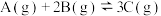
 向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应,
向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
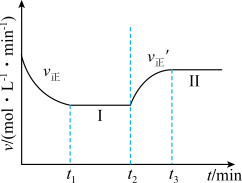
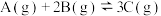
 向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应,
向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.平衡时A的体积分数 |
| B.容器内气体的平均相对分子质量不变,表明反应达到平衡 |
C. 时改变的条件:向容器中加入B 时改变的条件:向容器中加入B |
D.平衡常数 |
您最近半年使用:0次
2023-11-04更新
|
326次组卷
|
4卷引用:吉林省梅河口市第五中学2023-2024学年高二上学期12月月考化学试题
名校
6 . 某固定容积的密闭容器中发生反应: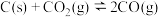 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
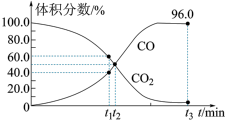
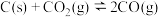 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
A. 时,CO2的转化率为20.0% 时,CO2的转化率为20.0% |
B. 时,该反应体系处于平衡状态 时,该反应体系处于平衡状态 |
C. 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 |
D. 时,该反应的 时,该反应的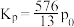 [气体分压(p分)=气体总压(p总)×体积分数] [气体分压(p分)=气体总压(p总)×体积分数] |
您最近半年使用:0次
名校
解题方法
7 . 请根据有关知识,填写下列空白:
(1)一种难溶的废弃矿渣杂卤石,其主要成分可表示为K2SO4·MgSO4·2CaSO4·2H2O,已知它在水溶液中存在如下平衡:K2SO4·MgSO4·2CaSO4·2H2O(s) 2K+(aq)+4
2K+(aq)+4 (aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
(aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
用化学平衡移动原理解释Ca(OH)2溶液能溶解出杂卤石中K+的原因:_____ 。
(2)向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L−1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.8×10−10,忽略溶液的体积变化,请计算:完全沉淀后,溶液中c(Ag+)=_____ mol·L−1.
(3)N2H4是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。
写出N2H4(g)完全燃烧生成氮气和气态水热化学方程式_____ 。
(4)硫酸亚铁溶液常压蒸干得到的固体物质是_____ ,原因是_____ 。
(5)NH4Cl溶液可作焊接时的除锈剂,原因是_____ 。
(1)一种难溶的废弃矿渣杂卤石,其主要成分可表示为K2SO4·MgSO4·2CaSO4·2H2O,已知它在水溶液中存在如下平衡:K2SO4·MgSO4·2CaSO4·2H2O(s)
 2K+(aq)+4
2K+(aq)+4 (aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
(aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。用化学平衡移动原理解释Ca(OH)2溶液能溶解出杂卤石中K+的原因:
(2)向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L−1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.8×10−10,忽略溶液的体积变化,请计算:完全沉淀后,溶液中c(Ag+)=
(3)N2H4是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。
写出N2H4(g)完全燃烧生成氮气和气态水热化学方程式
(4)硫酸亚铁溶液常压蒸干得到的固体物质是
(5)NH4Cl溶液可作焊接时的除锈剂,原因是
您最近半年使用:0次
名校
8 . 列实验方案设计、现象和结论都正确的是
| 目的 | 实验方案设计 | 现象和结论 | |
| A | 探究压强对平衡的影响 | 在针筒中充入一定量的NO2气体,压缩针筒,从针简顶部观察到气体颜色变浅 | 压强增大,平衡向气体体积减小的方向移动 |
| B | 探究浓度对平衡移动的影响 | 向K2Cr2O7溶液中缓慢滴加浓盐酸,黄色变为橙色 | 增大c(H+),平衡向生成 的方向移动 的方向移动 |
| C | 检验某溶液中是否含有Fe2+离子 | 向该溶液中滴加几滴新制氯水, 振荡,再加入少量KSCN溶液 | 溶液变为血红色,则该溶液中含有Fe2+离子 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-04-06更新
|
161次组卷
|
3卷引用:吉林省长春外国语学校2023-2024学年高二下学期开学化学试题
吉林省长春外国语学校2023-2024学年高二下学期开学化学试题(已下线)【2023】【高二上】【源清中学】【期末考】【高中化学】【廖汨平收集】江西省宜丰中学创新部2023-2024学年高一上学期10月月考化学试题
名校
解题方法
9 .  的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:

已知 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: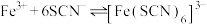 (红色);
(红色);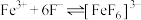 (无色)。
(无色)。
下列说法不正确的是
 的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:
已知
 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: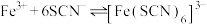 (红色);
(红色);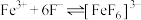 (无色)。
(无色)。下列说法不正确的是
A.Ⅰ中溶液呈黄色可能是由 水解产物的颜色引起的 水解产物的颜色引起的 |
B. 与 与 的配位能力强于 的配位能力强于 |
C.为了能观察到溶液Ⅰ中 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
| D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近半年使用:0次
2023-03-25更新
|
585次组卷
|
8卷引用:吉林省长春外国语学校2022-2023学年高二下学期3月月考化学试题
10 . 某化学工作者研究在不同 时,
时, 溶液对
溶液对 分解的催化作用。
分解的催化作用。
已知:a. 为红色固体,难溶于水,溶于硫酸生成
为红色固体,难溶于水,溶于硫酸生成 和
和 。
。
b.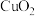 为棕褐色固体,难溶于水,溶于硫酸生成
为棕褐色固体,难溶于水,溶于硫酸生成 和
和 。
。
c. 为弱酸性。
为弱酸性。
请回答下列有关问题:
(1)写出 的电离方程式
的电离方程式___________ ;___________
(2)写出 的电子式
的电子式___________ ; 中
中 原子的杂化类型是
原子的杂化类型是___________ 。经检验生成的气体均为 ,Ⅰ中
,Ⅰ中 催化分解
催化分解 的化学方程式是
的化学方程式是___________ 。
(3)要检验某铜粉是否含 ,写出具体操作、现象及结论
,写出具体操作、现象及结论___________ 。
(4)结合离子方程式,运用化学反应原理解释Ⅲ中生成的沉淀多于Ⅱ中的原因:___________ 。
 时,
时, 溶液对
溶液对 分解的催化作用。
分解的催化作用。| 编号 | 实验 | 现象 |
| Ⅰ | 向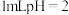 的 的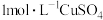 溶液中加入 溶液中加入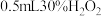 溶液 溶液 | 出现少量气泡 |
| Ⅱ | 向 的 的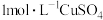 溶液中加入 溶液中加入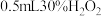 溶液 溶液 | 立即产生少量棕褐色沉淀,出现较明显气泡 |
| Ⅲ | 向 的 的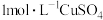 溶液中加入 溶液中加入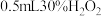 溶液 溶液 | 立即产生大量棕褐色沉淀,产生大量气泡 |
 为红色固体,难溶于水,溶于硫酸生成
为红色固体,难溶于水,溶于硫酸生成 和
和 。
。b.
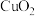 为棕褐色固体,难溶于水,溶于硫酸生成
为棕褐色固体,难溶于水,溶于硫酸生成 和
和 。
。c.
 为弱酸性。
为弱酸性。请回答下列有关问题:
(1)写出
 的电离方程式
的电离方程式(2)写出
 的电子式
的电子式 中
中 原子的杂化类型是
原子的杂化类型是 ,Ⅰ中
,Ⅰ中 催化分解
催化分解 的化学方程式是
的化学方程式是(3)要检验某铜粉是否含
 ,写出具体操作、现象及结论
,写出具体操作、现象及结论(4)结合离子方程式,运用化学反应原理解释Ⅲ中生成的沉淀多于Ⅱ中的原因:
您最近半年使用:0次



