名校
1 . 根据下列实验操作与现象所得出的结论正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液由浅绿色变为黄色 | 氧化性:H2O2>>Fe2+ |
| B | 向4mL0.1mol/LK2CrO4溶液中缓慢滴加1molL稀硫酸,溶液由黄色变为橙色 | 增大c(H+)有利于 转化为 转化为 |
| C | 等体积pH=2的HX和HY两种酸溶液分别与足量的锌粒反应,用排水法收集气体,HX溶液放出的氢气多且反应速率快 | 证明HX的酸性比HY强 |
| D | 室温下,向浓度均为0.05mol/L的NaI和NaCl的混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列事实不能用勒夏特列原理(化学平衡移动原理)解释的是
| A.合成氨时,选定温度为400~500℃,而不是常温 |
| B.人体血液的pH稳定在7.4±0.05范围内 |
| C.氯气在水中的溶解度大于在饱和食盐水中的溶解度 |
| D.生活中,可用热的纯碱溶液除油污 |
您最近一年使用:0次
2024-01-18更新
|
79次组卷
|
3卷引用:四川省雅安市多校联考2023-2024学年高二上学期12月月考化学试题
名校
解题方法
3 . I:室温下,通过下列实验探究 溶液的性质。
溶液的性质。
依据实验操作和现象,回答下列问题:
(1)向0.1mol/L 溶液滴入酚酞溶液,观察到的现象是
溶液滴入酚酞溶液,观察到的现象是___________ ,原因___________ (用离子方程式表示)。
(2)实验3中随 的不断通入,溶液中
的不断通入,溶液中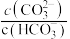
___________ (填减小、不变或增大)。
(3)常温下, 均为12的
均为12的 溶液与NaOH溶液中水电离出的
溶液与NaOH溶液中水电离出的 之比为
之比为___________ 。
Ⅱ:① 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 气体⑤碘水⑥氨水⑦
气体⑤碘水⑥氨水⑦ 溶液
溶液
(4)向②中通入足量④,发生反应的离子方程式为___________ 。
(5)为得到浓度较大的⑤,实验室在配制时,常加入 ,溶液中存在如下平衡:
,溶液中存在如下平衡: ,向⑤中加入一定量的①,该平衡将
,向⑤中加入一定量的①,该平衡将___________ (填“正向”或“逆向”)移动。
Ⅲ:
(6)泡沫灭火器原理(用离子方程式表示):___________
(7)配置 溶液为什么要将
溶液为什么要将 固体溶解在浓盐酸中(用离子方程式表示):
固体溶解在浓盐酸中(用离子方程式表示):___________
(8)加热蒸干 为什么得不到
为什么得不到 原理(用化学方程式表示):
原理(用化学方程式表示):___________
 溶液的性质。
溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 用 试纸测定0.1mol/L 试纸测定0.1mol/L 溶液的 溶液的 ,测得 ,测得 约为12 约为12 |
| 2 | 向0.1mol/L 溶液中加入过量0.2mol/L 溶液中加入过量0.2mol/L 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 3 | 向0.1mol/L 溶液中通入过量 溶液中通入过量 ,测得溶液 ,测得溶液 约为8 约为8 |
| 4 | 向0.1mol/L 溶液中滴加几滴0.05mol/L 溶液中滴加几滴0.05mol/L ,观察不到实验现象 ,观察不到实验现象 |
(1)向0.1mol/L
 溶液滴入酚酞溶液,观察到的现象是
溶液滴入酚酞溶液,观察到的现象是(2)实验3中随
 的不断通入,溶液中
的不断通入,溶液中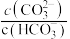
(3)常温下,
 均为12的
均为12的 溶液与NaOH溶液中水电离出的
溶液与NaOH溶液中水电离出的 之比为
之比为Ⅱ:①
 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 气体⑤碘水⑥氨水⑦
气体⑤碘水⑥氨水⑦ 溶液
溶液(4)向②中通入足量④,发生反应的离子方程式为
(5)为得到浓度较大的⑤,实验室在配制时,常加入
 ,溶液中存在如下平衡:
,溶液中存在如下平衡: ,向⑤中加入一定量的①,该平衡将
,向⑤中加入一定量的①,该平衡将Ⅲ:
(6)泡沫灭火器原理(用离子方程式表示):
(7)配置
 溶液为什么要将
溶液为什么要将 固体溶解在浓盐酸中(用离子方程式表示):
固体溶解在浓盐酸中(用离子方程式表示):(8)加热蒸干
 为什么得不到
为什么得不到 原理(用化学方程式表示):
原理(用化学方程式表示):
您最近一年使用:0次
名校
4 . 化学在日常生活和生产中有着重要的应用。下列说法不正确的是
| A.中和反应反应热的测定实验中的玻璃搅拌器换成铜制搅拌器效果更好 |
| B.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化 |
| C.工业上SO2催化氧化制取SO3时,适当增大氧气浓度可以增大SO2的平衡转化率 |
| D.配制FeCl3溶液时加入少量的盐酸,抑制Fe3+水解 |
您最近一年使用:0次
名校
5 . 人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应: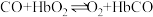 ,37℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,导致人的智力受损。据此,下列结论错误的是
,37℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,导致人的智力受损。据此,下列结论错误的是
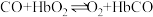 ,37℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,导致人的智力受损。据此,下列结论错误的是
,37℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,导致人的智力受损。据此,下列结论错误的是A.CO与HbO2反应的平衡常数 |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动 |
您最近一年使用:0次
名校
6 . 下列事实不能用勒夏特列原理解释的是
| A.向氯水中加入CaCO3固体提高HClO的浓度 |
| B.盛有Na2S2O3溶液与稀硫酸混合液的试管浸入热水时迅速变浑浊 |
| C.向0.1mol/LK2Cr2O7溶液中滴入10滴浓NaOH溶液,溶液由橙色变黄色 |
| D.红棕色的NO2,加压后颜色先变深后变浅 |
您最近一年使用:0次
名校
7 . 下列不能用勒夏特列原理解释的是
| A.向K2Cr2O7溶液中加入少量浓NaOH溶液,溶液由橙色变为黄色 |
| B.实验室常用排饱和食盐水法收集Cl2 |
| C.H2(g)、I2(g)、HI(g)平衡混合气体加压后颜色变深 |
| D.将盛有热CuCl2溶液的试管置于冷水浴中,试管中溶液由黄绿色变为蓝绿色 |
您最近一年使用:0次
名校
解题方法
8 . 在一个固定体积的密闭容器中,加入 和
和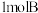 ,发生反应
,发生反应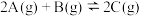 ,达到平衡时,C的物质的量浓度为
,达到平衡时,C的物质的量浓度为 ,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是
,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是 的是
的是
 和
和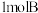 ,发生反应
,发生反应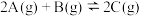 ,达到平衡时,C的物质的量浓度为
,达到平衡时,C的物质的量浓度为 ,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是
,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是 的是
的是A.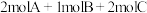 | B. |
C. | D. |
您最近一年使用:0次
名校
9 . 化学与生产、生活和社会发展密切相关,下列叙述不正确的是
| A.考古队为“经远舰”舰体焊接镁合金实施保护,采用的是牺牲阳极法 |
| B.茶叶等包装中加入还原性铁粉,能显著延长茶叶的储存时间 |
| C.西周时期发明的“酒曲”催化酿酒工艺,是利用了“酒曲”使平衡正向移动的原理 |
D.硫酸工业中,为提高 的转化率,通入过量的空气 的转化率,通入过量的空气 |
您最近一年使用:0次
名校
10 . 下列现象不能用平衡移动原理解释的是
A.室温下,将 平衡体系压缩体积后颜色加深 平衡体系压缩体积后颜色加深 |
B. ,把 ,把 球浸泡在冰水中,气体颜色变浅 球浸泡在冰水中,气体颜色变浅 |
C.工业制取钾 ,选取合适的温度,使 ,选取合适的温度,使 变成蒸气从体系逸出 变成蒸气从体系逸出 |
| D.实验室制备氯气,用排饱和食盐水收集氯气 |
您最近一年使用:0次



