名校
1 . 下列事实不能用平衡移动原理解释的是
| A.铁质器件附有铜质配件,久置,在接触处铁易生锈 |
| B.用稀硫酸洗涤BaSO4沉淀比用等体积蒸馏水洗涤损失的BaSO4少 |
| C.加氨水除去氯化铵中的氯化镁 |
| D.电镀实验中,用[Cu(NH3)4]SO4溶液作电镀液比用CuSO4溶液得到的铜镀层光亮牢固 |
您最近一年使用:0次
2 . 工业上以铬铁矿( ,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题:
,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题: (铁、铬分别为
(铁、铬分别为 、
、 价)转化为
价)转化为 和
和 ,同时A1、Si氧化物转化为可溶性钠盐。
,同时A1、Si氧化物转化为可溶性钠盐。
(1)“焙烧”过程与 有关的化学反应中,氧化剂和还原剂物质的量之比为
有关的化学反应中,氧化剂和还原剂物质的量之比为___________ 。“浸取”过程所得滤渣的用途有___________ (合理即可)。
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度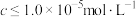 时,可认为已除尽。
时,可认为已除尽。___________ ;从平衡移动的角度解释“酸化”过程加入 的原因
的原因___________ 。
(3)“冷却结晶”时,相关化学反应方程式为___________ 。
(4) 价铬的化合物毒性较大,需将
价铬的化合物毒性较大,需将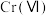 转化为毒性较低的
转化为毒性较低的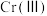 ;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。
;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。 :向含铬(Ⅵ)废水中加入适量
:向含铬(Ⅵ)废水中加入适量 溶液发生反应,生成在乙醚中较稳定存在的
溶液发生反应,生成在乙醚中较稳定存在的 价的含铬氧化物
价的含铬氧化物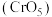 ,1mol
,1mol 中含过氧键
中含过氧键 的数量是
的数量是___________ 。
②电解开始时,A极上主要发生的电极反应式为___________ 。
③电解产生的 将
将 还原为
还原为 同时产生
同时产生 ,其离子方程式为
,其离子方程式为___________ 。
 ,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题:
,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题: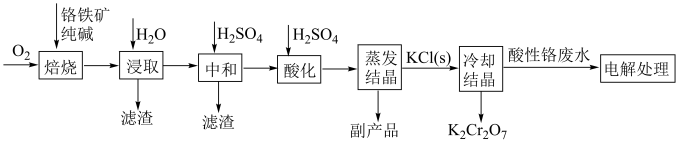
 (铁、铬分别为
(铁、铬分别为 、
、 价)转化为
价)转化为 和
和 ,同时A1、Si氧化物转化为可溶性钠盐。
,同时A1、Si氧化物转化为可溶性钠盐。(1)“焙烧”过程与
 有关的化学反应中,氧化剂和还原剂物质的量之比为
有关的化学反应中,氧化剂和还原剂物质的量之比为(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度
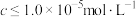 时,可认为已除尽。
时,可认为已除尽。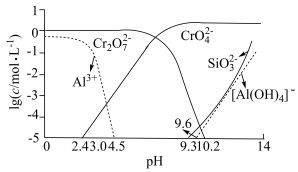
 的原因
的原因(3)“冷却结晶”时,相关化学反应方程式为
(4)
 价铬的化合物毒性较大,需将
价铬的化合物毒性较大,需将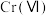 转化为毒性较低的
转化为毒性较低的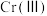 ;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。
;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。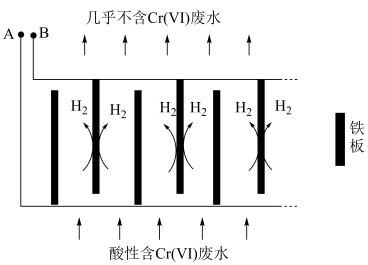
 :向含铬(Ⅵ)废水中加入适量
:向含铬(Ⅵ)废水中加入适量 溶液发生反应,生成在乙醚中较稳定存在的
溶液发生反应,生成在乙醚中较稳定存在的 价的含铬氧化物
价的含铬氧化物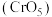 ,1mol
,1mol 中含过氧键
中含过氧键 的数量是
的数量是②电解开始时,A极上主要发生的电极反应式为
③电解产生的
 将
将 还原为
还原为 同时产生
同时产生 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
2024-04-11更新
|
279次组卷
|
2卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学
名校
3 . CH3CHO在NaOH溶液作用下制取2-丁烯醛的历程如下:
下列说法不正确 的是

下列说法
| A.OH-是该反应的催化剂 |
B.CH3CHO分子中甲基上的“ ”比 ”比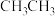 中的“ 中的“ ”更易电离出H+ ”更易电离出H+ |
| C.反应(4)加热失水有利于反应(3)平衡正向移动 |
| D.CH3CHO与CH3CH2CHO的混合液在NaOH溶液作用下最多可得到2种羟基醛 |
您最近一年使用:0次
2024-04-10更新
|
535次组卷
|
5卷引用:2024届浙江省嘉兴市高三下学期二模化学试题
2024届浙江省嘉兴市高三下学期二模化学试题(已下线)化学(浙江卷01)-2024年高考押题预测卷湖北省沙市中学2024届高三下学期模拟预测化学试题(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)(已下线)选择题11-16
名校
解题方法
4 . 相变离子液体体系因节能潜力大被认为是新一代 吸收剂,某新型相变离子液体X吸收
吸收剂,某新型相变离子液体X吸收 的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
 吸收剂,某新型相变离子液体X吸收
吸收剂,某新型相变离子液体X吸收 的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是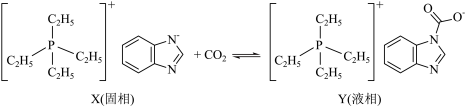
| A.X的阳离子中所有原子(除H外)均达到最外层8电子稳定状态 |
B.真空条件下有利于Y解析出 |
| C.X的阴离子中所有N均提供2个电子参与大π键的形成 |
| D.Y的熔点比X的低,可推知阴离子半径:Y>X |
您最近一年使用:0次
2024-04-07更新
|
416次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2024届高三下学期模拟试卷(一) 化学试题
解题方法
5 . 某小组同学探究铁离子与苯酚的反应。
已知: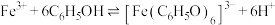 ;
;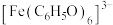 为紫色配合物。
为紫色配合物。
(1)配制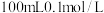 苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、
苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、__________ 。
(2)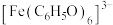 中,提供空轨道用以形成配位键的微粒是
中,提供空轨道用以形成配位键的微粒是__________ ,配位数为__________ 。
(3)探究铁盐种类和pH对苯酚与 显色反应的影响。
显色反应的影响。
查阅资料:
ⅰ. 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;
ⅱ.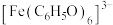 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与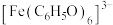 浓度在一定范围内成正比。
浓度在一定范围内成正比。
提出猜想:猜想1: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
猜想2: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
猜想3: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
进行实验:
常温下,用盐酸调节pH,配制得到pH分别为a和b的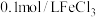 溶液(
溶液( );用硫酸调节pH,配制得到pH分别为a和b的
);用硫酸调节pH,配制得到pH分别为a和b的 溶液。取4支试管各加入
溶液。取4支试管各加入 苯酚溶液,按实验1~4分别再加入0.1mL含
苯酚溶液,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
结果讨论:实验结果为
①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是__________________ 。
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中试剂M为__________________ 。(限选试剂:NaCl溶液、 溶液、NaCl固体、
溶液、NaCl固体、 固体)。
固体)。
③根据实验1~6的结果,小组同学得出猜想1不成立,猜想2成立,且 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是:
的显色反应起抑制作用,得出此结论的依据是: 、A1
、A1__________ A6(填“>”“<”或者“=”)。
④根据实验1~6的结果,小组同学得出猜想3成立,且 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是______________________________ 。
(4)通过以上实验结论分析:与苯酚相比,对羟基苯甲酸(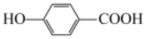 )与
)与 溶液发生显色反应
溶液发生显色反应__________ (填“容易”或“更难”)。
(5)实验室中常用某些配合物的性质进行物质的检验,请举一例子并说明现象____________ 。
已知:
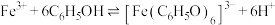 ;
;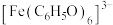 为紫色配合物。
为紫色配合物。(1)配制
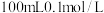 苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、
苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、(2)
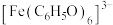 中,提供空轨道用以形成配位键的微粒是
中,提供空轨道用以形成配位键的微粒是(3)探究铁盐种类和pH对苯酚与
 显色反应的影响。
显色反应的影响。查阅资料:
ⅰ.
 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;ⅱ.
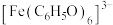 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与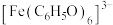 浓度在一定范围内成正比。
浓度在一定范围内成正比。提出猜想:猜想1:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响猜想2:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响猜想3:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响进行实验:
常温下,用盐酸调节pH,配制得到pH分别为a和b的
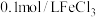 溶液(
溶液( );用硫酸调节pH,配制得到pH分别为a和b的
);用硫酸调节pH,配制得到pH分别为a和b的 溶液。取4支试管各加入
溶液。取4支试管各加入 苯酚溶液,按实验1~4分别再加入0.1mL含
苯酚溶液,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
| 序号 | 含 | 吸光度 | |
|
| |||
1 |
| / | A1 | |
2 |
| / | A2 | |
3 | / |
| A3 | |
4 | / |
| A4 | |

①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中试剂M为
 溶液、NaCl固体、
溶液、NaCl固体、 固体)。
固体)。
| 序号 | 含 | 再加入的试剂 | 吸光度 | |
|
| ||||
5 | / |
| NaCl固体 | A5 | |
6 |
| / | 试剂M | A6 | |
 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是:
的显色反应起抑制作用,得出此结论的依据是: 、A1
、A1④根据实验1~6的结果,小组同学得出猜想3成立,且
 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是(4)通过以上实验结论分析:与苯酚相比,对羟基苯甲酸(
 )与
)与 溶液发生显色反应
溶液发生显色反应(5)实验室中常用某些配合物的性质进行物质的检验,请举一例子并说明现象
您最近一年使用:0次
解题方法
6 . 尿素[CO(NH2)2]是一种重要的氮肥。工业上以CO2和NH3为原料合成尿素,在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
反应Ⅱ:H2NCOONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=
CO(NH2)2(s)+H2O(g) ΔH2=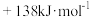
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3
(1)CO2的电子式为___________ ;1mol CO(NH2)2中含有___________ molπ键。
(2)反应Ⅰ的熵变ΔS___________  填“
填“ ”“
”“ ”或“
”或“ ”
” ,反应Ⅲ的
,反应Ⅲ的 H3=
H3=___________ 。
(3)下列关于尿素合成的说法正确的是___________。
反应Ⅰ:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
反应Ⅱ:H2NCOONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=
CO(NH2)2(s)+H2O(g) ΔH2=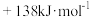
总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3(1)CO2的电子式为
(2)反应Ⅰ的熵变ΔS
 填“
填“ ”“
”“ ”或“
”或“ ”
” ,反应Ⅲ的
,反应Ⅲ的 H3=
H3=(3)下列关于尿素合成的说法正确的是___________。
| A.及时分离出尿素可促使反应Ⅱ向正反应方向移动 |
| B.从合成塔出来的混合气体分离出水蒸气后可以循环使用 |
| C.保持容积不变,充入惰性气体增大压强,可提高总反应Ⅲ的反应速率 |
| D.保持压强不变,降低氨碳比[n(NH3)/n(CO2)]可提高反应Ⅰ中NH3的平衡转化率 |
您最近一年使用:0次
名校
解题方法
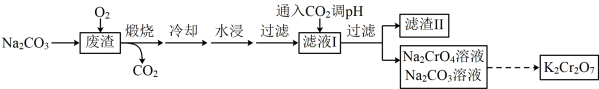
7 . 以某冶金工业产生的废渣(含 、
、 及少量的
及少量的 )为原料,根据如图流程可制备
)为原料,根据如图流程可制备 ,下列说法错误的是
,下列说法错误的是
 、
、 及少量的
及少量的 )为原料,根据如图流程可制备
)为原料,根据如图流程可制备 ,下列说法错误的是
,下列说法错误的是
A.煅烧过程 发生的反应为 发生的反应为 |
B.滤渣Ⅱ中的成分是 |
C.可循环使用的物质是 和 和 |
D.由 转化为 转化为 的过程中需加入KCl 的过程中需加入KCl |
您最近一年使用:0次
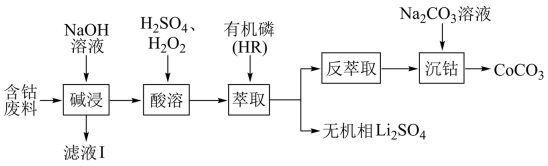
8 . 利用含钴废料(主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图:
已知:萃取 的反应原理:
的反应原理: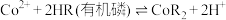 。下列说法错误的是
。下列说法错误的是
A.“滤液Ⅰ”中溶质的主要成分是 |
B.“酸溶”反应中 做氧化剂 做氧化剂 |
C.“反萃取”中可加入 分离出 分离出 |
D.“沉钴”时 溶液滴加速率不宜过快,目的是防止生成 溶液滴加速率不宜过快,目的是防止生成 |
您最近一年使用:0次
9 . 尿素是一种适用于各种土壤和植物的有机态氮肥,是首个由无机物人工合成的有机物。以 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与 在一定条件下反应制得
在一定条件下反应制得 。
。
①该反应的化学方程式是___________ 。
② 晶体中含有的化学键有
晶体中含有的化学键有___________ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
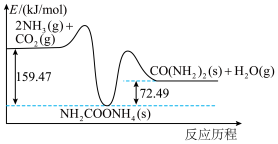
(2) 和
和 合成尿素
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:___________ 。
(3)在恒容密闭容器中发生反应: ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。
(4)在恒容密闭容器中发生反应: ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[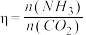 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
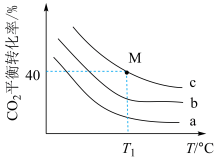
①曲线a代表的投料比为___________ ;
②若 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为___________  ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为___________  (列出计算式即可)。
(列出计算式即可)。
 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与
 在一定条件下反应制得
在一定条件下反应制得 。
。①该反应的化学方程式是
②
 晶体中含有的化学键有
晶体中含有的化学键有A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(2)
 和
和 合成尿素
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:
(3)在恒容密闭容器中发生反应:
 ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。A.单位时间内每消耗44g ,同时生成18g ,同时生成18g |
| B.容器中混合气体平均摩尔质量不变 |
C.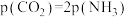 |
D. 的分压保持不变 的分压保持不变 |
(4)在恒容密闭容器中发生反应:
 ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[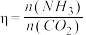 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
①曲线a代表的投料比为
②若
 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为 ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解题方法
10 . 为达到下列实验目的,对应的操作及原理均正确的是
| 选项 | 实验目的 | 操作 | 原理 |
| A. | 分离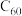 与 与 | 向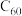 与 与 的混合物中加入与 的混合物中加入与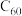 适配的杯酚,再加入甲苯溶解 适配的杯酚,再加入甲苯溶解 ,过滤,滤液中加入氯仿溶解杯酚 ,过滤,滤液中加入氯仿溶解杯酚 | 杯酚与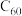 形成超分子,通过尺寸匹配实现分子识别 形成超分子,通过尺寸匹配实现分子识别 |
| B. | 检验硫代硫酸钠中是否混有亚硫酸钠 | 取样,加入稀盐酸,将生成的气体通入品红溶液 | 亚硫酸钠与盐酸反应生成的二氧化硫能使品红溶液褪色 |
| C. | 检验乙醇中是否混有乙醛 | 取待测液,加入酸性高锰酸钾溶液 | 醛基能被酸性高锰酸钾氧化 |
| D. | 探究浓度对化学平衡移动的影响 | 将5mL0.005mol/L的 溶液与5mL0.015mol/L的 溶液与5mL0.015mol/L的 溶液混合,再加 溶液混合,再加 固体 固体 | 在其他条件不变的情况下,增大生成物浓度,平衡向逆反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次