名校
1 . 科学探究是化学学科核心素养之一,下列实验方案设计中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明 | 平衡向逆反应方向移动向 和KSCN的混合溶液中,加入少量KCl固体 和KSCN的混合溶液中,加入少量KCl固体 |
| B | 探究 和 和 的反应存在一定的限度 的反应存在一定的限度 | 将12mL 0.01 KI溶液与2mL 0.005 KI溶液与2mL 0.005  溶液混合,充分反应后分成两份,一份滴加几滴KSCN溶液,另一份滴加几滴淀粉溶液 溶液混合,充分反应后分成两份,一份滴加几滴KSCN溶液,另一份滴加几滴淀粉溶液 |
| C | 探究碳酸和醋酸酸性强弱 | 取2mL碳酸钠溶液于试管中,向其中滴加1~2滴稀醋酸溶液 |
| D | 证明过氧化氢有氧化性 | 将足量的 溶液滴入酸性高锰酸钾溶液中 溶液滴入酸性高锰酸钾溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
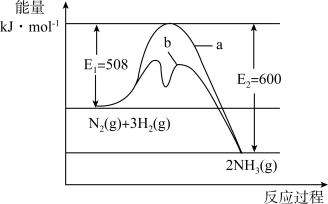
(1)根据图提供的信息,写出该反应的热化学方程式___________ ,在图中曲线___________ (填“a”或“b”)表示加入铁触媒的能量变化曲线,判断理由是___________ 。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=___________ ,该温度下的平衡常数K=___________ 。(小数点后保留3位有效数字)
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正___________ v逆(填“大于”、“小于”或“等于”)。

(1)根据图提供的信息,写出该反应的热化学方程式
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
| A.3v(H2)正=2v(NH3)逆 |
| B.单位时间内生成n mol N2的同时生成2n mol NH3 |
| C.混合气体的密度不再改变 |
| D.容器内压强不随时间的变化而变化 |
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正
您最近一年使用:0次
2023-11-04更新
|
80次组卷
|
2卷引用:甘肃省兰州市教育局第四片区联考2023-2024学年高二上学期期中考试化学试题
3 . 在一定条件下的溶液中,反应:FeCl3+3KSCN Fe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,改变下列条件,能使平衡逆向移动的是
Fe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,改变下列条件,能使平衡逆向移动的是
 Fe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,改变下列条件,能使平衡逆向移动的是
Fe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,改变下列条件,能使平衡逆向移动的是| A.加入少量KSCN固体 | B.加入少量FeCl3固体 |
| C.加入少量KCl固体 | D.加入少量氢氧化钠固体 |
您最近一年使用:0次
名校
解题方法
4 . 下列事实不能用勒夏特列原理解释的是
| A.Fe(SCN)3溶液中加入少量固体KSCN后颜色变深 |
| B.把食品存放在冰箱里可延长保质期 |
| C.合成氨反应,为提高原料的转化率,理论上应采取降低温度的措施 |
| D.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 |
您最近一年使用:0次
2023-10-17更新
|
495次组卷
|
7卷引用:甘肃省兰州第一中学2023-2024学年高二上学期11月期中考试化学试题
5 . 回答下列问题
(1)能够使化学平衡移动的因素有________ 、________ 、________ 。
(2)可逆反应A(g)+2B(g) 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡______ 移动(填正向、逆向、不),B的转化率_______ , v(正) ________ 。(填增大、减小、不变)。
(1)能够使化学平衡移动的因素有
(2)可逆反应A(g)+2B(g)
 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
您最近一年使用:0次
6 . 向FeCl3(黄色)+3KSCN Fe(SCN)3(血红色)+3KCl平衡体系中,加入下列物质,能使溶液血红色消失的是
Fe(SCN)3(血红色)+3KCl平衡体系中,加入下列物质,能使溶液血红色消失的是
 Fe(SCN)3(血红色)+3KCl平衡体系中,加入下列物质,能使溶液血红色消失的是
Fe(SCN)3(血红色)+3KCl平衡体系中,加入下列物质,能使溶液血红色消失的是| A.AgNO3 | B.KCl | C.H2O | D.Fe |
您最近一年使用:0次
7 . 下列叙述及解释正确的是
A.对于N2+3H2 2NH3,平衡后,压强不变,充入Ar,平衡左移 2NH3,平衡后,压强不变,充入Ar,平衡左移 |
B.H2(g)+I2(g) 2HI(g) ΔH<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 2HI(g) ΔH<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 |
C.FeCl3+3KSCN Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl固体,因为平衡向逆反应方向移动,故体系颜色变浅 Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl固体,因为平衡向逆反应方向移动,故体系颜色变浅 |
D.2NO2(g)(红棕色) N2O4(g)(无色) ΔH<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 N2O4(g)(无色) ΔH<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 |
您最近一年使用:0次
名校
8 . 铬酸钾溶液中存在如下平衡: (橙色)
(橙色) (黄色),下列说法正确的是
(黄色),下列说法正确的是
 (橙色)
(橙色) (黄色),下列说法正确的是
(黄色),下列说法正确的是A.加 固体,溶液的橙色加深 固体,溶液的橙色加深 | B.加水,溶液中 的浓度增大 的浓度增大 |
C.加 固体,溶液的橙色加深 固体,溶液的橙色加深 | D.加亚硫酸钠溶液,溶液的橙色加深 |
您最近一年使用:0次
9 . 甲醇是重要的工业原料,应用前景广阔。甲醇可由二氧化碳与氢气合成,恒容密闭容器内发生反应如下: 。研究温度对甲醇产率的影响如图所示,下列说法正确的是
。研究温度对甲醇产率的影响如图所示,下列说法正确的是

 。研究温度对甲醇产率的影响如图所示,下列说法正确的是
。研究温度对甲醇产率的影响如图所示,下列说法正确的是
| A.平衡后向体系内加入CO2,平衡正向移动,CO2的转化率增大 |
| B.正反应放热 |
| C.使用催化剂能提高甲醇的产率 |
| D.缩小体积,增大压强,平衡正向移动,平衡常数增大 |
您最近一年使用:0次
名校
解题方法
10 . 下列叙述及解释正确的是
A.  ,达到平衡后,对平衡体系采取扩大容积、减小压强的措施,体系颜色不变 ,达到平衡后,对平衡体系采取扩大容积、减小压强的措施,体系颜色不变 |
B. (无色) (无色)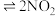 (红棕色) (红棕色)  ,达到平衡后,对平衡体系采取缩小容积、增大压强的措施, ,达到平衡后,对平衡体系采取缩小容积、增大压强的措施, 的转化率增大 的转化率增大 |
C. ,在达到平衡后,向溶液中加少量KCl固体,平衡逆向移动 ,在达到平衡后,向溶液中加少量KCl固体,平衡逆向移动 |
D. ,在达到平衡后,保持压强不变,充入氦气,平衡不移动 ,在达到平衡后,保持压强不变,充入氦气,平衡不移动 |
您最近一年使用:0次



