名校
1 . 现有一份“将二氧化硫转化为硫酸铵”的资料,摘录如下:
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是___________ ,简述不采用2∶1的理由是___________ 。
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合___________ 。
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵___________ 吨,消耗氨气___________ 吨。
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵
您最近一年使用:0次
2 . 25℃时,50mL0.10mol·L-1醋酸中存在下述平衡:CH3COOH⇌CH3COO-+H+,请回答以下问题:
(1)加入少量冰醋酸,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”);
(2)加入一定量蒸馏水,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”),c(OH-)将___________ (填“增大”“减小”或“不变”);
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”)。
(1)加入少量冰醋酸,平衡将
(2)加入一定量蒸馏水,平衡将
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将
您最近一年使用:0次
名校
3 . 把7 molA气体和5 molB气体混合放入2 L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K=
2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K= ,经5min达到平衡,此时生成2 mol C,求:
,经5min达到平衡,此时生成2 mol C,求:
(1)此反应的平衡常数的表达式___________ ,增大A的浓度,K值___________ (填“增大”“减小”或不变,下同),A的转化率______
(2)压缩容器的容积增大压强,平衡___________ 移动(填“向左”“向右”或“不”)。B的浓度___________ (填“增大”“减小”或不变)
(3)若在相同温度下,测得某个时刻2 L密闭容器中有2molA、4molB、4molC和4molD,则此时该反应
___________  (填“>”“=”或“<”)
(填“>”“=”或“<”)
(4)平衡时D的浓度为___________ ,平衡时压强与初始时压强之比___________
 2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K=
2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K= ,经5min达到平衡,此时生成2 mol C,求:
,经5min达到平衡,此时生成2 mol C,求:(1)此反应的平衡常数的表达式
(2)压缩容器的容积增大压强,平衡
(3)若在相同温度下,测得某个时刻2 L密闭容器中有2molA、4molB、4molC和4molD,则此时该反应

 (填“>”“=”或“<”)
(填“>”“=”或“<”)(4)平衡时D的浓度为
您最近一年使用:0次
4 . 化学是一门以实验为基础的学科。回答下列问题:
I.碘的溶解性
(1)在碘水溶液中加入1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成___________ 色的碘的四氯化碳溶液。再向试管里加入1mL浓碘化钾水溶液,振荡试管,溶液颜色变浅,用离子方程式解释溶液颜色变浅的原因:___________ ,碘在四氯化碳中比在纯水中的溶解性好,试从分子结构角度解释其原因:___________ 。
Ⅱ. 晶体制备
晶体制备
(2)向盛有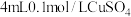 溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为
溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为___________ 。再向试管中加入极性较___________ 的试剂乙醇(填“大”或“小”),并用玻璃棒摩擦试管壁,可以观察到有___________ 色的Cu(NH3)4SO4·H2O晶体析出。
Ⅲ.乙酸乙酯的制备
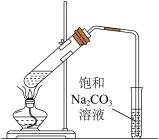
(3)利用下图装置制备乙酸乙酯,乙醇、乙酸、浓硫酸三种试剂的加入顺序为___________ ,反应的化学方程式为___________ 。
I.碘的溶解性
(1)在碘水溶液中加入1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成
Ⅱ.
 晶体制备
晶体制备(2)向盛有
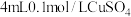 溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为
溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为Ⅲ.乙酸乙酯的制备
(3)利用下图装置制备乙酸乙酯,乙醇、乙酸、浓硫酸三种试剂的加入顺序为

您最近一年使用:0次
5 . 向pH≈10的含硫废水中加入适量 溶液,产生黑色沉淀且溶液的pH降低。
溶液,产生黑色沉淀且溶液的pH降低。 、
、 、
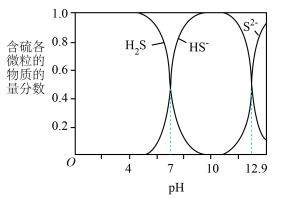
、 在水溶液中的物质的量含物分数随pH的分布曲线如图
在水溶液中的物质的量含物分数随pH的分布曲线如图
(1) 水溶液中存在电离平衡
水溶液中存在电离平衡 和
和 。下列关于
。下列关于 溶液的说法正确的是___________。
溶液的说法正确的是___________。
(2)pH≈10时,溶液中硫元素的主要存在形态为___________ 。
(3)用化学平衡移动原理解释向pH≈10的含硫废水中加入 溶液后pH降低的原因:
溶液后pH降低的原因:___________ 。
 溶液,产生黑色沉淀且溶液的pH降低。
溶液,产生黑色沉淀且溶液的pH降低。 、
、 、
、 在水溶液中的物质的量含物分数随pH的分布曲线如图
在水溶液中的物质的量含物分数随pH的分布曲线如图
(1)
 水溶液中存在电离平衡
水溶液中存在电离平衡 和
和 。下列关于
。下列关于 溶液的说法正确的是___________。
溶液的说法正确的是___________。| A.滴加新制氯水,平衡向左移动,溶液pH减小 |
| B.加水,平衡向右移动,溶液中氢离子浓度增大 |
C.通入过量 气体,平衡向左移动,溶液pH增大 气体,平衡向左移动,溶液pH增大 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小 |
(3)用化学平衡移动原理解释向pH≈10的含硫废水中加入
 溶液后pH降低的原因:
溶液后pH降低的原因:
您最近一年使用:0次
名校
6 . 从平衡移动的角度解释实验室用饱和食盐水收集Cl2的原因___________ 。
您最近一年使用:0次
7 . CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。CO进入血液后有如下平衡: 。
。
(1)C、N、O三种元素,第一电离能由大到小的顺序为___________ 。
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是___________ 。
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:___________ 。
 。
。(1)C、N、O三种元素,第一电离能由大到小的顺序为
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:
您最近一年使用:0次
22-23高一下·上海·期末
8 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近一年使用:0次
23-24高二上·浙江·期末
解题方法
9 . 为验证反应Fe3++Ag=Fe2++Ag+,利甩如图电池装置进行实验。
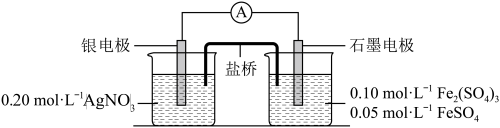
(1)由Fe2(SO4)3固体配制500 mL0.1 mol/LFe2(SO4)3溶液。在烧杯中溶解固体时,先加入一定体积的_______ 稀溶液,搅拌后再加入一定体积的水。
(2)电流表显示电流由银电极流向石墨电极。可知, 盐桥中的阳离子进入_______ 电极溶液中。
(3)根据(2)实验结果,可知石墨电极的电极反应式为_______ ,银电极的电极反应式为_______ 。因此,Fe3+氧化性小于_______ 。
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为KNO3,反应一段时间后,可以观察到电流表指针反转,原因是_______ 。

(1)由Fe2(SO4)3固体配制500 mL0.1 mol/LFe2(SO4)3溶液。在烧杯中溶解固体时,先加入一定体积的
(2)电流表显示电流由银电极流向石墨电极。可知, 盐桥中的阳离子进入
(3)根据(2)实验结果,可知石墨电极的电极反应式为
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为KNO3,反应一段时间后,可以观察到电流表指针反转,原因是
您最近一年使用:0次
名校
10 . 现有反应mA(g)+nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)m+n_______ (填“>”“<”或“=”)p。
(2)减压时,A的质量分数_______ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则B的转化率_______ 。
(4)若升高温度,则平衡时,B、C的浓度之比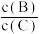 将
将_______ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_______ 。
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数_______ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色_______ (填“变浅”“变深”或“不变”)。
(1)m+n
(2)减压时,A的质量分数
(3)若加入B(体积不变),则B的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
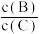 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数
您最近一年使用:0次



