21-22高二下·宁夏银川·阶段练习
名校
1 . 往 溶液中滴加少量
溶液中滴加少量 溶液,溶液呈红色,发生如下反应:
溶液,溶液呈红色,发生如下反应: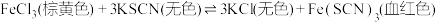 ,下列说法中正确的是
,下列说法中正确的是
 溶液中滴加少量
溶液中滴加少量 溶液,溶液呈红色,发生如下反应:
溶液,溶液呈红色,发生如下反应: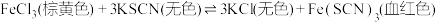 ,下列说法中正确的是
,下列说法中正确的是A.往上述溶液中滴入 溶液,溶液红色变浅 溶液,溶液红色变浅 |
B.往上述溶液中滴入 溶液,溶液红色变浅 溶液,溶液红色变浅 |
| C.往上述溶液中加入铁粉,溶液红色加深 |
D.往上述溶液中滴入 溶液,溶液红色不变 溶液,溶液红色不变 |
您最近半年使用:0次
2023-08-09更新
|
238次组卷
|
4卷引用:6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题浙江省台州市台州八校联盟2022-2023学年高二上学期11月期中联考化学试题天津市北辰区2023-2024学年高二上学期期中考试化学试题
2022·全国·模拟预测
解题方法
2 . 已知,25℃时K2Cr2O7溶液中存在以下平衡:
①Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15
②Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2
③HCrO (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K3
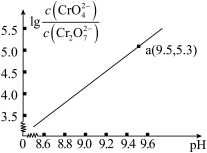
25℃时,0.1mol/LK2Cr2O7溶液中,lg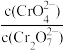 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
①Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15②Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2③HCrO
 (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K325℃时,0.1mol/LK2Cr2O7溶液中,lg
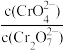 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
A.0.1mol/LK2Cr2O7溶液中,加入少量的HI气体,c(CrO )增大 )增大 |
| B.溶液颜色不再变化,可以判断该体系达到平衡 |
C.a点溶液中离子浓度关系:c(K+)>c(CrO )>c(Cr2O )>c(Cr2O )>c(H+) )>c(H+) |
D.反应③的化学平衡常数K3=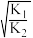 |
您最近半年使用:0次
22-23高三下·重庆渝中·阶段练习
名校
3 . 25℃时,向恒容容器中加入A发生反应:① ;②
;② 。反应体系中
。反应体系中 、
、 、
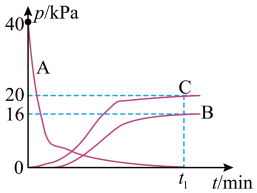
、 的分压随时间t的变化曲线如图所示。下列说法正确的是
的分压随时间t的变化曲线如图所示。下列说法正确的是
 ;②
;② 。反应体系中
。反应体系中 、
、 、
、 的分压随时间t的变化曲线如图所示。下列说法正确的是
的分压随时间t的变化曲线如图所示。下列说法正确的是
A.曲线C表示 的分压随时间的变化曲线 的分压随时间的变化曲线 |
B.25℃时,反应②的分压平衡常数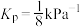 |
C.当 、 、 的分压相等时,反应②中的 的分压相等时,反应②中的 转化率为12.5% 转化率为12.5% |
D.时间 后,保持温度和体积不变,再充入 后,保持温度和体积不变,再充入 (g),则 (g),则 (g)的分压增大 (g)的分压增大 |
您最近半年使用:0次
2023-02-18更新
|
491次组卷
|
4卷引用:2022年重庆高考真题化学试题变式题(选择题11-14)
(已下线)2022年重庆高考真题化学试题变式题(选择题11-14)(已下线)素养卷04 化学反应速率与平衡图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)重庆市巴蜀中学校2023届高三下学期高考适应性月考卷(六)化学试题重庆市育才中学校2023-2024学年高二上学期三校联考模拟考化学试题(平行班)
2021高三·浙江·专题练习
解题方法
4 . 向平衡体系 中加入适量
中加入适量 固体,平衡逆向移动,溶液的颜色变浅。( )
固体,平衡逆向移动,溶液的颜色变浅。( )
 中加入适量
中加入适量 固体,平衡逆向移动,溶液的颜色变浅。( )
固体,平衡逆向移动,溶液的颜色变浅。( )
您最近半年使用:0次
2023-02-11更新
|
317次组卷
|
5卷引用:考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第七章 化学反应速率与化学平衡 第43讲 化学平衡移动原理及应用(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
22-23高三下·重庆沙坪坝·阶段练习
名校
解题方法
5 . 尽管计算机模拟实验已经有相当广泛的应用,但化学仍然是一门以实际操作并进行相应探究的学科。下列实验操作、现象与相应结论或解释相对应的一组是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在葡萄糖溶液中滴入少量酸性 溶液 溶液 |  溶液褪色 溶液褪色 | 醛基具有还原性 |
| B | 在 平衡体系中保持恒温恒容条件继续充入一定量 平衡体系中保持恒温恒容条件继续充入一定量 | 体系颜色变浅 | 反应物浓度增大,平衡向正向移动 |
| C | 在 气体氛围中点燃金属钠 气体氛围中点燃金属钠 | 产生浓烟并有黑色颗粒生成 | 单质还原性: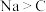 |
| D | 取适量 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值 | 加热后pH值变小 |  的水解为吸热过程 的水解为吸热过程 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
22-23高二上·天津南开·期末
名校
6 . 反应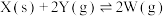
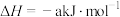 (a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
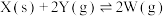
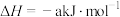 (a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是
(a>0),一定温度下,在恒容的密闭容器中,加入1molX和2molY发生反应,下列说法正确的是| A.充分反应后,放出的热量为akJ |
| B.当Y与W的物质的量浓度之比为1∶1时,表明该反应一定已达到平衡状态 |
| C.当容器内气体的压强不再改变时,表明该反应一定已达到平衡 |
| D.当达到平衡状态时,向容器中加入X,平衡不移动 |
您最近半年使用:0次
2023-01-10更新
|
315次组卷
|
4卷引用:河北省部分学校2022-2023学年高三上学期期末考试变式汇编(1-9)
(已下线)河北省部分学校2022-2023学年高三上学期期末考试变式汇编(1-9)天津大学附属中学2022-2023学年高二上学期期末考试化学试题陕西省宝鸡市渭滨区2022-2023学年高一下学期期末检测化学试题(已下线)专项02 化学反应速率与化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)
22-23高二上·山西·期末
名校
解题方法
7 . 硫酸锌是一种重要的工业原料,ZnSO4∙H2O可用于制造印染用的媒染剂,木材及皮革保存剂等。以炼锌厂锌渣为原料,含ZnO、FeO、CuO、CdO等,生产ZnSO4∙H2O的流程如下:
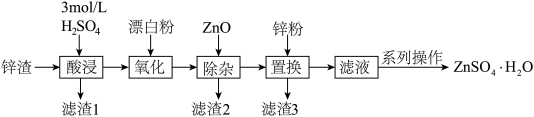
已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
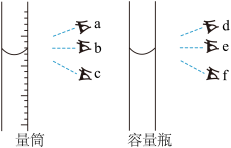
(1)“酸浸”时,需不断通入高温水蒸气,其目的是___________ (填字母)。用18 mol∙L-1的浓硫酸配制3 mol∙L-1H2SO4溶液,下列操作会使所配溶液浓度偏小的是___________ (填字母)。
(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:___________ 。除杂过程中,若控制pH=4,溶液中c(Fe3+)=___________ mol∙L-1。结合实际生产情况一般取pH4.5~5.0,pH不宜过大的原因是___________ 。
(3)滤渣3含有Zn和___________ (写化学式)。
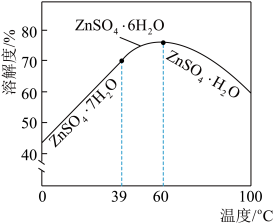
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:___________ ,洗涤、干燥。

已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
(1)“酸浸”时,需不断通入高温水蒸气,其目的是

(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:
(3)滤渣3含有Zn和
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:

您最近半年使用:0次
2023-01-08更新
|
285次组卷
|
3卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(21-24)
(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(21-24)山西省名校联考2022-2023学年高二上学期期末考试化学试题福建省宁德市2022-2023学年高二上学期期末居家检测化学试题
22-23高三·重庆沙坪坝·阶段练习
名校
8 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 探究聚氯乙烯的反应 | 加热试管中的聚氯乙烯薄膜碎片试管口湿润的蓝色石蕊试纸变红 | 氯乙烯加聚是可逆反应 |
| B | 证明卤素性质强弱 | 向淀粉碘化钾溶液通入足量Cl2、溶液先变蓝后褪色 | 不能证明Cl2氧化性比I2强 |
| C | 探究氢离子浓度对CrO 、Cr2O 、Cr2O 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中缓慢滴加氢氧化钠溶液,黄色变为橙红色 | 减小氢离子浓度,转化平衡向生成Cr2O 的方向移动 的方向移动 |
| D | 检验浓硫酸的性质 | 将浓硫酸与蔗糖混合搅拌,并用湿润的品红试纸检验产生的气体,蔗糖变黑,品红试纸褪色 | 浓硫酸具有脱水性和氧化性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
22-23高三上·北京大兴·期末
解题方法
9 . 某实验小组同学做电解CuCl2溶液实验,发现电解后 (电极未从溶液中取出)阴极上析出的铜会消失。为探究铜“消失”的原因,该小组同学用不同电解质溶液(足量)、在相同时间内进行如下实验。
已知:① ②
② (无色)③
(无色)③ ;黄色
;黄色
下列分析不正确 的是
| 装置 |
| |
| 序号 | 电解质溶液 | 实验现象(电解后) |
| I |  溶液 溶液 | 溶液仍呈蓝色,附着的铜层无明显变化 |
| II | 稀 溶液 溶液 | 溶液由蓝色开始变为浅黄绿色,2min后溶液变浑浊 |
| III | 浓 溶液 溶液 | 溶液由绿色逐渐变为深黄绿色(略黑),附着的铜层变薄 |
 ②
② (无色)③
(无色)③ ;黄色
;黄色下列分析
A.电解后 溶液的 溶液的 减小,原因是 减小,原因是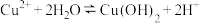 |
B.浓 溶液呈绿色原因是 溶液呈绿色原因是 增大, 增大,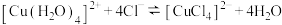 平衡正向移动 平衡正向移动 |
C.II中溶液变浑浊,推测难溶物为 |
D.III中溶液变为深黄绿色,推测原因是 ,溶液中 ,溶液中 增大 增大 |
您最近半年使用:0次
2022·浙江·模拟预测
解题方法
10 . 在一定条件下, 与甲醛发生如下反应:
与甲醛发生如下反应:
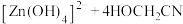
已知:i、HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ii、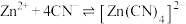
 ;
;

下列说法不正确的是
 与甲醛发生如下反应:
与甲醛发生如下反应:
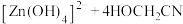
已知:i、HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ii、
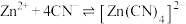
 ;
;

下列说法不正确的是
A. 与 与 中 中 均形成4个配位键 均形成4个配位键 |
B. 中键角 中键角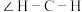 小于 小于 |
C.依据 与甲醛反应可以生成 与甲醛反应可以生成 ,可推测: ,可推测: |
| D.上述反应必须在碱性条件下进行,既保证安全性,也能提高反应物转化率 |
您最近半年使用:0次




