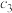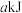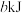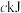1 . 向相同容积的甲、乙两容器中分别充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)=2SO3(g) △H<0。若甲容器保持恒温恒容,乙容器保持恒温恒压,分别达到平衡。乙容器中平衡时生成SO3为1.6 mol,同时放出热量Q kJ。下列说法正确的是
| A.平衡时,反应放出的热量:甲>乙 |
| B.平衡时,O2的质量:甲<乙 |
| C.乙容器若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO2)大于2.4 mol |
| D.平衡时,向乙容器中再通入一定量的SO3气体,重新达到平衡时,SO2的百分含量升高 |
您最近一年使用:0次
名校
2 . 甲、乙两容器都发生反应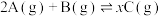 ,两容器温度和初始压强都相同。甲容器中充入2molA和1molB,达平衡后,C在平衡混合气中的体积分数为φ、物质的量为
,两容器温度和初始压强都相同。甲容器中充入2molA和1molB,达平衡后,C在平衡混合气中的体积分数为φ、物质的量为 ;乙容器中充入1.4molA、0.7molB和0.6molC,达平衡后C在平衡混合气中的体积分数为φ、物质的量为
;乙容器中充入1.4molA、0.7molB和0.6molC,达平衡后C在平衡混合气中的体积分数为φ、物质的量为 。下列说法中正确的是
。下列说法中正确的是
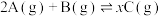 ,两容器温度和初始压强都相同。甲容器中充入2molA和1molB,达平衡后,C在平衡混合气中的体积分数为φ、物质的量为
,两容器温度和初始压强都相同。甲容器中充入2molA和1molB,达平衡后,C在平衡混合气中的体积分数为φ、物质的量为 ;乙容器中充入1.4molA、0.7molB和0.6molC,达平衡后C在平衡混合气中的体积分数为φ、物质的量为
;乙容器中充入1.4molA、0.7molB和0.6molC,达平衡后C在平衡混合气中的体积分数为φ、物质的量为 。下列说法中正确的是
。下列说法中正确的是| A.若甲、乙两容器均为恒容容器,则x一定等于2 |
| B.若甲、乙两容器均为恒压容器,则x一定等于3 |
C.若甲为恒容容器、乙为恒压容器,且 ,则 ,则 一定大于 一定大于 |
D.若甲为恒压容器、乙为恒容容器,且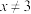 ,则 ,则 一定小于 一定小于 |
您最近一年使用:0次
名校
解题方法
3 . 氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)碘蒸气的存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: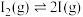 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: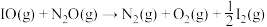 (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程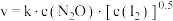 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________
(2)对反应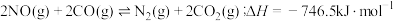 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
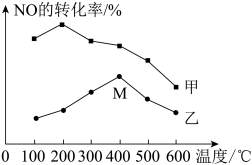
图中M点对应的速率(对应温度 )
)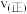
___________ 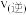 (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是___________ 。
(3)在密闭容器中充入 和
和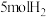 ,发生反应:
,发生反应: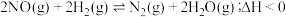 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。

①下列物理量中,图中d点大于b点的是___________ (填字母)。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为___________ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的___________ 点。
(4) 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、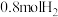 ,发生反应:
,发生反应: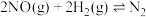
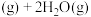 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示:
①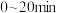 内该反应的平均反应速率
内该反应的平均反应速率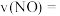
___________  。
。
②该温度下反应的平衡常数
___________  (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(1)碘蒸气的存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
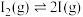 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
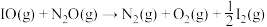 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程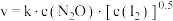 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
C. 为反应的催化剂 为反应的催化剂 |
D. 分解反应的速率与是否含碘蒸气有关 分解反应的速率与是否含碘蒸气有关 |
(2)对反应
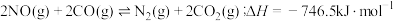 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
图中M点对应的速率(对应温度
 )
)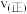
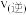 (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是(3)在密闭容器中充入
 和
和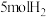 ,发生反应:
,发生反应: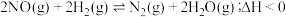 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中d点大于b点的是
A.正反应速率 B.逆反应速率
C.
 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的
(4)
 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、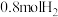 ,发生反应:
,发生反应: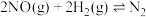
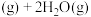 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示: | 0 | 10 | 20 | 30 | 40 |
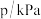 | 240 | 226 | 216 | 210 | 210 |
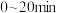 内该反应的平均反应速率
内该反应的平均反应速率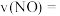
 。
。②该温度下反应的平衡常数

 (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
您最近一年使用:0次
2023-12-18更新
|
166次组卷
|
2卷引用:广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题
4 . 一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
 Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是| A.达到平衡时X浓度为0.03mol/L |
| B.将容器体积变为20L,Z的平衡浓度变为0.015mol/L |
| C.若升高温度,X的体积分数增大,则该反应的△H<0 |
| D.若增大压强,平衡向正反应方向移动,平衡常数变大 |
您最近一年使用:0次
名校
5 . 在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
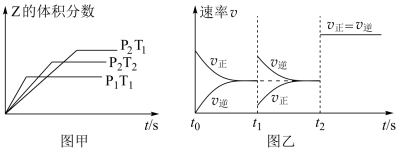
 aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
| A.图甲,p1>p2 |
| B.图甲,T1<T2,Q>0 |
| C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 |
| D.图乙,t2时表示压缩反应容器 |
您最近一年使用:0次
2023-11-29更新
|
311次组卷
|
2卷引用:江苏省苏州市苏州大学附属中学2023-2024学年高二上学期10月月考化学试题
名校
6 . 下列说法正确的是
A. 其他条件不变,增大反应容器体积,正逆反应速率不变 其他条件不变,增大反应容器体积,正逆反应速率不变 |
B. ,碳的质量不再改变说明反应已达平衡 ,碳的质量不再改变说明反应已达平衡 |
C.若平均相对分子质量不再随时间变化能说明反应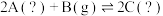 已达平衡,则A、C不能同时是气体 已达平衡,则A、C不能同时是气体 |
D.4mol 分解为 分解为 和 和 的转化率为10%时,吸收热量 的转化率为10%时,吸收热量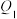 ;在相同温度和压强下,当2mol ;在相同温度和压强下,当2mol 和6mol 和6mol 反应达到平衡时 反应达到平衡时 转化率为10%,放出热量 转化率为10%,放出热量 , , 不等于 不等于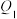 |
您最近一年使用:0次
2023-11-23更新
|
148次组卷
|
2卷引用:北京师范大学附属中学2022-2023学年高二上学期10月月考化学试题
名校
解题方法
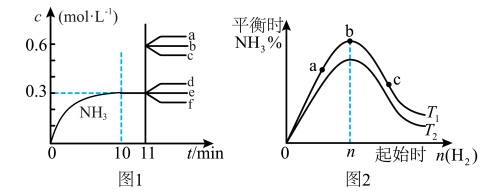
7 . 合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
| A.图1中,10min末H2的消耗速率v(H2)=0.045mol/(L·min) |
| B.图1中,其他条件不变,第11min迅速压缩容器体积为1L,则c(NH3)-t曲线变化为a |
| C.图2中,反应物N2的平衡转化率:b>a>c |
| D.图2中,T1、T2表示温度,则T1>T2 |
您最近一年使用:0次
2023-11-12更新
|
309次组卷
|
4卷引用:河南省南阳市第一中学校2023-2024学年高二上学期第三次月考化学试题
名校
解题方法
8 . 工业上通过将CO、CO2与氢气反应,实现碳中和。
(1)已知反应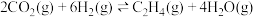
 ,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
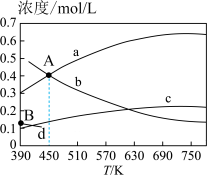
①该反应的平衡常数表达式为___________ 。
②图中曲线b、c分别表示的是平衡时___________ 和___________ 的浓度变化。
③已知坐标A(450,0.4),B(390,0.13),求450K时该反应的K=___________ 。(列出带数值的计算表达式即可,不需要算最终结果)
(2)用CO和H2合成CH3OH的反应为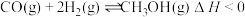 ,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
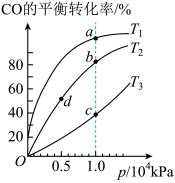
①图中T1、T2、T3的大小关系为___________ 。
②图中b、c点逆反应速率的大小关系为___________ 。
③图中b、c、d点平衡常数的大小关系为___________ 。
④若忽略坐标上的数值,横坐标表示温度,T1、T2、T3分别用P1、P2、P3替换,则纵坐标可以表示___________ ,P1、P2、P3的大小关系为___________ 。
(1)已知反应
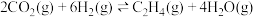
 ,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
①该反应的平衡常数表达式为
②图中曲线b、c分别表示的是平衡时
③已知坐标A(450,0.4),B(390,0.13),求450K时该反应的K=
(2)用CO和H2合成CH3OH的反应为
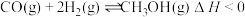 ,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
①图中T1、T2、T3的大小关系为
②图中b、c点逆反应速率的大小关系为
③图中b、c、d点平衡常数的大小关系为
④若忽略坐标上的数值,横坐标表示温度,T1、T2、T3分别用P1、P2、P3替换,则纵坐标可以表示
您最近一年使用:0次
名校
9 . 向两个不同容器中分别通入 和
和 ,发生反应:在压强为
,发生反应:在压强为 和
和 下分别达到平衡,平衡时
下分别达到平衡,平衡时 和
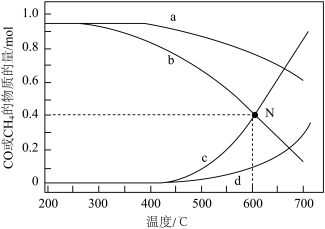
和 的物质的量在不同温度下的变化如图所示,下列说法正确的是
的物质的量在不同温度下的变化如图所示,下列说法正确的是
Ⅰ.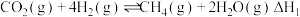
Ⅱ.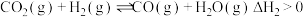
 和
和 ,发生反应:在压强为
,发生反应:在压强为 和
和 下分别达到平衡,平衡时
下分别达到平衡,平衡时 和
和 的物质的量在不同温度下的变化如图所示,下列说法正确的是
的物质的量在不同温度下的变化如图所示,下列说法正确的是
Ⅰ.
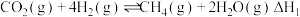
Ⅱ.
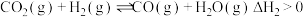
A.曲线c表示 时 时 的物质的量 的物质的量 |
B.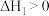 |
| C.在N点条件下,反应Ⅱ的平衡常数为2.4 |
D.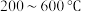 ,随着温度升高 ,随着温度升高 的体积分数增大 的体积分数增大 |
您最近一年使用:0次
名校
10 . 温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容条件,已知
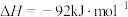 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:
下列说法正确的是

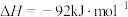 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:容器1 | 容器2 | 容器3 | |
| 反应物投入量 |
|
|
|
|
|
|
|
反应的能量变化 | 放出 | 吸收 | 吸收 |
体系的压强 |
|
|
|
反应物的转化率 |
|
|
|
A.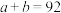 | B. | C. | D.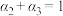 |
您最近一年使用:0次
2023-10-15更新
|
500次组卷
|
2卷引用:北京大学附属中学2023-2024学年高二上学期10月月考化学试题

 、
、