名校
解题方法
1 . 将玉米秸秆进行热化学裂解可制备出以CO、 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
(1)已知:几种常见共价键的键能如下表所示:
由此可计算反应 的焓变
的焓变
___________ kJ⋅mol 。
。
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是___________(填标号)。
(3) 和
和 合成乙醇的反应为
合成乙醇的反应为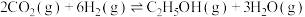 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。
___________  (填“>、<”或“=”,下同)。判断依据是
(填“>、<”或“=”,下同)。判断依据是___________ 。
②a、b两点的平衡常数
___________  。
。
③已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
___________ J⋅mol 。从图中信息获知催化效率较高的催化剂是
。从图中信息获知催化效率较高的催化剂是___________ (填“m”或“n”)。
 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。(1)已知:几种常见共价键的键能如下表所示:
| 共价键 | C-H | C-O | C≡O | H-H | O-H |
键能(kJ⋅mol ) ) | 413 | 358 | 839 | 436 | 467 |
 的焓变
的焓变
 。
。(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是___________(填标号)。
| A.体系温度不再发生变化时,反应达到化学平衡状态 |
B.体系中若 和 和 的物质的量之比达到2∶1,则反应已达到平衡 的物质的量之比达到2∶1,则反应已达到平衡 |
C.加入催化剂,可以提高 的平衡产率 的平衡产率 |
| D.其它条件不变,增大CO的浓度,能提高H2的平衡转化率 |
(3)
 和
和 合成乙醇的反应为
合成乙醇的反应为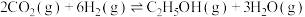 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。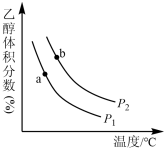

 (填“>、<”或“=”,下同)。判断依据是
(填“>、<”或“=”,下同)。判断依据是②a、b两点的平衡常数

 。
。③已知Arrhenius经验公式为
 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
 。从图中信息获知催化效率较高的催化剂是
。从图中信息获知催化效率较高的催化剂是
您最近一年使用:0次
名校
解题方法
2 . 在恒温恒压下,向密闭容器中充入4mol  和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是
 和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是A.若反应开始时容器体积为2L,则 |
B.若把条件“恒温恒压”改为“恒压恒容”,则平衡后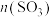 大于1.4mol 大于1.4mol |
C.2min后,向容器中再通入一定量的 气体,重新达到平衡时 气体,重新达到平衡时 的含量变小 的含量变小 |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近一年使用:0次
3 . 下列说法或表示正确的是
A. 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 |
B. 要在光照和点燃条件下才反应,所以 要在光照和点燃条件下才反应,所以 , , |
C.已知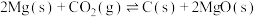 ,达平衡后,缩小容器体积, ,达平衡后,缩小容器体积, 浓度增大 浓度增大 |
D.将 的醋酸稀释为 的醋酸稀释为 的过程中, 的过程中, 减小 减小 |
您最近一年使用:0次
4 . NOx是污染大气的主要成分之一,它主要来源于汽车尾气的排放和化石燃料的燃烧。回答下列问题:
(1)已知:①2C(s)+O2(g) 2CO(g)
2CO(g)  H1=-221kJ/mol
H1=-221kJ/mol
②2NO(g) N2(g)+O2(g)
N2(g)+O2(g)  H2=-180kJ/mol
H2=-180kJ/mol
③2NO(g)+C(s) CO2(g)+N2(g)
CO2(g)+N2(g)  H3=-573kJ/mol
H3=-573kJ/mol
则2NO(g)+2CO(g) 2CO2(g)+N2(g)的反应热
2CO2(g)+N2(g)的反应热 H=
H=___________ 。
(2)燃煤烟气脱硝的反应之一为2NO2(g)+4CO(g) N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
①c值可能为___________ (填字母),其他条件不变,若不使用催化剂,则0~2min内NO2的转化率将___________ (填“变大”“变小”或“不变”)。
A.1.68 B.1.65 C.1.6 D.1.55
②维持其他条件不变,第9min时向容器中再充入1.0molNO2和1.0molN2,则v(正)___________ (填“>”或“<”)v(逆)。
(3)烟气脱硝的另一个反应为2C(s)+2NO2(g) N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。
N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。___________ ,在T℃时,用此反应脱硝适宜的压强是___________ ,1100kPa时,该反应的化学平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度,气体分压=气体总压×体积分数,结果保留两位小数)。
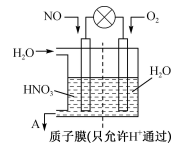
(4)利用电化学原理脱硝可获得电能,其工作原理如图所示:___________ 。
(1)已知:①2C(s)+O2(g)
 2CO(g)
2CO(g)  H1=-221kJ/mol
H1=-221kJ/mol②2NO(g)
 N2(g)+O2(g)
N2(g)+O2(g)  H2=-180kJ/mol
H2=-180kJ/mol③2NO(g)+C(s)
 CO2(g)+N2(g)
CO2(g)+N2(g)  H3=-573kJ/mol
H3=-573kJ/mol则2NO(g)+2CO(g)
 2CO2(g)+N2(g)的反应热
2CO2(g)+N2(g)的反应热 H=
H=(2)燃煤烟气脱硝的反应之一为2NO2(g)+4CO(g)
 N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
N2(g)+4CO2(g),在一定温度下,向1L恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:| 时间 | 0min | 2min | 4min | 6min | 8min | 10min |
| c(NO2)/mol·L-1 | 2.00 | 1.80 | c | 1.55 | 1.50 | 1.50 |
A.1.68 B.1.65 C.1.6 D.1.55
②维持其他条件不变,第9min时向容器中再充入1.0molNO2和1.0molN2,则v(正)
(3)烟气脱硝的另一个反应为2C(s)+2NO2(g)
 N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。
N2(g)+2CO2(g)。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强下,相同时间内NO2的转化率与压强的关系如图所示。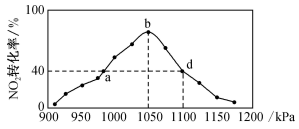
(4)利用电化学原理脱硝可获得电能,其工作原理如图所示:
您最近一年使用:0次
名校
5 . 恒温恒容,可逆反应N2O4(g) 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是| A.NO2的体积分数增大 | B.达新平衡后平衡体系压强比原平衡大 |
| C.平衡正向移动 | D.达新平衡后N2O4转化率降低 |
您最近一年使用:0次
名校
6 . 下列有关对应图像的说法正确的是

A.据①知,某温度下,平衡状态由A变到B时,平衡常数 |
B.据平衡常数的负对数(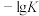 )—温度(T)图像②知,30℃时,B点对应状态的 )—温度(T)图像②知,30℃时,B点对应状态的 |
C.由 的稳定性与溶液pH的关系可知图③中 的稳定性与溶液pH的关系可知图③中 |
D.图④所示体系中气体平均摩尔质量: , , |
您最近一年使用:0次
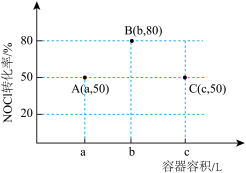
7 . 一定温度下,向三个容积不等的恒容密闭容器中分别投入2molNOCl,发生反应: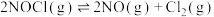 。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
| A.A点加入适当催化剂,可以提高NOCl的转化率 |
| B.容积为aL的容器达到平衡后再投入1molNOCl、1molNO,平衡向左移动 |
| C.A、B两点的压强之比为25:28 |
| D.容积为cL的容器NOCl的平衡转化率大于80% |
您最近一年使用:0次
名校
8 . 以下说法中操作正确、能达到目的且判断正确的是
选项 | 操作 | 目的 | 判断 |
A | 向 | 使 | 错误,根据反应 |
B | 合成氨时在经济性良好的范围内选择尽可能高的压强 | 增加 转化率 转化率 | 正确,压强增大使得反应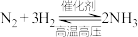 向右进行 向右进行 |
C | 向两支盛有2ml0.2mol/L的乙二酸试管中滴加1ml浓度分别为0.1mol/L和0.2mol/L的 溶液 溶液 | 探究反应物浓度对反应速率的影响 | 正确,浓度越大反应速率越快, 褪色越快 褪色越快 |
D | 向滴有KSCN溶液的 溶液中加入 溶液中加入 固体 固体 | 探究浓度对平衡的影响 | 正确,增加 浓度,使 浓度,使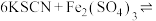 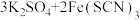 平衡移动 平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应:A(g)+B(g) xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是

 xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
| A.x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是增大反应物的浓度或降温 |
| D.t1~t2、t2~t3平衡常数相等,且K=4 |
您最近一年使用:0次
名校
10 . 可逆反应aA(g)+bB(s)⇌cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
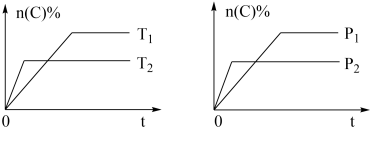

| A.升高温度,平衡向逆反应方向移动 |
| B.使用催化剂,C的物质的量分数增加 |
| C.化学方程式系数a>c+d |
| D.达到平衡后,P1条件V逆反应速率大于P2条件下V正反应速率 |
您最近一年使用:0次

 和生石灰混合体系加压
和生石灰混合体系加压 的K的表达式可知,压强增大不能使
的K的表达式可知,压强增大不能使

