名校
1 . 工业合成氨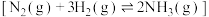 是人类科学技术的一项重大突破。各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。下列说法正确的个数为
是人类科学技术的一项重大突破。各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。下列说法正确的个数为 的
的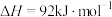
②可选择不同的催化剂来改变合成氨反应的焓变
③升高温度,正反应速率增大,逆反应速率减小
④恒温恒容的条件下进行合成氨反应,混合气体密度保持不变时,则说明反应达到平衡
⑤恒温恒容的条件下进行合成氨反应,体系压强不再变化时,则说明反应达到平衡
⑥综合考虑反应条件的成本和实际的可能性,工业合成氨采用的压强不能太大
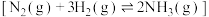 是人类科学技术的一项重大突破。各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。下列说法正确的个数为
是人类科学技术的一项重大突破。各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。下列说法正确的个数为
 的
的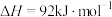
②可选择不同的催化剂来改变合成氨反应的焓变
③升高温度,正反应速率增大,逆反应速率减小
④恒温恒容的条件下进行合成氨反应,混合气体密度保持不变时,则说明反应达到平衡
⑤恒温恒容的条件下进行合成氨反应,体系压强不再变化时,则说明反应达到平衡
⑥综合考虑反应条件的成本和实际的可能性,工业合成氨采用的压强不能太大
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
名校
2 . 回答下列问题。
I.我国提出争取在2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。“碳中和”是指CO2的排放总量和减少总量相当。工业上有一种方法是利用CO2生产甲醇(CH3OH):CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:_______ (填“放热”或“吸热”)反应,若有1molCO2(g)参加反应,则变化的能量是_______ kJ。
(2)一定条件下,将2molCO2和6molH2在2L恒容密闭容器中发生上述反应,经过2min反应达到了平衡,此时CH3OH浓度为0.8mol/L。
①2min内用CO2表示该反应的速率为v(CO2)=_______ 。
②达到平衡时氢气的转化率为_______ ,平衡时体系内气体压强与开始时的压强之比为_______ 。
(3)一定能说明该反应达到平衡的标志是_______ 。
A.v正(CO2)=3v逆(H2)
B.单位时间内3molH-H键断裂,同时形成2molO-H键
C.CO2和CH3OH物质的量浓度的比值不变
D.混合气体的平均摩尔质量不再改变
E.混合气体的密度保持不变
(4)如表列出了在不同温度和压强下,反应达到平衡时CO2的转化率,从化学反应速率、化学平衡及生产成本、产量等角度综合分析,在实际生产中有关该反应适宜条件选择的说法正确的是_______ 。
A.CO2的转化率与温度成反比,故采用尽可能低的温度
B.该反应在450℃左右、0.1Mpa(常压)下进行较为合适
C.CO2的转化率与压强成正比,故采用尽可能高的压强
Ⅱ.有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。_______ (填“增大”或“减小”)
(6)a电极上的电极反应式是_______ ,当a电极极消耗1mol氮气,则b电极消耗氢气体积(标况下)为_______ 。
I.我国提出争取在2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。“碳中和”是指CO2的排放总量和减少总量相当。工业上有一种方法是利用CO2生产甲醇(CH3OH):CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
(2)一定条件下,将2molCO2和6molH2在2L恒容密闭容器中发生上述反应,经过2min反应达到了平衡,此时CH3OH浓度为0.8mol/L。
①2min内用CO2表示该反应的速率为v(CO2)=
②达到平衡时氢气的转化率为
(3)一定能说明该反应达到平衡的标志是
A.v正(CO2)=3v逆(H2)
B.单位时间内3molH-H键断裂,同时形成2molO-H键
C.CO2和CH3OH物质的量浓度的比值不变
D.混合气体的平均摩尔质量不再改变
E.混合气体的密度保持不变
(4)如表列出了在不同温度和压强下,反应达到平衡时CO2的转化率,从化学反应速率、化学平衡及生产成本、产量等角度综合分析,在实际生产中有关该反应适宜条件选择的说法正确的是
| 温度/℃ | 平衡时的转化率 | ||||
| 0.1Mpa | 0.5Mpa | 1Mpa | 5Mpa | 10Mpa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
B.该反应在450℃左右、0.1Mpa(常压)下进行较为合适
C.CO2的转化率与压强成正比,故采用尽可能高的压强
Ⅱ.有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
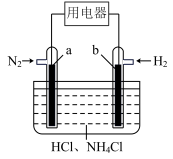
(6)a电极上的电极反应式是
您最近一年使用:0次
名校
3 .  参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
①催化剂是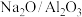 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气
 参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是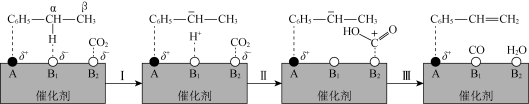
①催化剂是
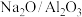 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气②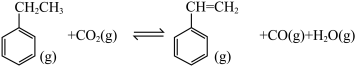

| A.反应过程中需要控制催化剂表面的酸碱性,不能太高或太低 |
B.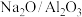 复合催化剂使 复合催化剂使 位点带较多负电荷,活化C-H发生耦合脱氢 位点带较多负电荷,活化C-H发生耦合脱氢 |
C.恒温恒容,其他条件不变时,适当提高 分压,可能使反应速率加快 分压,可能使反应速率加快 |
D.恒温恒压, 能提高乙苯的平衡转化率是降低了气体分压并消耗了 能提高乙苯的平衡转化率是降低了气体分压并消耗了 ,使平衡正向移动 ,使平衡正向移动 |
您最近一年使用:0次
名校
4 . 在CO2与H2反应制甲醇的反应体系中,主要反应的热化学方程式为
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.5 kJ·mol-1
反应Ⅱ:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
反应Ⅲ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH3=+40.9 kJ·mol-1
CO(g)+H2O(g) ΔH3=+40.9 kJ·mol-1
在恒压密闭容器中,n始(CO2)∶ n始(H2)=1∶3时,若仅考虑上述反应,平衡时CO2的转化率、CH3OH的产率随温度的变化如图所示。下列说法正确的是
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.5 kJ·mol-1反应Ⅱ:CO(g)+2H2(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2反应Ⅲ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3=+40.9 kJ·mol-1
CO(g)+H2O(g) ΔH3=+40.9 kJ·mol-1在恒压密闭容器中,n始(CO2)∶ n始(H2)=1∶3时,若仅考虑上述反应,平衡时CO2的转化率、CH3OH的产率随温度的变化如图所示。下列说法正确的是

| A.升高温度至约380℃后以反应Ⅲ为主 |
| B.一定温度下,增大n始(CO2)/n始(H2)可提高CO2的平衡转化率 |
| C.图中曲线a表示平衡时CH3OH产率随温度的变化 |
| D.一定温度下,加压或选用高效催化剂,均能提高平衡时CH3OH产率 |
您最近一年使用:0次
名校
解题方法
5 . 在密闭容器中,一定量混合气体发生反应: ,平衡时测得C的浓度为
,平衡时测得C的浓度为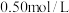 。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为
。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为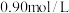 。下列有关判断不正确的是
。下列有关判断不正确的是
 ,平衡时测得C的浓度为
,平衡时测得C的浓度为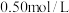 。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为
。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为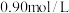 。下列有关判断不正确的是
。下列有关判断不正确的是| A.C的体积分数减小 | B.化学平衡常数减小 |
C.在建立新平衡的过程中, 逐渐减小 逐渐减小 | D.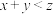 |
您最近一年使用:0次
名校
6 . 一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)  zC(g),达到平衡后测得A气体的浓度为0.5mol·L-1,当恒温下将密闭容器的容积扩大到两倍(就是减压)再达到平衡后,测得A浓度为0.3mol·L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为0.5mol·L-1,当恒温下将密闭容器的容积扩大到两倍(就是减压)再达到平衡后,测得A浓度为0.3mol·L-1,则下列叙述正确的是
 zC(g),达到平衡后测得A气体的浓度为0.5mol·L-1,当恒温下将密闭容器的容积扩大到两倍(就是减压)再达到平衡后,测得A浓度为0.3mol·L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为0.5mol·L-1,当恒温下将密闭容器的容积扩大到两倍(就是减压)再达到平衡后,测得A浓度为0.3mol·L-1,则下列叙述正确的是| A.平衡向正反应方向移动 | B.x +y<z |
| C.C的质量分数降低 | D.B的转化率降低 |
您最近一年使用:0次
名校
7 . 研究化学反应的快慢和限度对人类的生产、生活具有重要意义。在一定条件下,向体积恒为 的密闭容器中通入
的密闭容器中通入 和
和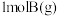 发生反应:
发生反应: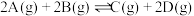 ,测得反应过程中
,测得反应过程中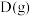 的物质的量分数随时间的变化关系如图:
的物质的量分数随时间的变化关系如图:
(1) 点的
点的
______  点的
点的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2) 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为______  。
。
(3)该反应条件下,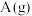 的平衡转化率约为
的平衡转化率约为______ %(保留1位小数)。
(4)测得不同压强下(其他条件不变)上述反应达平衡状态时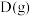 的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是
的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是______ ,为了促进更多的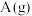 转化为生成物,可采取的措施是
转化为生成物,可采取的措施是______ 。
 的密闭容器中通入
的密闭容器中通入 和
和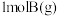 发生反应:
发生反应: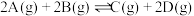 ,测得反应过程中
,测得反应过程中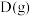 的物质的量分数随时间的变化关系如图:
的物质的量分数随时间的变化关系如图: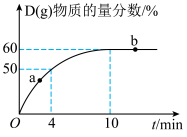
(1)
 点的
点的
 点的
点的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)
 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为 。
。(3)该反应条件下,
 的平衡转化率约为
的平衡转化率约为(4)测得不同压强下(其他条件不变)上述反应达平衡状态时
 的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是
的物质的量分数如图所示。由图可得,影响该反应限度的一个因素是 转化为生成物,可采取的措施是
转化为生成物,可采取的措施是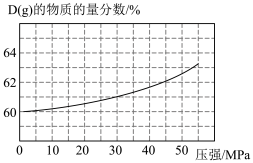
您最近一年使用:0次
名校
8 . 我国科学家实现了在铜催化剂条件下将 转化为三甲胺
转化为三甲胺 计算机模拟单个DMF分子在铜催化剂表面并发生转化的反应历程如图所示(用“*”表示吸附在催化剂表面的状态)。已知三甲胺是可燃性气体,
计算机模拟单个DMF分子在铜催化剂表面并发生转化的反应历程如图所示(用“*”表示吸附在催化剂表面的状态)。已知三甲胺是可燃性气体,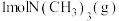 完全燃烧放出2357kJ的热量。下列说法正确的是
完全燃烧放出2357kJ的热量。下列说法正确的是
 转化为三甲胺
转化为三甲胺 计算机模拟单个DMF分子在铜催化剂表面并发生转化的反应历程如图所示(用“*”表示吸附在催化剂表面的状态)。已知三甲胺是可燃性气体,
计算机模拟单个DMF分子在铜催化剂表面并发生转化的反应历程如图所示(用“*”表示吸附在催化剂表面的状态)。已知三甲胺是可燃性气体,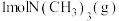 完全燃烧放出2357kJ的热量。下列说法正确的是
完全燃烧放出2357kJ的热量。下列说法正确的是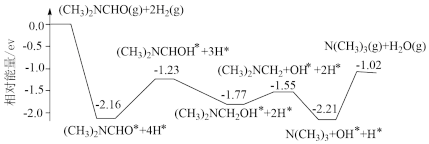
A.发生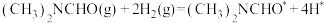 后,体系能量下降,是因为断开H-H键放出能量 后,体系能量下降,是因为断开H-H键放出能量 |
B.上述历程中能垒(活化能)最小的反应为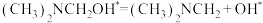 |
| C.增大压强或升高温度均能加快反应速率,并增大DMF的平衡转化率 |
D.表示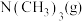 燃烧热的热化学方程式为 燃烧热的热化学方程式为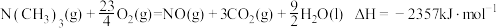 |
您最近一年使用:0次
解题方法
9 . 一定温度下,分别将两种亚硫酸氢盐加热分解,达平衡时的压强分别为 、
、 。
。
ⅰ.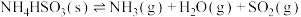
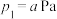
ⅱ.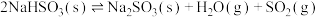
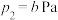
在该温度下,将一定质量的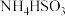 与
与 加入某密闭容器中,平衡时,三种固体均存在。下列说法
加入某密闭容器中,平衡时,三种固体均存在。下列说法不正确 的是
 、
、 。
。ⅰ.
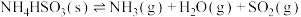
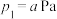
ⅱ.
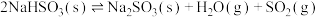
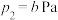
在该温度下,将一定质量的
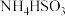 与
与 加入某密闭容器中,平衡时,三种固体均存在。下列说法
加入某密闭容器中,平衡时,三种固体均存在。下列说法A.平衡时,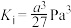 , ,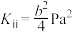 |
| B.保持恒温将容器体积压缩,再次平衡时各气体的浓度均减小 |
C.保持恒温、恒压,若再通入少量 ,再次平衡时容器内 ,再次平衡时容器内 的物质的量不变 的物质的量不变 |
D.保持恒温、恒容,若再通入少量 ,再次平衡时体系的总压强不变 ,再次平衡时体系的总压强不变 |
您最近一年使用:0次
名校
10 . 已知
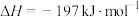 。在下列条件下发生该反应,测定平衡时数据如表所示:
。在下列条件下发生该反应,测定平衡时数据如表所示:
下列说法错误的是

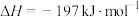 。在下列条件下发生该反应,测定平衡时数据如表所示:
。在下列条件下发生该反应,测定平衡时数据如表所示:| 实验编号 | 实验I | 实验II | 实验III |
| 起始投料 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO3 |
| 温度、压强 | T℃、200kPa恒温恒压容器 | T℃、200kPa恒温恒容容器 | T℃、400kPa恒温恒容容器 |
| 平衡时间 | t1 | t2 | t3 |
| 能量 | 放Q1 kJ | 吸Q2 kJ | 吸Q3 kJ |
| c(SO2) | c1(SO2、) | c2(SO2) | c3(SO2) |
| 转化率(α) | α1(SO2) | α2(SO3) | α3(SO3) |
A. |
B.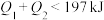 且 且 |
C.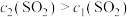 且 且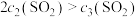 |
D.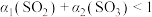 且 且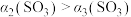 |
您最近一年使用:0次



