1 . 工业上一般采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)在一定温度下,将2 mol CO和5 mol H2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25mol·L-1。该反应的平衡常数K=_______ 。
(2)若在一体积可变的容器中充入lmolCO、2molH2和3molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的0.6倍,则该反应向_______ (填“正”、“逆”)反应方向移动。
(3)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
则下列关系正确的是_______。
 CH3OH(g)。
CH3OH(g)。(1)在一定温度下,将2 mol CO和5 mol H2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25mol·L-1。该反应的平衡常数K=
(2)若在一体积可变的容器中充入lmolCO、2molH2和3molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的0.6倍,则该反应向
(3)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容 器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度(mol/l) | 能量变化(Q1、Q2、Q3均大于0) |
| 1 | 2molCO和4molH2 | a1% | c1 | 放出Q1kJ热量 |
| 2 | 2molCH3OH | a2% | c2 | 吸收Q2kJ热量 |
| 3 | 4molCO和8molH2 | a3% | c3 | 放出Q3kJ热量 |
| A.2Q1=Q3 | B.c1=c2 | C.a1+a2=1 | D.2a1=a3 |
您最近一年使用:0次
解题方法
2 . 已知:①
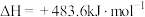
②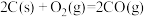
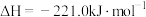
③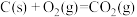

④
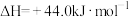
回答下列问题:
(1)上述过程属于放热反应的是_______ (填序号)。
(2)下图是反应②的能量变化图
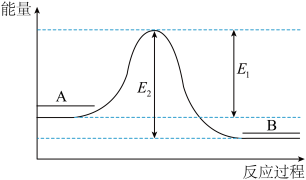
①请写出图中A、B处对应的物质、状态及其物质的量[如:
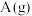 ]:
]:
A:_______ ;B:_______ 。
② 表示
表示_______ ;
③ 与
与 的差值为
的差值为_______ (填具体数字)
(3)写出 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式_______ 。
(4)其他条件不变,压缩容器体积,反应④的平衡_______ (填“正反应方向”“逆反应方向”或“不”)移动,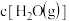
_______ (填“变大”“变小”或“不变”)。

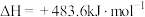
②
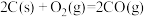
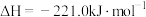
③
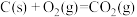

④

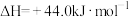
回答下列问题:
(1)上述过程属于放热反应的是
(2)下图是反应②的能量变化图

①请写出图中A、B处对应的物质、状态及其物质的量[如:

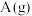 ]:
]:A:
②
 表示
表示③
 与
与 的差值为
的差值为(3)写出
 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式(4)其他条件不变,压缩容器体积,反应④的平衡
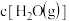
您最近一年使用:0次
解题方法
3 . 在密闭容器中进行如下反应: ,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
(1)增加C的含量,平衡____________ ,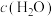
___________ .
(2)保持反应容器体积和温度不变,通入 ,平衡
,平衡____________ ,
____________ .
(3)在一定温度下,缩小反应容器体积,平衡向____________ 方向移动,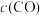
___________ , 的转化率
的转化率
______________ 。
(4)保持反应容器体积不变,升高温度,平衡向_________ 方向移动,
___________ .
(5)保持反应容器体积和温度不变,再通入 ,平衡向
,平衡向__________ 方向移动, 的转化率
的转化率
_________ ,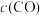
___________ 。
 ,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。(1)增加C的含量,平衡
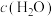
(2)保持反应容器体积和温度不变,通入
 ,平衡
,平衡
(3)在一定温度下,缩小反应容器体积,平衡向
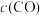
 的转化率
的转化率
(4)保持反应容器体积不变,升高温度,平衡向

(5)保持反应容器体积和温度不变,再通入
 ,平衡向
,平衡向 的转化率
的转化率
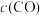
您最近一年使用:0次
4 . 完成下列填空
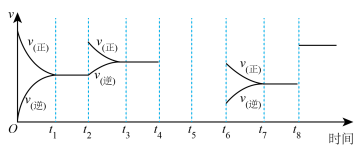
(1)下图表示反应
 的反应速率与时间的关系,回答下列问题:
的反应速率与时间的关系,回答下列问题:
①由图可知 、
、 、
、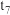 、
、 时都达到了平衡状态,
时都达到了平衡状态, 、
、 时都改变了外在条件,则
时都改变了外在条件,则 时改变的条件为
时改变的条件为_______ ;
②若在 时对该反应进行加压,在
时对该反应进行加压,在 时达到了平衡状态,请在图中画出反应速率在
时达到了平衡状态,请在图中画出反应速率在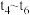 时间段的变化趋势。
时间段的变化趋势。_________
(2)某化学科研小组研究在其他条件不变时,改变某一外界条件对反应 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),回答下列问题:
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),回答下列问题:
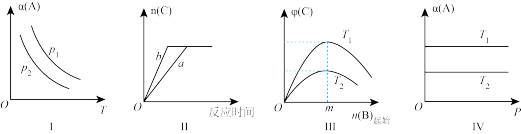
①在Ⅰ中,若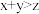 ,则
,则
_______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
②在Ⅱ中,若a→b为使用合适的催化剂,则A的转化率_______ (填“增大”“减小”或“不变”);
③在Ⅲ中,随着B的起始物质的量的增加,在m点时,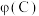 达到最大值,则m点反应物A与B的投料量比为
达到最大值,则m点反应物A与B的投料量比为_______ ;
④在Ⅳ中,若 ,则该反应的平衡常数
,则该反应的平衡常数
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)下图表示反应

 的反应速率与时间的关系,回答下列问题:
的反应速率与时间的关系,回答下列问题:
①由图可知
 、
、 、
、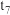 、
、 时都达到了平衡状态,
时都达到了平衡状态, 、
、 时都改变了外在条件,则
时都改变了外在条件,则 时改变的条件为
时改变的条件为②若在
 时对该反应进行加压,在
时对该反应进行加压,在 时达到了平衡状态,请在图中画出反应速率在
时达到了平衡状态,请在图中画出反应速率在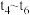 时间段的变化趋势。
时间段的变化趋势。(2)某化学科研小组研究在其他条件不变时,改变某一外界条件对反应
 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),回答下列问题:
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),回答下列问题:
①在Ⅰ中,若
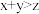 ,则
,则
 (填“>”“<”或“=”)
(填“>”“<”或“=”)②在Ⅱ中,若a→b为使用合适的催化剂,则A的转化率
③在Ⅲ中,随着B的起始物质的量的增加,在m点时,
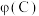 达到最大值,则m点反应物A与B的投料量比为
达到最大值,则m点反应物A与B的投料量比为④在Ⅳ中,若
 ,则该反应的平衡常数
,则该反应的平衡常数
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
5 . 在密闭容器中进行如下反应
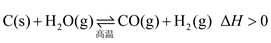
达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况:
(1)增加C的含量,平衡____________ ,c(H2O)___________ 。
(2)保持反应容器体积和温度不变,通入He,平衡____________ ,c(H2)____________ 。
(3)在一定温度下,缩小反应容器体积,平衡向____________ 方向移动,c(CO)___________ ,H2O(g)的转化率
______________ 。
(4)保持反应容器体积不变,升高温度,平衡向_________ 方向移动,c(H2)___________ 。
(5)保持反应容器体积和温度不变,再通入H2O(g),平衡向__________ 方向移动,H2O(g)的转化率
_________ ,c(CO)___________ 。
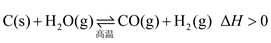
达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况:
(1)增加C的含量,平衡
(2)保持反应容器体积和温度不变,通入He,平衡
(3)在一定温度下,缩小反应容器体积,平衡向

(4)保持反应容器体积不变,升高温度,平衡向
(5)保持反应容器体积和温度不变,再通入H2O(g),平衡向

您最近一年使用:0次
2021-11-07更新
|
313次组卷
|
2卷引用:四川省成都市蓉城名校联盟2021-2022学年高二上学期期中联考化学试题
名校
6 . 一定条件下,在2L的密闭容器中充入1molA和3molB,发生如下反应:aA(g)+bB(g)⇌cC(?)+dD(g)ΔH。达到平衡后,测得A减少了0.5mol,B的物质的量浓度为0.75mol•L﹣1,C的物质的量为1mol,v(B):v(D)=3:2,请回答下列问题:
(1)a:b:c:d=_____ 。
(2)增大压强至原来的2倍,D的物质的量不发生变化,则C为_____ 态(填“固”、“液”或“气”),当增大压强至原来的10倍,D的物质的量增大,则可能的原因是_____ 。
(3)升高温度,D的物质的量浓度增大,则ΔH_____ 0.(填“>”“<”或“=”)
(4)保持体积不变,且反应体系中各物质均为气态时,若再加入10molA,则A的转化率_____ (填“增大”、“减小”或“不变”,下同),C的体积分数_____ 。保持体积不变,若再加入10molAr,则A的正反应速率_____ ,混合气体的密度_____ 。
(5)在恒容、绝热的密闭容器中,反应体系中各物质均为气态时,下列情况不能说明该反应已达到平衡状态的是_____。(填正确答案标号)
(1)a:b:c:d=
(2)增大压强至原来的2倍,D的物质的量不发生变化,则C为
(3)升高温度,D的物质的量浓度增大,则ΔH
(4)保持体积不变,且反应体系中各物质均为气态时,若再加入10molA,则A的转化率
(5)在恒容、绝热的密闭容器中,反应体系中各物质均为气态时,下列情况不能说明该反应已达到平衡状态的是_____。(填正确答案标号)
| A.平衡常数不再变化 |
| B.混合气体的平均相对分子质量不再改变 |
| C.压强不再变化 |
| D.v正(A):v逆(D)=1:2 |
您最近一年使用:0次
2021-10-28更新
|
192次组卷
|
2卷引用:四川省成都市蓉城名校联盟2020-2021学年高二上学期期中考试化学试题
解题方法
7 . 按要求填空
Ⅰ.可逆反应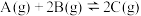
 ,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
(1)升高温度,v(正)___________ 。
(2)使用催化剂,A的物质的量___________ 。
(3)压缩容器体积,v(逆)___________ ,C占混合气体的体积分数___________ 。
(4)增大A的浓度,则B的转化率___________ 。
Ⅱ. 已知可逆反应: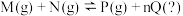 请回答下列问题:
请回答下列问题:
(5)在某温度下,反应物的起始浓度分别为: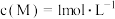 ,
,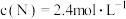 ;
; 后达到平衡,
后达到平衡, 的转化率为
的转化率为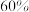 ,此时
,此时 的转化率为
的转化率为___________ ;用物质P表示的反应速率为___________ 。
(6)若其他条件不变,加热后P的质量分数减少,则正反应是___________ 热反应。
(7)若其他条件不变,增大压强时,如果平衡不发生移动,则Q是___________ 态(填“气”、“液”、“固”),n=___________ 。
Ⅰ.可逆反应
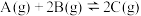
 ,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:(1)升高温度,v(正)
(2)使用催化剂,A的物质的量
(3)压缩容器体积,v(逆)
(4)增大A的浓度,则B的转化率
Ⅱ. 已知可逆反应:
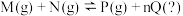 请回答下列问题:
请回答下列问题:(5)在某温度下,反应物的起始浓度分别为:
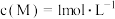 ,
,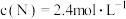 ;
; 后达到平衡,
后达到平衡, 的转化率为
的转化率为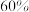 ,此时
,此时 的转化率为
的转化率为(6)若其他条件不变,加热后P的质量分数减少,则正反应是
(7)若其他条件不变,增大压强时,如果平衡不发生移动,则Q是
您最近一年使用:0次
8 . 运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g) H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式_________________ 。
(2)已知在400℃时,N2(g)+3H2(g) 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①在400℃时,2NH3(g) N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=______ (填数值)。
②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v正(N2)_____ v逆(N2)(填“>”、“<”“=”或“不能确定”)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡_____ 移动(填“向左”、“向右”或“不”);加入催化剂,反应的ΔH_______ (填“增大”、“减小”或“不改变”)。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)
 H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式(2)已知在400℃时,N2(g)+3H2(g)
 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。①在400℃时,2NH3(g)
 N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v正(N2)
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
您最近一年使用:0次
9 . 在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g) NH3(g) △H<0。
NH3(g) △H<0。
(1)当反应达到平衡时,N2和H2的浓度比是___ ;N2和H2的转化率比是___ 。反应的化学平衡常数K表达式为___ 。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___ ,密度___ 。(填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将___ (填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将___ (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度____ (填“大于”“小于”或“等于”)原来的2倍。
(5)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图象如图所示:则下列说法符合该图象的是____ 。

A.t1时刻,增大了N2的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
 NH3(g) △H<0。
NH3(g) △H<0。(1)当反应达到平衡时,N2和H2的浓度比是
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
(5)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图象如图所示:则下列说法符合该图象的是

A.t1时刻,增大了N2的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
您最近一年使用:0次
名校
10 . 一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g) CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=__ ;根据图,升高温度,K值将__ (填“增大”、“减小”或“不变”)。
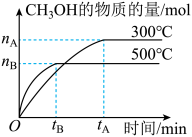
(2)500℃时,从反应开始到化学平衡状态,以H2的浓度变化表示的化学反应速率是__ (用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是__ (填字母,下同)。
a.υ生成(CH3OH)=υ消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是____ 。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时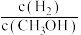 减小
减小
 CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。(1)该反应的平衡常数表达式K=

(2)500℃时,从反应开始到化学平衡状态,以H2的浓度变化表示的化学反应速率是
(3)判断该可逆反应达到化学平衡状态的标志是
a.υ生成(CH3OH)=υ消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的
 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时
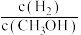 减小
减小
您最近一年使用:0次
2019-11-26更新
|
648次组卷
|
22卷引用:四川省苍溪实验中学校2020-2021学年高二上学期期中质量检测化学试题
四川省苍溪实验中学校2020-2021学年高二上学期期中质量检测化学试题四川省广元市八二一中学2021-2022学年高二上学期期中考试化学试题2015-2016学年湖南省常德一中高二上学期期末理化学试卷2017届广东省韶关市六校高三上10月联考化学试卷辽宁省瓦房店市高级中学2016-2017学年高一6月基础知识竞赛化学试题山西省朔州市第一中学2017-2018学年高二8月月考化学试题2018-2019学年鲁科版高中化学选修四:第2章检测题山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】内蒙古集宁一中(西校区)2018-2019学年高二上学期第一次月考理科综合化学试题山东省济宁市邹城市兖矿第一中学2018-2019学年高二上学期期中模拟考化学试题新疆乌鲁木齐市二十三中学2018-2019学年高二10月月考化学试题山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题重庆市北碚区2019-2020学年高二11月联合性测试化学试题福建省建瓯市芝华中学2019-2020学年高二上学期期中考试化学(1-2班)试题内蒙古自治区通辽市开鲁县第一中学2019-2020学年高一下学期期末考试化学试题河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学试题(普通版)(已下线)第10单元 化学反应速率与化学平衡(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题湖北省黄冈麻城市第二中学2021届高三上学期第一次质量检测化学试题安徽省安庆市九一六学校2020-2021学年高二3月月考化学试题新疆疏勒县实验学校2021-2022学年高二上学期期末考试化学试题陕西省渭南市华州区咸林中学2023-2024学年高二上学期第二次月考化学试卷



