1 . 近年来,雾霾已经给人类的生产生活带来了极大的危害。据分析,雾霾主要成分为灰尘、SO2、NOx、有机碳氢化合物等粒子。据研究,烟气脱硝是治理雾霾的方法之一。
Ⅰ.可用氨气作为脱硝剂,其脱硝原理是NH3与NO反应生成两种无毒的物质。
已知:①2NO(g)=N2(g)+O2(g) ∆H=a kJ•mol-1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ∆H=b kJ•mol-1
(1)写出该氨气脱硝反应的热化学反应方程式:___________ 。
Ⅱ.臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为:2NO2(g)+O3(g) N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
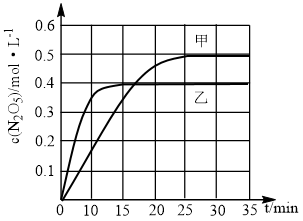
(2)T1___________ T2(填“<”或“>”或“无法确定”),该反应的△H___________ 0(填“<”“>”)
(3)在恒温恒容条件下,下列条件能够证明该反应已经达到平衡的是___________ 。
a.混合气体密度不再改变 b.消耗2n mol NO2的同时,消耗了n mol O3
c.O2浓度不再改变 d.混合气体的平均相对分子质量不再改变
e.容器内混合气体压强不再改变 f.2υ正(NO2)=υ逆(O2)
(4)其他条件一定,且反应时间相同,NO2的转化率与温度、压强的关系如图所示。据此,回答下列问题:

①p1___________ p2,(填“<”或“>”或“无法确定”);
②a点的正逆反应速率的关系为:υa正___________ υa逆(填“<”或“>”或“无法确定”)
Ⅰ.可用氨气作为脱硝剂,其脱硝原理是NH3与NO反应生成两种无毒的物质。
已知:①2NO(g)=N2(g)+O2(g) ∆H=a kJ•mol-1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ∆H=b kJ•mol-1
(1)写出该氨气脱硝反应的热化学反应方程式:
Ⅱ.臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为:2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:| 容器 | 甲 | 乙 |
| 容积/L | 1 | 1 |
| 温度/K | T1 | T2 |
| 起始充入量 | 1 mol O3和2 mol NO2 | 1 mol O3和2 mol NO2 |

(2)T1
(3)在恒温恒容条件下,下列条件能够证明该反应已经达到平衡的是
a.混合气体密度不再改变 b.消耗2n mol NO2的同时,消耗了n mol O3
c.O2浓度不再改变 d.混合气体的平均相对分子质量不再改变
e.容器内混合气体压强不再改变 f.2υ正(NO2)=υ逆(O2)
(4)其他条件一定,且反应时间相同,NO2的转化率与温度、压强的关系如图所示。据此,回答下列问题:

①p1
②a点的正逆反应速率的关系为:υa正
您最近一年使用:0次
解题方法
2 . 请回答下列问题:
(1)已知反应mA(g)+nB(g) pC(g)+qD(g),当反应达到平衡后,改变某一反应条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变某一反应条件,其反应速率的变化曲线分别如图所示。

i.①表示改变压强的方式是___________ (“增大”、“减小”或“不变”,下同),化学平衡___________ 移动(填“正向”“逆向”“不”,下同),m+n___________ p+q(填“>”“<”或“=”,下同)。
ii.②表示改变温度的方式是___________ (“升温”、“降温”或“不变”),化学平衡___________ 移动,该反应逆反应为___________ (吸热或放热)反应。
iii.③表示改变压强的方式是___________ ,化学平衡___________ 移动,m+n___________ p+q。
(2)温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,回答下列问题:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,回答下列问题:
①反应在前50 s~250 s内的用PCl5表示平均速率为___________
②该反应的平衡常数K=___________ 。
③体系平衡时与反应起始时的压强之比为___________
④其它条件均不变,在上述平衡体系中再加入1.0 mol PCl5,达到新平衡时n(PCl3)___________ 0.4 mol(填>,<,=)
⑤相同温度下,起始时向容器中充入0.6 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)___________ v(逆)(填>,<,=)
(1)已知反应mA(g)+nB(g)
 pC(g)+qD(g),当反应达到平衡后,改变某一反应条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变某一反应条件,其反应速率的变化曲线分别如图所示。
i.①表示改变压强的方式是
ii.②表示改变温度的方式是
iii.③表示改变压强的方式是
(2)温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)
 PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,回答下列问题:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,回答下列问题:| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
①反应在前50 s~250 s内的用PCl5表示平均速率为
②该反应的平衡常数K=
③体系平衡时与反应起始时的压强之比为
④其它条件均不变,在上述平衡体系中再加入1.0 mol PCl5,达到新平衡时n(PCl3)
⑤相同温度下,起始时向容器中充入0.6 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)
您最近一年使用:0次
解题方法
3 . 醛类物质的用途广泛。如,甲醛蒸气可对空气消毒、甲醛溶液可用于生物标本的防腐等;脂肪醛类一般具有麻醉、催眠作用等。回答下列问题:
Ⅰ. 与
与 反应用
反应用 催化的机理如图所示。
催化的机理如图所示。
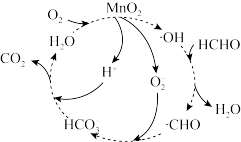
(1)在 ,催化下,
,催化下, 转化成
转化成 ,
, 被氧化成
被氧化成___________ (填离子符号)。
(2)该催化反应的总反应方程式为___________ 。
(3)已知 的两步电离常数分别为
的两步电离常数分别为 、
、 ,当溶液中
,当溶液中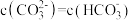 时,溶液
时,溶液
___________ 。
Ⅱ.利用乙二醛 催化氧化法合成乙醛酸的反应原理为:
催化氧化法合成乙醛酸的反应原理为:

可能发生副反应有: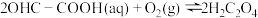 (草酸)
(草酸)
在反应瓶内加入含 (乙二醛)的反应液
(乙二醛)的反应液 ,加热至45~60℃,通入氧气并保持氧气压强为
,加热至45~60℃,通入氧气并保持氧气压强为 ,反应
,反应 达平衡状态,得到的混合液中含
达平衡状态,得到的混合液中含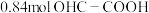 (乙醛酸),
(乙醛酸), (草酸),
(草酸),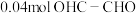 (乙二醛)(溶液体积变化可忽略不计)。
(乙二醛)(溶液体积变化可忽略不计)。
(1)草酸的平均生成速率为___________  。
。
(2)通过化学反应原理分析,增大压强有利于加快反应速率,对于乙二醛的转化率的影响是___________ (填“增大”或“减小”)。
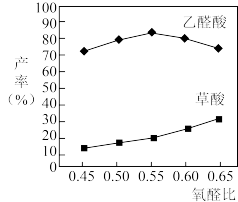
(3)如图所示为起始时氧醛比[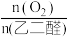 ]对乙醛酸产率的影响,则选择最佳氧醛比为
]对乙醛酸产率的影响,则选择最佳氧醛比为___________ 。
(4)已知: 为二元弱酸,
为二元弱酸,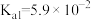 ,
,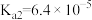 ,向
,向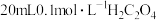 溶液中滴加
溶液中滴加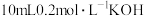 溶液。溶液中
溶液。溶液中
___________  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
Ⅰ.
 与
与 反应用
反应用 催化的机理如图所示。
催化的机理如图所示。
(1)在
 ,催化下,
,催化下, 转化成
转化成 ,
, 被氧化成
被氧化成(2)该催化反应的总反应方程式为
(3)已知
 的两步电离常数分别为
的两步电离常数分别为 、
、 ,当溶液中
,当溶液中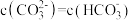 时,溶液
时,溶液
Ⅱ.利用乙二醛
 催化氧化法合成乙醛酸的反应原理为:
催化氧化法合成乙醛酸的反应原理为:
可能发生副反应有:
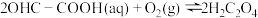 (草酸)
(草酸)在反应瓶内加入含
 (乙二醛)的反应液
(乙二醛)的反应液 ,加热至45~60℃,通入氧气并保持氧气压强为
,加热至45~60℃,通入氧气并保持氧气压强为 ,反应
,反应 达平衡状态,得到的混合液中含
达平衡状态,得到的混合液中含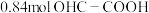 (乙醛酸),
(乙醛酸), (草酸),
(草酸),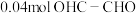 (乙二醛)(溶液体积变化可忽略不计)。
(乙二醛)(溶液体积变化可忽略不计)。(1)草酸的平均生成速率为
 。
。(2)通过化学反应原理分析,增大压强有利于加快反应速率,对于乙二醛的转化率的影响是
(3)如图所示为起始时氧醛比[
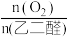 ]对乙醛酸产率的影响,则选择最佳氧醛比为
]对乙醛酸产率的影响,则选择最佳氧醛比为
(4)已知:
 为二元弱酸,
为二元弱酸,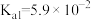 ,
,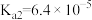 ,向
,向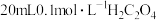 溶液中滴加
溶液中滴加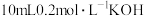 溶液。溶液中
溶液。溶液中
 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
您最近一年使用:0次
4 . (1)高炉炼铁是CO气体的重要用途之一,其基本反应为: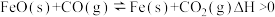 。已知在1100℃时,该反应的化学平衡常数K=0.263。
。已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值__________ (填“增大”“减小”或“不变”)。
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO) =0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?_____ (填“是”或“否”),其判断依据是_____ 。
(2)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g) +3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.0kJ/mol。现向体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
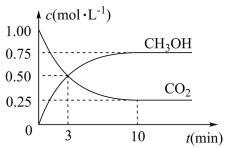
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____ 。
②下列措施能使 增大的是大的是
增大的是大的是______ (填字母)。
A.升高温度 B.再充入H2 C.再充入CO2 D.将H2O从体系中分离 E.充入氦气使体系压强增大
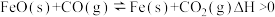 。已知在1100℃时,该反应的化学平衡常数K=0.263。
。已知在1100℃时,该反应的化学平衡常数K=0.263。①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO) =0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?
(2)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g) +3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.0kJ/mol。现向体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施能使
 增大的是大的是
增大的是大的是A.升高温度 B.再充入H2 C.再充入CO2 D.将H2O从体系中分离 E.充入氦气使体系压强增大
您最近一年使用:0次
2020-11-14更新
|
127次组卷
|
2卷引用:天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题



