1 . 在容积2L的刚性容器中充入1molX和2molY,发生反应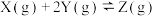 ,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
(用压强计算平衡常数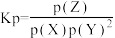 ;分压=总压×物质的量分数)
;分压=总压×物质的量分数)
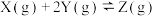 ,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是
,正反应为放热反应,反应过程中测得容器内压强的变化如表所示。下列说法正确的是| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
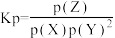 ;分压=总压×物质的量分数)
;分压=总压×物质的量分数)| A.20min后,增大压强,反应速率增大且v(逆)>v(正) |
| B.20min内Y转化率为50% |
| C.25min时,再向容器中通入X、Z各1mol,平衡不移动 |
D.该温度下平衡常数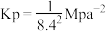 |
您最近一年使用:0次
名校
解题方法
2 . 乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g) ⇌C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L]。下列分析不正确的是
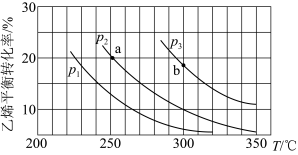

| A.乙烯气相直接水合反应的ΔH>0 |
| B.图中压强的大小关系为p1>p2>p3 |
C.图中a点对应的平衡常数的数值K= |
| D.达到平衡状态a、b所需要的时间:a>b |
您最近一年使用:0次
名校
3 . 用CO还原 可减轻汽车尾气对空气的污染,该反应的热化学方程式为:
可减轻汽车尾气对空气的污染,该反应的热化学方程式为: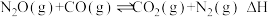 。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol
。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol 和0.4molCO,测得容器中
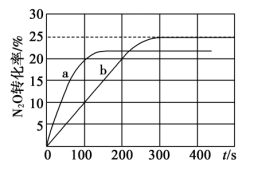
和0.4molCO,测得容器中 转化率随时间变化关系如图。下列说法正确的是
转化率随时间变化关系如图。下列说法正确的是
 可减轻汽车尾气对空气的污染,该反应的热化学方程式为:
可减轻汽车尾气对空气的污染,该反应的热化学方程式为: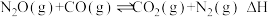 。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol
。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol 和0.4molCO,测得容器中
和0.4molCO,测得容器中 转化率随时间变化关系如图。下列说法正确的是
转化率随时间变化关系如图。下列说法正确的是
A.A容器中 的转化率随时间的变化关系是图中的曲线a 的转化率随时间的变化关系是图中的曲线a |
B.可通过缩小容器体积来缩短b曲线对应容器达到平衡的时间,同时不改变 的平衡转化率 的平衡转化率 |
C.500℃该反应的化学平衡常数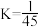 |
D.在平衡后向A容器中加入0.075mol 与0.025mol 与0.025mol ,则平衡正向移动 ,则平衡正向移动 |
您最近一年使用:0次
2022-06-07更新
|
960次组卷
|
3卷引用:湖南省常德市临澧县第一中学2022-2023学年高二上学期第三次月考化学试题
湖南省常德市临澧县第一中学2022-2023学年高二上学期第三次月考化学试题山东省德州市2022届高考三模化学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
解题方法
4 . 恒温恒容条件下,发生反应: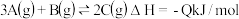 。在3个密闭容器中,按下列方式投入反应物:Ⅰ
。在3个密闭容器中,按下列方式投入反应物:Ⅰ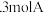 、1molB; Ⅱ
、1molB; Ⅱ 、2molB; Ⅲ
、2molB; Ⅲ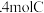 。则在保持恒温恒容反应达到平衡时,下列选项正确的是
。则在保持恒温恒容反应达到平衡时,下列选项正确的是
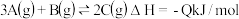 。在3个密闭容器中,按下列方式投入反应物:Ⅰ
。在3个密闭容器中,按下列方式投入反应物:Ⅰ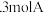 、1molB; Ⅱ
、1molB; Ⅱ 、2molB; Ⅲ
、2molB; Ⅲ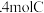 。则在保持恒温恒容反应达到平衡时,下列选项正确的是
。则在保持恒温恒容反应达到平衡时,下列选项正确的是| A.容器Ⅰ与容器Ⅱ中,C的浓度2Ⅰ<Ⅱ |
| B.容器Ⅰ与容器Ⅲ中,反应的能量变化2Ⅰ=Ⅲ |
| C.容器Ⅱ与容器Ⅲ中,转化率Ⅱ+Ⅲ=100% |
| D.容器Ⅰ容器Ⅱ容器Ⅲ中,平衡常数关系为:Ⅰ2 =Ⅱ = Ⅲ-1 |
您最近一年使用:0次
名校
5 . 一定温度下,在3个体积均为1.0L的恒容密闭容器中反应: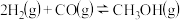 ,达到平衡,下列说法不正确的是。
,达到平衡,下列说法不正确的是。
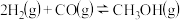 ,达到平衡,下列说法不正确的是。
,达到平衡,下列说法不正确的是。| 容器 | 温度/K | 物质的起始浓度 | 物质的平衡浓度 | ||
 | 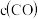 | 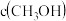 | 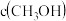 | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A.该反应的正反应为放热反应 |
| B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 |
C.达到平衡时,容器Ⅱ中 大于容器Ⅲ中 大于容器Ⅲ中 的两倍 的两倍 |
| D.达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大 |
您最近一年使用:0次
2021-12-07更新
|
345次组卷
|
2卷引用:河北省邢台市四校联盟2021-2022学年高三12月联考化学试题
6 . 向两个体积可变的密闭容器中均充入1mol的A和2mol的B,发生反应:A2(g)+2B2(g)⇌2AB2(g)ΔH.维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
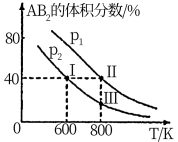
已知:①图中I、II、III点均处于曲线上;②点II时容器的体积为0.1L。下列叙述正确的是

已知:①图中I、II、III点均处于曲线上;②点II时容器的体积为0.1L。下列叙述正确的是
| A.由图象可知:p1<p2 ΔH<0 |
| B.点I时A2的平衡转化率为40% |
| C.点III所对应的反应平衡常数K=0.2 |
| D.将点II所对应的容器冷却到600K,不可能变成点I |
您最近一年使用:0次
名校
解题方法
7 . 可逆反应 ,
, 。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使
。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使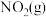 百分含量减小,应采取的措施是
百分含量减小,应采取的措施是
 ,
, 。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使
。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使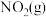 百分含量减小,应采取的措施是
百分含量减小,应采取的措施是| A.增大容器体积 | B.温度体积不变,充入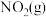 |
C.温度压强不变,充入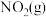 | D.温度体积不变,充入N2O4(g) |
您最近一年使用:0次
2021-01-02更新
|
268次组卷
|
3卷引用:山东省济宁市实验中学2020-2021学年高二上学期10月月考化学试题
名校
8 . 在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g) + 3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
下列说法正确的是( )
 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V(甲) | V(乙) | V(丙) |
| 反应的平衡常数K | K(甲) | K(乙) | K(丙) |
| 平衡时NH3的浓度c/mol·L-1 | c(甲) | c(乙) | c(丙) |
| 平衡时NH3的反应速率 v/mol·L-1·min-1 | v(甲) | v(乙) | v(丙) |
| A.V(甲)>V(丙) | B.K(乙)<K(丙) | C.c(乙)>c(甲) | D.v(甲)=v(丙) |
您最近一年使用:0次
2017-12-02更新
|
540次组卷
|
10卷引用:2015届浙江省嘉兴市一中等五校高三上学期第一次联考化学试卷
2015届浙江省嘉兴市一中等五校高三上学期第一次联考化学试卷2015届浙江省高三第一次五校联考化学试卷2015届江苏省宿迁市三校高三下学期3月质量检测化学试卷2016-2017学年河南省南阳市新野高级中学高二上第二次月考化学卷黑龙江省虎林市高级中学2023-2024学年高二上学期第一次月考化学试题2015-2016学年湖北武汉第二中学高二上期中考试化学试卷江苏省溧阳市2017-2018学年高三第一学期阶段性调研测试化学试题【全国百强校】河北省武邑中学2019届高三上学期第三次调研考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末模拟考试化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过模拟
9 . 在①、②、③容积不等的恒容密闭容器中,均充入0.lmolCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)  CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
下列说法正确的是
 CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示: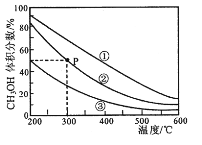
下列说法正确的是
| A.该反应的正反应为放热反应 |
| B.三个容器容积:①>②>③ |
| C.在P点,CO转化率为75% |
| D.在P点,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时 v(CO)正<v (CO)逆 |
您最近一年使用:0次
2017-03-22更新
|
683次组卷
|
5卷引用:江苏省泰州中学2018届高三10月月考化学试题
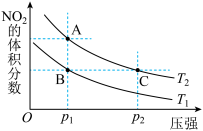
10 . 对反应N2O4(g) 2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
 2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是 
| A.B、C两点的反应速率:B>C |
| B.由状态B到状态A,可以用加热的方法 |
| C.C点颜色比A点深 |
| D.A、C两点的化学平衡常数:A>C |
您最近一年使用:0次



