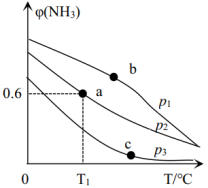
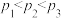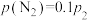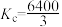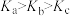一定温度下,在3个体积均为1.0L的恒容密闭容器中反应: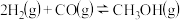 ,达到平衡,下列说法不正确的是。
,达到平衡,下列说法不正确的是。
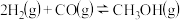 ,达到平衡,下列说法不正确的是。
,达到平衡,下列说法不正确的是。| 容器 | 温度/K | 物质的起始浓度 | 物质的平衡浓度 | ||
 | 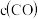 | 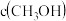 | 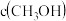 | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A.该反应的正反应为放热反应 |
| B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 |
C.达到平衡时,容器Ⅱ中 大于容器Ⅲ中 大于容器Ⅲ中 的两倍 的两倍 |
| D.达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大 |
更新时间:2021-12-07 09:05:55
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】金属M的盐 ,溶液中存在平衡:
,溶液中存在平衡: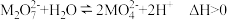 。分别在
。分别在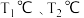 恒温条件下,向
恒温条件下,向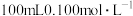 的
的 溶液中加入等量
溶液中加入等量 固体,持续搅拌下用
固体,持续搅拌下用 传感器连续测量溶液的
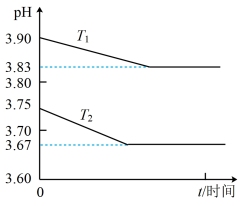
传感器连续测量溶液的 ,得到实验图象,下列说法错误的是
,得到实验图象,下列说法错误的是
 ,溶液中存在平衡:
,溶液中存在平衡: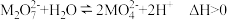 。分别在
。分别在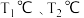 恒温条件下,向
恒温条件下,向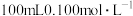 的
的 溶液中加入等量
溶液中加入等量 固体,持续搅拌下用
固体,持续搅拌下用 传感器连续测量溶液的
传感器连续测量溶液的 ,得到实验图象,下列说法错误的是
,得到实验图象,下列说法错误的是
A. |
B. 时平衡常数的数量级是 时平衡常数的数量级是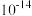 |
C.溶液中存在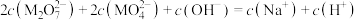 |
D. 温度下,加入 温度下,加入 ,固体再次达到平衡后, ,固体再次达到平衡后,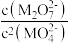 减小 减小 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】已知: ,现在将三个同温、同体积密闭容器编号为甲乙丙,并分别加入①
,现在将三个同温、同体积密闭容器编号为甲乙丙,并分别加入①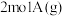 和
和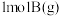 ②
②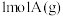 和
和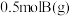 ③
③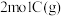 。在恒温,恒容下反应达平衡时,下列关系一定正确的是
。在恒温,恒容下反应达平衡时,下列关系一定正确的是
 ,现在将三个同温、同体积密闭容器编号为甲乙丙,并分别加入①
,现在将三个同温、同体积密闭容器编号为甲乙丙,并分别加入①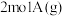 和
和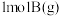 ②
②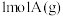 和
和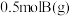 ③
③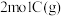 。在恒温,恒容下反应达平衡时,下列关系一定正确的是
。在恒温,恒容下反应达平衡时,下列关系一定正确的是A.容器内压强p: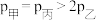 |
B.反应放出或吸收热量的数值Q: |
C.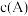 与 与 之比k: 之比k: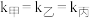 |
D.C的质量m: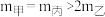 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐3】甲、乙两个密闭容器中均发生反应:C(s)+2H2O(g) CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
下列说法正确的是( )
 CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 平衡 常数 | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2.0 | 4.0 | 3.2 | K1 |
| 乙 | 1 | T2 | 1.0 | 2.0 | 1.2 | K2 |
| A.K1=12.8 |
| B.T1<T2 |
| C.T1℃时向甲容器中再充入0.1 mol H2O(g),则平衡正向移动,CO2(g)的体积分数增大 |
| D.若在T2温度下,向2 L密闭容器中充入1.0 mol CO2和2.0 mol H2,达平衡时,CO2的转化率小于40% |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】硅烷法制备多晶硅的核心反应为2SiHCl3(g) SiH2Cl2(g)+SiCl4(g) △H>0。已知v正=k正•x2(SiHCl3),v逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为各组分的物质的量分数。在恒容密闭容器中加入一定量的SiHCl3,不同温度下速率常数的对数(lgk)如表所示。下列说法错误的是
SiH2Cl2(g)+SiCl4(g) △H>0。已知v正=k正•x2(SiHCl3),v逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为各组分的物质的量分数。在恒容密闭容器中加入一定量的SiHCl3,不同温度下速率常数的对数(lgk)如表所示。下列说法错误的是
 SiH2Cl2(g)+SiCl4(g) △H>0。已知v正=k正•x2(SiHCl3),v逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为各组分的物质的量分数。在恒容密闭容器中加入一定量的SiHCl3,不同温度下速率常数的对数(lgk)如表所示。下列说法错误的是
SiH2Cl2(g)+SiCl4(g) △H>0。已知v正=k正•x2(SiHCl3),v逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为各组分的物质的量分数。在恒容密闭容器中加入一定量的SiHCl3,不同温度下速率常数的对数(lgk)如表所示。下列说法错误的是| 温度/K | 500 | 700 |
| lgk正 | a | b |
| lgk逆 | a+2 | c |
| A.c>b+2 |
| B.升高温度,k正—k逆增大 |
| C.500K时,SiHCl3的平衡转化率为16.67% |
| D.保持温度不变,改变容器体积,x(SiHCl3)及SiHCl3的平衡分压均保持不变 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】已知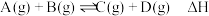 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:
 时,向
时,向 密闭容器中充入
密闭容器中充入 的A和
的A和 的B,反应
的B,反应 时测得C的物质的量
时测得C的物质的量 。下列说法正确的是
。下列说法正确的是
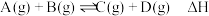 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:温度/ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 时,向
时,向 密闭容器中充入
密闭容器中充入 的A和
的A和 的B,反应
的B,反应 时测得C的物质的量
时测得C的物质的量 。下列说法正确的是
。下列说法正确的是A. 时 时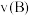 为 为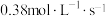 |
B. 达平衡时,A的转化率为 达平衡时,A的转化率为 |
| C.反应达平衡后,升高温度,平衡正向移动 |
D.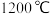 时反应 时反应 的平衡常数的值为2.5 的平衡常数的值为2.5 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g) + 3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
下列说法正确的是( )
 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V(甲) | V(乙) | V(丙) |
| 反应的平衡常数K | K(甲) | K(乙) | K(丙) |
| 平衡时NH3的浓度c/mol·L-1 | c(甲) | c(乙) | c(丙) |
| 平衡时NH3的反应速率 v/mol·L-1·min-1 | v(甲) | v(乙) | v(丙) |
| A.V(甲)>V(丙) | B.K(乙)<K(丙) | C.c(乙)>c(甲) | D.v(甲)=v(丙) |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知2SO2(g)+O2(g)=2SO3(g) ΔH<0)
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 2 mol SO3 | 4 mol SO2、2 mol O2 |
| c (SO3)/(mol·L-1) | c1 | c2 | c3 |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1>c3 | B.2p2>p3 | C.α1=α2 | D.α1<α3 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】汽车尾气净化器中发生的反应为2NO(g)+2CO(g) N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
下列说法正确的是
 N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:| 容器 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||||
| NO | CO | N2 | CO2 | N2 | CO2 | ||
| 甲 | 400 | 0.3 | 0.3 | 0 | 0 | 0.2 | |
| 乙 | 400 | 0.6 | 0.6 | 0 | 0 | ||
| 丙 | 500 | 0 | 0 | 0.15 | 0.3 | 0.08 | |
| A.该反应正反应为放热反应 |
| B.达到平衡时,转化率:α(NO,容器甲)+α(N2,容器丙)<1 |
| C.达到平衡时,体系中c(CO)关系:c(CO,容器乙)<2c(CO,容器甲) |
| D.400℃时,若起始时向容器中充入NO、CO、N2、CO2各0.2 mol,开始时v正<v逆 |
您最近一年使用:0次
【推荐2】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:
CH3OH(g)+CO(g) CH3COOH(g) △H<0。下列说法正确的是
CH3COOH(g) △H<0。下列说法正确的是
CH3OH(g)+CO(g)
 CH3COOH(g) △H<0。下列说法正确的是
CH3COOH(g) △H<0。下列说法正确的是 | 容器编号 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | ||
| c(CH3OH) | c(CO) | c(CH3COOH) | c(CH3COOH) | ||
| I | 530 | 0.50 | 0.50 | 0 | 0.40 |
| II | 530 | 0.20 | 0.20 | 0.40 | |
| III | 510 | 0 | 0 | 0.50 | |
| A.达平衡时,容器I与容器II中的总压强之比为3:4 |
B.达平衡时,容器II中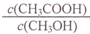 比容器I中的大 比容器I中的大 |
| C.达平衡时,容器Ⅲ中的正反应速率比容器I中的大 |
| D.达平衡时,容器I中CH3OH 转化率与容器III中CH3COOH 转化率之和小于1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应: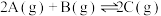 ,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
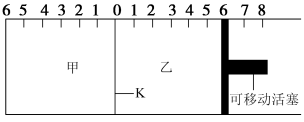
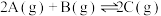 ,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
| A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
| B.达到平衡后,隔板K最终停留在左侧刻度2-0之间 |
| C.若平衡时K停留在左侧1刻度处,则活塞停留在右侧5-6刻度之间 |
| D.若一开始就将K和可移动活塞都固定,其他条件均不变,则达到平衡时甲中A的转化率与乙中C的转化率一定相等 |
您最近一年使用:0次

 和
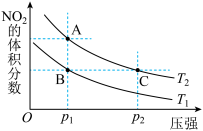
和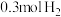 充入密闭容器中反应,平衡后混合物中氨的物质的量分数(φ)随温度、压强变化如图所示。下列说法正确的是
充入密闭容器中反应,平衡后混合物中氨的物质的量分数(φ)随温度、压强变化如图所示。下列说法正确的是