名校
解题方法
1 . 温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1molNO2,发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
 N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。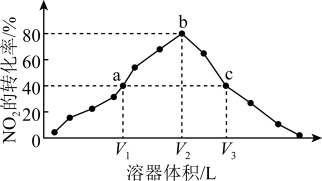
A.T℃时,该反应的化学平衡常数为Kc= mol·L-1 mol·L-1 |
| B.由图可知,c点V正>V逆 |
| C.向a点平衡体系中充入一定量的NO2,达到平衡时,NO2的转化率比原平衡小 |
| D.容器内的压强:pa∶pb=6∶7 |
您最近一年使用:0次
2021-09-06更新
|
1450次组卷
|
16卷引用:重庆育才中学2022届高考适应性考试二化学试题
重庆育才中学2022届高考适应性考试二化学试题江西省抚州市临川一中、临川一中实验学校2022届高三第一次月考化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题河北省保定市定州市2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题四川省成都市树德中学2021-2022学年高二上学期11月阶段性测试(期中)化学试题 山西省长治市第二中学2021-2022学年高三上学期第三次练考化学试题安徽省六安市第一中学2022届高三上学期第三次月考化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期期中考试化学试题广东省梅州市蕉岭县蕉岭中学2022-2023学年高三上学期高二第二次质检化学试题(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)易错点4化学反应速率、平衡图像分析错误(已下线)题型24 化学反应平衡常数、平衡转化率图像福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题
2 . CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为CO(g)+2H2(g)  CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
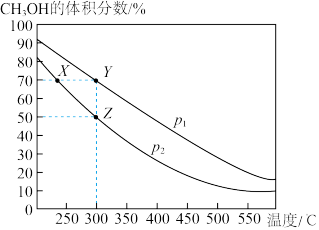
 CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
| A.p1<p2 | B.该反应的ΔH>0 |
| C.平衡常数:K(X)=K(Y) | D.在Z点时,CO转化率为75% |
您最近一年使用:0次
2022-04-11更新
|
349次组卷
|
23卷引用:福建省龙海第二中学2021届高三上学期第三次月考试题(1月)化学试题
福建省龙海第二中学2021届高三上学期第三次月考试题(1月)化学试题北京市通州区2021届高三一模化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题北京师大附中2017-2018学年上学期高二年级期中考试化学试卷云南省民族大学附属中学2019届高三上学期期中考试化学试题内蒙古北方重工业集团有限公司第三中学2019-2020学年高二10月月考化学试题湖北省武汉市汉阳一中2019-2020学年高二9月月考化学试题人教版选修四2019-2020学年高二上学期期末复习化学综合训练福建省漳州市龙海市第二中学2020届高三上学期第二次月考化学试题甘肃省张掖市第二中学2020届高三上学期11月月考化学试题江西省赣州市会昌中学2019-2020学年高二上学期第二次月考化学试题河北省衡水中学2020届高三上学期第四次调研考试化学试题【省级联考】浙江省2019—2020学年普通高校招生选考科目化学模拟试题(已下线)《2020年新高考政策解读与配套资源》模拟试题11-2020年北京新高考化学模拟试题河南省实验中学2020-2021学年高二上学期期中考试化学试题江西省景德镇一中2020-2021学年高二上学期期中考试化学(2班)试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期12月月考化学试题江西省南昌市第三中学2020~2021学年高二上学期期中考试化学试题山西省运城市芮城中学2021-2022学年高二上学期12月月考化学试题广东省汕头市金山中学2021-2022学年高二上学期期末考试化学试题广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题
解题方法
3 . 一定条件下,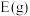 和
和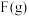 反应生成
反应生成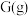 和
和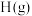 达到平衡,平衡常数
达到平衡,平衡常数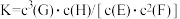 ,且温度升高K值变大。下列说法错误的是
,且温度升高K值变大。下列说法错误的是
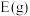 和
和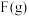 反应生成
反应生成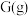 和
和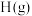 达到平衡,平衡常数
达到平衡,平衡常数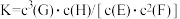 ,且温度升高K值变大。下列说法错误的是
,且温度升高K值变大。下列说法错误的是A.该反应的化学方程式为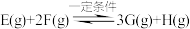 |
B.该反应的 |
| C.该反应在低温下能自发进行 |
D.恒温恒容条件下,增大压强,平衡时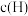 可能不变 可能不变 |
您最近一年使用:0次
名校
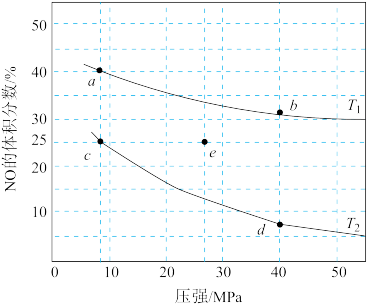
4 . 反应2NO(g) + 2CO(g) N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
 N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
| A.温度:T1>T2 |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
您最近一年使用:0次
2022-10-13更新
|
305次组卷
|
10卷引用:黑龙江省嫩江市高级中学2021届高三上学期模拟考试化学试题
黑龙江省嫩江市高级中学2021届高三上学期模拟考试化学试题北京市朝阳区2020届高三学业水平等级性考试练习化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:化学平衡 离子平衡上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题上海行知中学2022-2023学年高三上学期第一次月考化学试题甘肃省张掖市高台县第一中学2022-2023学年高二上学期期中考试化学试题河南省鹤壁市高中2022-2023学年高三上学期第三次模拟考试化学试题河南省汝州市第一高级中学2022-2023学年高二上学期11月月考化学试题甘肃省张掖市高台县第一中学2023-2024学年高二上学期开学(暑假学习效果)检测化学试题河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题
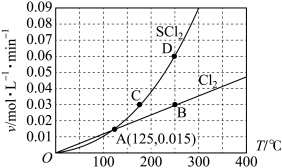
5 . 一定压强下,向 10 L 密闭容器中充入 1 mol S2Cl2和 1 mol Cl2,发生反应 S2Cl2(g)+Cl2(g) 2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
 2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
| A.正反应的活化能大于逆反应的活化能 |
| B.达到平衡后再加热,平衡向逆反应方向移动 |
| C.A、B、C、D 四点对应状态下,达到平衡状态的为 B、D |
| D.一定温度下,在恒容密闭容器中,达到平衡后缩小容器体积,重新达到平衡后,Cl2的平衡转化率不变 |
您最近一年使用:0次
2021-03-26更新
|
158次组卷
|
4卷引用:浙江省湖州市德清县第三中学2020-2021学年高二下学期返校考试化学试题
名校
6 . 25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.方程式为X+3Y⇌2Z,平衡常数为1600 |
| C.增大压强使平衡正向方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
2021-12-29更新
|
223次组卷
|
11卷引用:河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题
河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题(已下线)第二章 第三节化学平衡(第3课时 化学平衡常数)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期12月月考化学试题河南省范县第一中学等学校2021-2022学年高二上学期联考检测化学试题 广西玉林市市直六所普通高中2021-2022学年高二上学期期中考试理科综合化学试题河南省安阳市滑县实验学校2020-2021学年高二上学期期中考试化学试题(普通班)内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题
7 . 甲醇水蒸气重整制氢具有能耗低、产物组成简单、副产物易分离等优点,是未来制氢技术的重要发展方向。该重整反应体系主要涉及以下反应:
I.CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H1
CO2(g)+3H2(g) △H1
II.CH3OH(g) CO(g)+2H2(g) △H2=+90kJ•mol-1
CO(g)+2H2(g) △H2=+90kJ•mol-1
(1)已知CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1
反应I的△H1=___ kJ•mol-1。
(2)将组成(物质的量分数)为25%CH3OH(g)、35%H2O(g)和40%N2(g)(N2不参与反应)的气体通入恒容容器中反应相同时间,测得CH3OH转化率和产物的物质的量分数随温度变化关系如图所示。
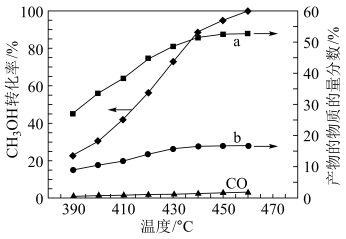
①曲线a和b分别代表产物___ 和___ 。
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有___ 。
A.增大N2的浓度,反应I、II的正反应速率都增加
B.移除CO2能提高CH3OH的平衡转化率
C.升高温度,N2的物质的量分数保持不变
D.440℃~460℃时,升高温度,H2的产率增大
③反应I活化能小于反应II,结合图中信息解释判断依据___ 。
(3)一定条件下,向2L的恒容密闭容器中通入1molCH3OH(g)和1molH2O(g)发生上述反应,达到平衡时,容器中CO2为0.8mol,CO为0.1mol,此时H2的浓度为___ mol•L-1,反应I的平衡常数K=___ (写出计算式)。
(4)研究发现以铜作催化剂时,反应I经历三步:
①CH3OH→HCHO+H2,
②HCHO+H2O→HCOOH+H2,
③___ 。
I.CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H1
CO2(g)+3H2(g) △H1II.CH3OH(g)
 CO(g)+2H2(g) △H2=+90kJ•mol-1
CO(g)+2H2(g) △H2=+90kJ•mol-1(1)已知CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1反应I的△H1=
(2)将组成(物质的量分数)为25%CH3OH(g)、35%H2O(g)和40%N2(g)(N2不参与反应)的气体通入恒容容器中反应相同时间,测得CH3OH转化率和产物的物质的量分数随温度变化关系如图所示。

①曲线a和b分别代表产物
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有
A.增大N2的浓度,反应I、II的正反应速率都增加
B.移除CO2能提高CH3OH的平衡转化率
C.升高温度,N2的物质的量分数保持不变
D.440℃~460℃时,升高温度,H2的产率增大
③反应I活化能小于反应II,结合图中信息解释判断依据
(3)一定条件下,向2L的恒容密闭容器中通入1molCH3OH(g)和1molH2O(g)发生上述反应,达到平衡时,容器中CO2为0.8mol,CO为0.1mol,此时H2的浓度为
(4)研究发现以铜作催化剂时,反应I经历三步:
①CH3OH→HCHO+H2,
②HCHO+H2O→HCOOH+H2,
③
您最近一年使用:0次
2021-12-22更新
|
430次组卷
|
3卷引用:广东省广州市2021-2022学年高三上学期12月调研考试化学试题
广东省广州市2021-2022学年高三上学期12月调研考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省茂名高州市2021-2022学年高二上学期期末考试化学试题
8 .  法是工业上消除氮氧化物的常用方法,反应如下:
法是工业上消除氮氧化物的常用方法,反应如下:
主反应:
副反应:
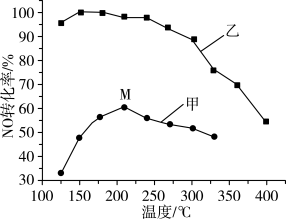
相同条件下,在甲、乙两种催化剂作用下进行上述反应,下列说法错误的是
 法是工业上消除氮氧化物的常用方法,反应如下:
法是工业上消除氮氧化物的常用方法,反应如下:主反应:

副反应:

相同条件下,在甲、乙两种催化剂作用下进行上述反应,下列说法错误的是

| A.工业上选择催化剂乙的原因是低温下有很强的催化活性 |
B.投料比一定时有利于提高 平衡转化率的反应条件是降低温度、减少压强 平衡转化率的反应条件是降低温度、减少压强 |
C.图中M点处(对应温度为210℃) 的转化率一定不是该温度下的平衡转化率 的转化率一定不是该温度下的平衡转化率 |
D.相同条件下选择高效催化剂,可以提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
2021-03-12更新
|
1467次组卷
|
11卷引用:山东省济宁市2021届高三3月模拟(一模)化学试题
山东省济宁市2021届高三3月模拟(一模)化学试题山东省济南市2021届高三4月阶段性检测化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题09 反应速率、化学平衡-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
9 . 如图,I是恒压密闭容器,II是恒容密闭容器。其它条件相同时,在I、II中分别加入2molX和2molY,起始时容器体积均为VL,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是

 aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:II>I |
| B.a值为2 |
| C.若X为固态,Y为气态,则I、II中从起始到平衡所需时间相同 |
| D.平衡时I容器的体积小于VL |
您最近一年使用:0次
10 . 某恒定温度下,在一个2L的密闭容器中充入A气体,B气体,测得其浓度分别为2mol/L和1mol/L,且发生如下反应:3A(g)+2B(g) 4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
①该反应用C表示反应速率为1.2mol/(L•min)
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
 4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是①该反应用C表示反应速率为1.2mol/(L•min)
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
| A.①② | B.②③ | C.①④ | D.③④ |
您最近一年使用:0次



